
| A、Ca2+、Mg2+的总含量 |
| B、Ca2+的含量 |
| C、Mg2+的含量 |
科目:高中化学 来源: 题型:

| 序号 | 反应 | 平衡常数 |
| 1 | Au+6HNO3(浓)═Au(NO3)3+3NO2↑+3H2O | <<1 |
| 2 | Au3++4Cl-═AuCl4- | K |
查看答案和解析>>
科目:高中化学 来源: 题型:

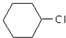 为原料合成重要的化工产品
为原料合成重要的化工产品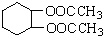 的路线流程图(无机试剂任选)合成路线流程图示例如图2.
的路线流程图(无机试剂任选)合成路线流程图示例如图2.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用焰色反应鉴别氯化钠固体和氢氧化钠固体 |
| B、用丁达尔效应鉴别NaCl溶液和KCl溶液 |
| C、用AgNO3溶液鉴别NaCl溶液和Na2SO4溶液 |
| D、用萃取法鉴别溴水和碘水 |
查看答案和解析>>
科目:高中化学 来源: 题型:


| 400℃ |
| 约1250℃ |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同浓度下列溶液中:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl④NH3?H2O,C(NH4+)由大到小的顺序是:①>③>②>④ |
| B、常温时,将等体积的盐酸和氨水混合后,pH=7,则C(NH4+)>C (Cl-) |
| C、0.2 mol/LNa2CO3溶液中:C (OH-)=C (HCO3-)+C (H+)+C (H2CO3) |
| D、同浓度的下列溶液中,①NaCl ②Na2CO3 ③CH3COONa④NaOH,pH值由大到小的顺序是:④>③>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在潮湿的酸性土壤中 |
| B、在潮湿不透气的中性土壤中 |
| C、在干燥致密不透气的土壤中 |
| D、在潮湿透气的盐碱地中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在含大量Al3+的溶液中:NH4+、Na+、HCO3-、SO42- |
| B、能使甲基橙试液变红的溶液中:Na+、K+、MnO4-、NO3- |
| C、在水电离出的c(H+)=10-13mol?L-1 的溶液中:NH4+、[Al(OH)4]-、SO42-、NO3- |
| D、在pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙酸乙酯和水,酒精和水,植物油和水 |
| B、甘油和水,乙酸和水,乙酸和乙醇 |
| C、四氯化碳和水,溴苯和水,硝基苯和水 |
| D、汽油和水,苯和水,乙醛和水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com