
【题目】离子液体在有机合成、无机合成等方面有着重要应用。咪唑是合成“离子液体”的一种原料,其结构如图所示。下列有关咪唑说法不正确的是
![]()
A. 化学式C3H4N2
B. 分子中含有一种非极性键和两种极性键
C. 可以发生取代、加成、氧化反应
D. 一氯取代物的同分异构体共有4种
科目:高中化学 来源: 题型:
【题目】(1)普鲁士蓝的化学式为Fe4[Fe(CN)6]3,该物质中存在的化学键有离子键、
_____和_____;含有的Fe3+的核外电子排布式为______。
(2)KCN可被H2O2氧化为KOCN
①KOCN可作为制药原料,其晶体类型是____;碳原子采取sp杂化,1mol该物质中含有的π键数目为______。含有的三种非金属元素的电负性由大到小的顺序是______。
②H2O2常温下是液体,沸点较高(150℃),其主要原因是______。
(3)成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如下左图,As原子的杂化方式为___,雌黄和SnCl2在盐酸中反应转化为雌黄(As4S4)和SnCl4,SnCl4分子的空间构型为______。

(4)某晶体的晶胞结构如上右图所示,该晶体的化学式为_____,该晶胞参数为a=250.4pm,c=666.1pm,y=120o;1号原子坐标为(0,0,0),2号原子坐标为(1/3,2/3,0),则3号原子坐标为_____,计算上述晶体中A和B两原子间的最小核间距为____。(保留四位有效数字。已知![]() =1.141,
=1.141, ![]() =1.732.)
=1.732.)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质属于同位素的是___________,属于同分异构体的是_________,属于同一物质的是__________。
(1)O2和O3
(2)3517Cl和3717Cl
(3)CH3CH3和CH3CH2CH2CH3
(4)金刚石和石墨
(5)氕、氘、氚
(6)CH3CH2CH2CH(CH3)CH2CH3和CH3CH2CH(CH3)CH(CH3)CH3
(7)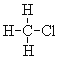 和
和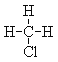
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10molL-1NaOH溶液分别滴定20.00mL浓度均为0.10molL-1CH3COOH溶液和HCN溶液所得滴定曲线如下图。下列说法正确的是

A.点①和点②所示溶液中:c(CH3COO-)<c(CN-)
B.点③和点④所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
C.点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
D.点②和点③所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的回收利用是环保和能源领域研究的热点课题。
(1)新的研究表明,利用太阳能可以将CO2分解制取炭黑,其原理如右图所示。该过程的能量转化形式为______,在整个过程中,FeO的作用是_________。
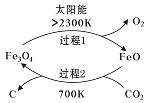
已知:
①2Fe2O4(s)=6FeO(s)+O2(g) ΔH=akJ/mol
②C(s)+O2(g)=CO2(g) ΔH=bKJ/mol 则过程2的热化学方程式为________。
(2)一定温度下,在密闭容器中进行反应CO2(g)+CH4(g)![]() 2CO(g)+2H2(g) ΔH>0,下列说法正确的是________。
2CO(g)+2H2(g) ΔH>0,下列说法正确的是________。
A.当混合气体的平均相对分子质量不变时,反应达到平衡状态
B.升高温度,加快反应速率,CO2的转化率降低
C.增大CO2的浓度,平衡向正反应方向移动,平衡常数增大
D.平衡时CO、H2的体积分数不一定相等
(3)在2L恒容密闭容器中充入2molCO2和nmolH2,在一定条件下发生反应CO2(g)+3H2(g)![]() CH3COOH(g)+H2O(g),CO2的转化率与温度、投料比
CH3COOH(g)+H2O(g),CO2的转化率与温度、投料比![]() 的关系如右图所示。
的关系如右图所示。
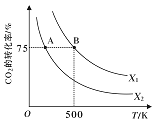
①若从反应开始到A点需要10s,则V(H2)= _____。
②该反应的平衡常数表达式为______,若X1=3,则B点的K=___________。
③根据图像判断X1 ____X2(填“>”、“<”或“=”,下同),平衡常数KA ___KB。
④若在500K时,按X1投料,在恒压下进行,达到平衡状态,此时CO2的转化率______75%(填“>”、“<”或“=”)
(4)美国伊利诺大学芝加哥分校(UIC)的研究团队设计出一种突破性的新太阳能电池,能把大气中的二氧化碳转换成碳氢化合物(hydrocarbon)燃料,解决了现代社会的两大挑战:“减少大气的碳含量”以及“有效率地制造高密度能源”。右图是通过CO2和H2O作用制备CH3OH的原理示意图。
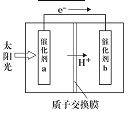
①a电极的名称_________,电极产物___________。
②b电极的电极反应为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向仅含Fe2+、I-、Br-的溶液中通入适量氯气,溶液中这三种离子的物质的量随消耗氯气物质的量的变化如图所示.下列说法中不正确的是( )

A. 线段Ⅲ代表Br-的变化情况
B. a值等于8
C. 线段I代表I-的变化情况
D. 原混合溶液中n(Fe2+)=4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MgH2和Mg2Cu可用作贮氢材料,MgO可用作炉膛内脱硫脱硝的试剂。
(1)MgH2是一种离子化合物,其电子式为_______________。
(2)Mg2Cu在加压条件下储氢时生成MgH2和MgCu2,该反应的化学方程式为_____________。
(3)已知MgH2的有关热化学方程式如下:
MgH2(s) =Mg(s)+H2(g) △H1=+74.4kJ mol-1;
H2(g)+l/2O2(g)=H2O(g) △H2=-241.8 kJ mol-1;
Mg(s)+l/2O2(g)=MgO(s) △H3=-141.6 KJ mol-1。
①氢化镁燃烧生成氧化镁和水蒸气的热化学方程式为______________。
②MgH2作贮氢材料时,单位贮氢材料释放出氢气的质量随时间的变化如图甲所示,其中温度T1、T2、T3由小到大的顺序为__________________。
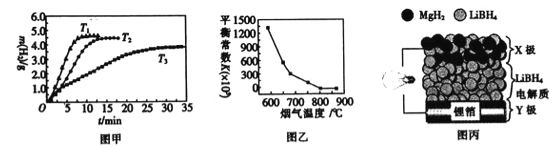
(4)炉膛内脱除 SO2、NO 反应为2MgO(s)+2SO2(g)+2NO(g)![]() 2MgSO4(s)+N2(g) △H =akJ/ mol,其平衡常数与温度的关系如图乙所示。
2MgSO4(s)+N2(g) △H =akJ/ mol,其平衡常数与温度的关系如图乙所示。
①上述反应的平衡常数表达式为K=_________。
②a_________0(填“>”或“,<”)。
(5)全固态锂离子电池的结构如图丙所示,放电时电池反应为2Li+MgH2=Mg+2LiH。放电时,X极的电极反应式为_________。充电时,Y极的电极反应式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑上述反应中能设计成原电池的是______。
(2)将纯锌片和纯铜片按图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是____________。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲_______乙(填“>”、“<“或“=” )
③请写出图中构成原电池的负极电极反应式_________________________。
④当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为____________________。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用氢氧化钠溶液为电解液;则氢气应通入_____________极(填a或b),电子从 __________(填a或b)极流出。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com