
【题目】已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大,X、Z、Q的单质在常温下呈气态;Y的原子最外层电子数是其电子层数的2倍;X与M同主族;Z、G分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)M在元素周期表中的位置为____________。
(2)X 与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分子式)_______,在实验室中,制取该物质的反应原理是(写化学方程:式)________。
(3)MX与水反应可放出气体,该反应的化学方程式为____________。.
(4)常温下不能与G的单质发生反应的是(填序号)_________。
a.CuSO4溶液 b. Fe2O3 c.浓硫酸 d. NaOH溶液 e. Na2CO3固体
(5)工业上若以石墨为电极电解制G的单质,阳极产生混合气体的成分是(写化学式)______。
【答案】 第三周期ⅠA族 C2H2 CaC2+2H2O→Ca(OH)2+C2H2↑ NaH+H2O=NaOH+H2↑ be O2、CO2等
【解析】X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大,Z、G分别是地壳中含量最高的非金属元素和金属元素,则Z为O元素、G为Al元素;Y的原子最外层电子数是其电子层数的2倍,原子序数小于O,只能处于第二周期,最外层电子数为4,则Y为C元素;X单质在常温下呈气态,则X为H元素;X与M同主族,原子序数大于O,则M为Na;Q单质常温下为气态,原子序数大于Al,则Q为Cl。
(1)M为Na,在元素周期表中位于第三周期ⅠA族,故答案为:第三周期ⅠA族;
(2)H与C能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是C2H2,在实验室中,制取该物质的反应原理是:CaC2+2H2O→Ca(OH)2+C2H2↑,故答案为:C2H2;CaC2+2H2O→Ca(OH)2+C2H2↑;
(3)NaH与水反应可放出气体为氢气,同时生成NaOH,该反应的化学方程式为 NaH+H2O=NaOH+H2↑,故答案为:NaH+H2O=NaOH+H2↑;
(4)常温下,Al与硫酸铜溶液反应置换铜,与浓硫酸反应生成致密的氧化物保护膜,发生钝化现象,与氢氧化钠溶液反应生成偏铝酸钠与氢气,不能与氧化铁和碳酸钠反应,故选be;
(5)工业上用电解法制Al的单质的化学方程式是2Al2O3(熔融)![]() 4Al+3O2↑,若以石墨为电极,阳极产生的氧气与碳反应生成二氧化碳或CO,故阳极的混合气体的成分是O2、CO2等,故答案为:O2、CO2等。
4Al+3O2↑,若以石墨为电极,阳极产生的氧气与碳反应生成二氧化碳或CO,故阳极的混合气体的成分是O2、CO2等,故答案为:O2、CO2等。


科目:高中化学 来源: 题型:
【题目】某温度下发生的反应:2C2H2(g)+5O2(g)4CO2(g)+2H2O(g) △H = -2599 kJ·mol-1,下列描述不正确的是
A.该反应是放热反应B.增大c(O2),K增大
C.K随温度升高而减小D.可通过Qc与K之间的大小关系判断反应的移动方向
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的下列溶液:HCl、H2SO4、CH3COOH,导电能力由强到弱的顺序是
A. HCl=H2SO4>CH3COOH B. HCl>H2SO4>CH3COOH
C. H2SO4>HCl>CH3COOH D. HCl=H2SO4=CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:
H2O(g) == H2(g) +1/2 O2(g) △H = +241.8 kJ·mol-1
H2(g)+ 1/2O2(g) == H2O(1) △H = -285.8 kJ·mol-1
当1g液态水变为水蒸气时,其热量变化是
A. 吸热88kJ B. 吸热2.44 kJ C. 放热2.44 kJ D. 吸热44 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲配制250mL0.1molL﹣1的H2SO4溶液,回答下列有关问题,有如下操作步骤:
①把量取好的浓H2SO4沿烧杯壁缓缓倒入盛有一定量水的小烧杯中,并用玻璃棒不断搅拌
②把①中所得溶液小心转入仪器A中
③继续向A中加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入A中,并轻轻摇匀
⑤用玻璃塞将A塞紧,充分摇匀
请填写下列空白: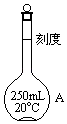
(1)写出图中仪器A的名称 , 使用此仪器A前应检查它是否 .
(2)操作步骤的正确顺序为(填序号) .
(3)转移溶液时,应先将溶液 , 然后将溶液沿玻璃棒注入仪器A中.
(4)若出现下列操作时,对所配溶液浓度将有何影响(填“偏高、偏低、无影响”)
①量筒用蒸馏水冼净后,再量取浓硫酸;
②不将洗涤液转移入仪器A就定容;
③定容时,仰视仪器A刻度线;
④仪器A只用蒸馏水洗涤,但未经干燥而配制溶液 .
(5)若实验过程中出现如下情况应如何处理?
①加蒸馏水时不慎超出了刻度;
②向容量瓶中转移溶液时,不慎有液滴掉在容量瓶外面 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸盐(NaClO2)可作漂白剂,在常温下不见光时可保存一年,但在酸性溶液里因生成
亚氯酸而发生分解:5HClO2=4ClO2↑+H++Cl-+2H2O。分解时,刚加入硫酸,反应缓慢,随后突然反应释放出大量 ClO2,这是因为
A. 酸使亚氯酸的氧化性增强
B. 溶液中的 H+起催化剂的作用
C. 溶液中的 Cl-起催化剂的作用
D. 逸出的 ClO2 使反应的生成物的浓度降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学反应的说法中不正确的是 ( )
A. 化学反应过程中一定有热量释放出来
B. 化学反应的特征是有新物质生成
C. 化学反应的过程实际上是一个旧键断裂、新键形成的过程
D. 在一确定的化学反应关系中,反应物的总能量与生成物的总能量一定不相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com