
【题目】某制药有限公司生产有多种型号的钙尔奇D片剂,为测定某型号片剂中碳酸钙含量,进行如下实验:取10片该片剂碾碎后放入足量的盐酸中充分反应(假设盐酸只与碳酸钙反应)后过滤,取滤液加(NH4)2C2O4使Ca2+生成CaC2O4沉淀,沉淀过滤洗涤后溶解于强酸中并稀释成1L溶液,取20.00mL,然后用0.0500mol·L-1KMnO4溶液滴定,反应中用去12.00mLKMnO4溶液,发生反应的离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
请回答:
(1)该型号片剂中每片含碳酸钙的质量为_____克
(2)该公司一种“钙尔奇D600片剂”(其主要成分与题中某型号的片剂相同,仅仅是碳酸钙的含量不同)的部分文字说明如下:“本品每片含主要成分碳酸钙1.5g(相当于钙元素600mg),成人每天服用1片”。则某型号的片剂应称为“钙尔奇D_____(填数字)片剂。”
【答案】0.75 300
【解析】
由题意可捋出如下关系式:5CaCO3~5Ca2+~5CaC2O4~5H2C2O4~2KMnO4,利用关系式法计算。
(1)每片该钙剂对应消耗KMnO4的物质的量n(KMnO4)=0.0500mol·L-1×12.00mL×10-3×![]() =3×10-3mol,由5CaCO3~2KMnO4得,每片该钙剂中CaCO3的物质的量n(CaCO3)=
=3×10-3mol,由5CaCO3~2KMnO4得,每片该钙剂中CaCO3的物质的量n(CaCO3)=![]() =7.5×10-3mol,所以,每片该钙剂中CaCO3的质量m=7.5×10-3mol×100g/mol=0.75g,故答案为:0.75;
=7.5×10-3mol,所以,每片该钙剂中CaCO3的质量m=7.5×10-3mol×100g/mol=0.75g,故答案为:0.75;
(2)“某型号”钙剂中,每片含CaCO3的质量为0.75g,因为每片含碳酸钙1.5g表示为钙尔奇D600片剂,则“某型号”钙剂表示为:钙尔奇D300片剂,故答案为:300。


科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W在周期表中的相对位置如图所示,其中X、Y、W的最外层电子数之和为15,Z和X的最外层电子数相差2,下列说法正确的是
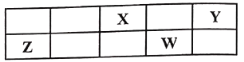
A.原子半径:r(Z)>r(W)>r(Y)>r(X)B.X的氢化物的沸点一定比Y的氢化物的沸点低
C.一定条件下,Z可以置换出XD.X、Y元素的单质均只有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。
根据题意回答下列问题:
①写出酸H2A的电离方程式___。
②若溶液M由2mol/LNaHA溶液与2mol/LNaOH溶液等体积混合而得,则溶液M的pH___7(填“>”“<”或“=”);溶液M中各微粒的浓度关系正确的是___。
A.c(Na+)>c(A2-)>c(H+)>c(OH-)
B.c(HA-)+c(H2A)+c(H+)=c(OH-)
C.c(A2-)+c(HA-)+c(H2A)=1mol/L
D.c(A2-)+c(HA-)+c(OH-)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应X(g) + Y(g) 2Z(g)的能量变化如图所示。下列说法正确的是( )
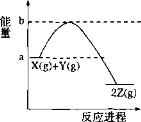
A.1 mol X(g)的能量一定高于1 mol Z(g)的能量
B.该反应一定不需要加热就可以进行
C.升高温度,该反应的正、逆反应速率都加快
D.其他条件不变,若加入催化剂,则反应物的平衡转化率提高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用CO和H2合成再生能源甲醇,反应为:2H2(g)+CO(g)![]() CH3OH(g) ΔH<0
CH3OH(g) ΔH<0
(1)一定温度下,将1molCO与1molH2通入VL恒容密闭容器中发生反应。
①该反应能自发进行的条件是______(填“高温”、“低温”或“任意温度”)
②下列说法正确的是______。
A.v正(H2)=2v逆(CO)时,反应达到化学平衡状态
B.达到平衡时CO与H2的转化率相等
C.恒温恒压,往原料气中通入少量稀有气体,CO的转化率会降低
D.该反应的正反应活化能大于逆反应活化能
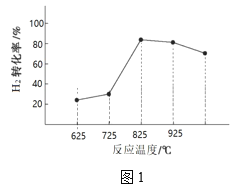
③图1为温度对H2合成甲醇反应的影响,请从反应速率和平衡的角度分析725℃以后H2百分含量随时间增长呈现该变化趋势的原因______。
(2)在恒温T、恒压P的条件下,将3.0molCO与4.5molH2通入容积可变的密闭容器中。达平衡时容器的体积为2L,CO的转化率为50%。
①此反应的正、逆反应速率与浓度的关系为v正=k正c(CO)·c2(H2),v逆=k逆c(CH3OH),其中k正、k逆为速率常数。在温度T下k正、k逆的关系式为k正=_____k逆。
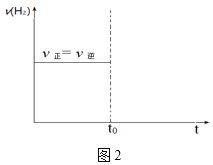
②若平衡时,在t0时刻再向容器中通入9.0molCO,在图2中画出充入CO后的v正、v逆随时间变化的图像_____。
(3)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,请写出生成甲醇的电极反应式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组为探究NO和Cl2O(Cl2O是酸性氧化物,易溶于水)的性质,将两种气体同时通入水中,实验装置如图:
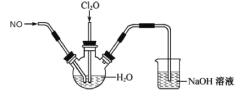
请回答:
(1)三颈瓶中检测到有2种强酸生成,用一个化学方程式表示_____。
(2)该实验装置有一处不合理,请指出_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。
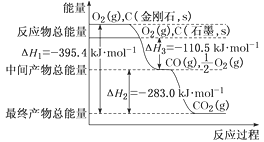
(1)在通常状况下,金刚石和石墨相比较,___(填“金刚石”或“石墨”)更稳定。
(2)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497kJ·mol-1。N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol-1。NO分子中化学键的键能为___kJ·mol-1。
(3)综合上述有关信息,请写出用CO除去NO的热化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应:11P+15CuSO4+24H2O==5Cu3P+6H3PO4+15H2SO4中,7.5 mol CuSO4可氧化磷原子的物质的量为( )
A.1.5 mol B.3 mol C.5 mol D.6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物M的球棍模型如图所示:
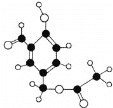
(1)请写出物质M的分子式_______含氧官能团名称_________
(2)M在一定条件下,可以发生水解反应,生成A、B两种物质(它们的相对分子质量关系A>B)。B可以用以下方法制得:X![]() Y
Y![]() Z
Z![]() W
W![]() B。其中W能发生银镜反应。则I属于________反应(填反应类型)
B。其中W能发生银镜反应。则I属于________反应(填反应类型)
(3)写出反应Ⅱ的化学方程式:_____。反应Ⅲ的化学方程式:________。
(4)1molA分别与Na、NaOH溶液反应,所用Na、NaOH物质的量的最大值之比是_______。
(5)A有多种同分异构体,符合下列三个件的同分异构体有_______种,其中分子结构中只有六种氢原子的结构简式为__________
a.环上只有两个取代基
b.与FeCl3溶液显紫色;
c.能发生银镜反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com