
| A、在含Fe2+的溶液中:Cl-、S2-、K+、I- |
| B、在c(H+)=0.01 mol?L-1的溶液中:Cu2+、Br-、SO42-、NH4+ |
| C、在使甲基橙呈红色的溶液中:Mg2+、Cl-、S2O32-、Na+ |
| D、在无色溶液中:Cr2O72-、K+、H+、CH3OH |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 周期表中前36号元素A、B、C、D、E、F、G、H,它们原子序数依次增大,其中B、C、D原子具有相同能层数,A和E同一主族,D和G同一主族,E、F、H是常见金属元素,A与B形成化合物是一种温室气体,D元素原子最外层电子数是次外层电子数的3倍,F元素的离子半径是同一周期形成简单离子中最小的,H原子基态d能级电子总数比P能级电子总数少4.请回答下列问题:
周期表中前36号元素A、B、C、D、E、F、G、H,它们原子序数依次增大,其中B、C、D原子具有相同能层数,A和E同一主族,D和G同一主族,E、F、H是常见金属元素,A与B形成化合物是一种温室气体,D元素原子最外层电子数是次外层电子数的3倍,F元素的离子半径是同一周期形成简单离子中最小的,H原子基态d能级电子总数比P能级电子总数少4.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:
 随着氮氧化物污染的日趋严重,国家将于“十二五”期间加大对氮氧化的排放的控制力度.消除氮氧化物污染有多种方法,其中一种是用活性炭还原法处理氮氧化物,有关反应为:C(s)+2NO(g)?N2(g)+CO2(g)△H>0.
随着氮氧化物污染的日趋严重,国家将于“十二五”期间加大对氮氧化的排放的控制力度.消除氮氧化物污染有多种方法,其中一种是用活性炭还原法处理氮氧化物,有关反应为:C(s)+2NO(g)?N2(g)+CO2(g)△H>0.| 时间/min | 0 | 20 | 40 | 50 |
| c(NO)/mol?L-1 | 0.100 | 0.040 | 0.032 | 0.032 |
| c(N2)/mol?L-1 | 0 | 0.030 | 0.034 | 0.034 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
A、可用酸性高锰酸钾溶液检验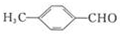 中的醛基 中的醛基 |
| B、可用新制的银氨溶液鉴别乙酸甲酯和乙醛 |
| C、能用一种试剂区分葡萄糖溶液、甘油、醋酸福尔马林等4种溶液 |
| D、1-戊炔和裂化汽油都能是溴水褪色,且褪色原理相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com