
【题目】将0.01mol的铁、铝混合物溶于100mL 0.2mol/LH2SO4溶液中,然后再滴加1mol/L NaOH溶液.若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.当V1=16mL时,则V2为( ) 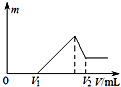
A.24mL
B.30mL
C.440mL
D.44mL
【答案】D
【解析】解:当V1=16mL时,此时,溶液是MgSO4、Al2(SO4)3和Na2SO4混合液, 由Na+离子守恒可知,n(Na2SO4)= ![]() n(Na+)=
n(Na+)= ![]() n(NaOH)=
n(NaOH)= ![]() ×0.016L×1mol/L=0.008mol,
×0.016L×1mol/L=0.008mol,
设MgSO4为xmol、Al2(SO4)3为ymol,则:
根据Mg原子、Al原子守恒有:x+2y=0.01,
100mL 0.2mol/L的H2SO4溶液中含有硫酸的物质的量为:0.2mol/L×0.1L=0.02mol,
根据SO42﹣离子守恒有:x+3y=0.02﹣0.008=0.012,
联立方程解得:x=0.006、y=0.002,
所以金属粉末中:n(Mg)=0.006mol,n(Al)=2y=2×0.02mol=0.004mol,
滴加NaOH溶液到体积V2时时,溶液是Na2SO4和NaAlO2混合液,根据SO42﹣离子、Na+离子和Al原子守恒有:
n(NaOH)=2n(Na2SO4)+n(NaAlO2)=2n(H2SO4)+n(Al)=2×0.02mol+0.004mol=0.044mol,
则V2= ![]() =0.044L=44mL,
=0.044L=44mL,
故选D.
根据图象可知,在滴加NaOH溶液到体积V1=16mL过程中,没有沉淀生成,说明硫酸有剩余,滴加的NaOH用于中和剩余硫酸,V1=16mL时,剩余的H2SO4与滴加的NaOH恰好完全反应,溶液是MgSO4、Al2(SO4)3和Na2SO4混合液,根据Mg原子、Al原子、SO42﹣离子、Na+离子守恒,列方程求算n(Mg)、n(Al);
当滴加NaOH溶液到体积V2时,Al(OH)3完全溶解,沉淀是Mg(OH)2 , 溶液是Na2SO4和NaAlO2混合液.根据SO42﹣离子、Na+离子和Al原子守恒,求出n(NaOH),再利用V= ![]() 计算滴入氢氧化钠溶液体积V2 .
计算滴入氢氧化钠溶液体积V2 .


科目:高中化学 来源: 题型:
【题目】将19.2g Cu溶于100mL浓度均为1molL﹣1的HNO3和H2SO4的混合溶液中,若产生的气体为NO,则产生的NO在标准状况下的体积为( )
A.2.24 L
B.1.68 L
C.3.36 L
D.1.12 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列文字表述与反应方程式对应且正确的是( )
A.乙醇与溴化氢的水溶液共热:CH3CH2OH+HBr→CH3CH2Br+H2O
B.甲烷和氯气在光照条件下的反应:2CH4+Cl2 ![]() 2CH3Cl+H2
2CH3Cl+H2
C.苯酚溶液中滴入NaOH溶液:H++OH﹣→H2O
D.苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O﹣→2C6H5OH+2CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaAlH4(氢化铝钠)和化合物甲都是重要的还原剂.一定条件下,由金属钠和H2反应生成甲,甲与水反应可产生H2 , 甲与AlCl3反应可得到NaAlH4 . 将4.80g甲加热至完全分解,得到金属钠和2.24L(已折算成标准状况)的H2 . 请推测并回答:
(1)NaAlH4中氢元素的化合价、甲的化学式为 .
(2)甲与AlCl3反应得到NaAlH4的化学方程式 .
(3)NaAlH4与盐酸反应的化学方程式为 .
(4)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列说法正确的是( )
A.1 mol NaHCO3与足量盐酸反应放出CO2气体的体积为22.4L
B.1 mol Al3+离子含有的核外电子数为3NA
C.O2和O3的混合气体,质量为48g,所含氧原子数为3NA
D.高温下,0.2mol Fe与足量水蒸气反应,生成的H2的分子数目为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的铝分别与足量的稀盐酸和氢氧化钠溶液反应,当铝完全溶解时,反应中消耗的HCl和NaOH物质的量之比为
A. 1:1B. 2:1C. 1:2D. 3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是某“加碘食盐”包装袋上的部分文字说明.
配料 | 氯化钠(NaCl)、碘酸钾(KIO3) |
含碘量 | 20~40mgkg﹣1 |
保质期 | 18个月 |
食用方法 | 勿长时间炖炒 |
贮藏指南 | 避热、避光、密封、防潮 |
(1)经测定,该“加碘食盐”中KIO3的含量为42.8mgkg﹣1 . 计算每千克“加碘食盐”中KIO3的物质的量为多少?该“加碘食盐”的含碘量为多少?.
(2)将5.0g该“加碘食盐”溶于水中配成100mL溶液,该溶液中IO ![]() 离子物质的量浓度为多少?
离子物质的量浓度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列盛放试剂的方法,错误的是
A. 把硝酸放在棕色试剂瓶中,并放置在阴暗处
B. 把氯水放在棕色试剂瓶中
C. 把氢氧化钠溶液放在带塑料塞的玻璃瓶中
D. 把氢氟酸放在玻璃瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2,5﹣二羟基苯甲酸甲酯俗称龙胆酸甲酯,可由龙胆酸与甲醇酯化得到,是合成制药中的常见中间体.其结构如图 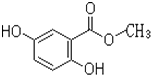 . 回答以下问题:
. 回答以下问题:
(1)龙胆酸甲酯所含官能团名称为
(2)龙胆酸甲酯的分子式为
(3)下列有关龙胆酸甲酯的描述,正确的是(填字母). a.能发生消去反应
b.能与氢气发生加成反应
c.能与浓溴水反应
(4)龙胆酸甲酯与足量氢氧化钠溶液反应的化学方程式 .
(5)写出满足下列条件的龙胆酸的两种同分异构体的结构简式、 . ①能发生银镜反应; ②能使FeCl3溶液显色;
③酯类 ④苯环上的一氯代物只有两种
(6)已知X及其它几种有机物存在如下转化关系,且测得C4H8含有一个支链,A的核磁共振氢谱图中有两个吸收峰. 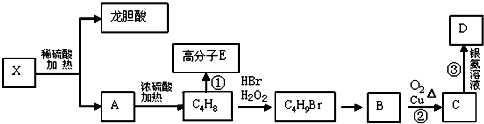
写出①的化学方程式 .
②的化学方程式 .
③的化学方程式 .
写出X的结构简式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com