
【题目】下表是某“加碘食盐”包装袋上的部分文字说明.
配料 | 氯化钠(NaCl)、碘酸钾(KIO3) |
含碘量 | 20~40mgkg﹣1 |
保质期 | 18个月 |
食用方法 | 勿长时间炖炒 |
贮藏指南 | 避热、避光、密封、防潮 |
(1)经测定,该“加碘食盐”中KIO3的含量为42.8mgkg﹣1 . 计算每千克“加碘食盐”中KIO3的物质的量为多少?该“加碘食盐”的含碘量为多少?.
(2)将5.0g该“加碘食盐”溶于水中配成100mL溶液,该溶液中IO ![]() 离子物质的量浓度为多少?
离子物质的量浓度为多少?
【答案】
(1)解: 已知m(KIO3)=42.8mg,则n(KIO3)= ![]() =2×10﹣4mol,m(I)=2×10﹣4mol×127g/mol=0.0254g,即25.4mg,
=2×10﹣4mol,m(I)=2×10﹣4mol×127g/mol=0.0254g,即25.4mg,
该“加碘食盐”的含碘量为25.4mgkg﹣1,
答:每千克“加碘食盐”中KIO3的物质的量为2×10﹣4mol,该“加碘食盐”的含碘量为25.4mgkg﹣1;
(2)解:5g该食盐中n(KIO3)=2×10﹣4mol× ![]() =10﹣6mol,
=10﹣6mol,
n(IO3﹣)= ![]() =1×10﹣5mol/L,
=1×10﹣5mol/L,
答:溶液中IO3﹣离子物质的量浓度为1×10﹣5mol/L.
【解析】解:(1)KIO3的含量为“42.8mgkg﹣1”,则每千克“加碘食盐”中KIO3的质量为42.8mg,其物质的量为 ![]() =2×10﹣4mol,碘元素质量为2×10﹣4mol×127g/mol=0.0254g,即25.4mg,该“加碘食盐”的含碘量为25.4mgkg﹣1 , 答:每千克“加碘食盐”中KIO3的物质的量为2×10﹣4mol,该“加碘食盐”的含碘量为25.4mgkg﹣1;(2)5g该食盐中KIO3的物质的量为2×10﹣4mol×
=2×10﹣4mol,碘元素质量为2×10﹣4mol×127g/mol=0.0254g,即25.4mg,该“加碘食盐”的含碘量为25.4mgkg﹣1 , 答:每千克“加碘食盐”中KIO3的物质的量为2×10﹣4mol,该“加碘食盐”的含碘量为25.4mgkg﹣1;(2)5g该食盐中KIO3的物质的量为2×10﹣4mol× ![]() =10﹣6mol,溶液中IO3﹣离子物质的量浓度为
=10﹣6mol,溶液中IO3﹣离子物质的量浓度为 ![]() =1×10﹣5mol/L。
=1×10﹣5mol/L。


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】氧化还原反应与四种基本反应类型的关系如图所示,则下列反应属于丙区域的是( ) 
A.Cl2+2KBr═Br2+2KCl
B.2NaHCO3 ![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.3Mg+N2 ![]() Mg3N2
Mg3N2
D.2Na2O2+2CO2═2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.01mol的铁、铝混合物溶于100mL 0.2mol/LH2SO4溶液中,然后再滴加1mol/L NaOH溶液.若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.当V1=16mL时,则V2为( ) 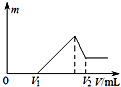
A.24mL
B.30mL
C.440mL
D.44mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于 ![]() 的说法正确的是( )
的说法正确的是( )
A.所有原子可能都在同一平面上
B.最多只可能有9个碳原子在同一平面
C.有7个碳原子可能在同一直线
D.只可能有5个碳原子在同一直线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各种应用中,利用了硅元素的还原性的是( )
A.用硅制造集成电路、晶体管等半导体器件
B.在野外,用硅、石灰、烧碱的混合物制取氢气:Si+Ca (OH)2+2NaOH=Na2SiO3+CaO+2H2↑
C.用HF酸刻蚀玻璃:SiO2+4HF=SiF4↑+2H2O
D.单质硅的制备:SiO2+2C ![]() ?Si+2CO↑
?Si+2CO↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多巴胺是一种重要的中枢神经传导物质.用香兰素与硝基甲烷等为原料合成多巴胺的路线如下. 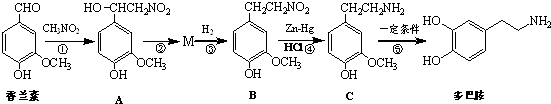
(1)下列说法正确的是 .
A.可用银镜反应鉴别香兰素和多巴胺
B.1mol香兰素与溴水发生取代反应时,最多消耗3mol Br2
C.有机物B分子中不含手性碳原子
D.多巴胺分子中最多有7个碳原子共平面
(2)有机物C中的含氧官能团的名称为 .
(3)反应①、②的反应类型分别为 .
(4)写出同时满足下列条件的A的一种同分异构体的结构简式 .
①具有α﹣氨基酸的共同结构片段;
②能与FeCl3溶液发生显色反应;
③由6种不同化学环境的氢原子.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com