
【题目】(1)写出在空气中加热Ni(OH)2制取NiOOH的化学方程式:__________________________。
(2)H2S燃烧生成的SO2与H2S进一步反应,硫元素转化为S2,写出反应的化学方程式:__________________________。
(3)在酸性条件下,NaHSO3使Cr2O72-还原成为Cr3+,请写出NaHSO3与Cr2O72-反应的离子方程式:__________________。
【答案】4Ni(OH)2+O2![]() 4NiOOH+2H2O 4H2S+2SO2=3S2+4H2O 3HSO3-+Cr2O72-+5H+=3SO42-+2Cr3++4H2O
4NiOOH+2H2O 4H2S+2SO2=3S2+4H2O 3HSO3-+Cr2O72-+5H+=3SO42-+2Cr3++4H2O
【解析】
(1)在空气中加热Ni(OH)2,Ni(OH)2和O2反应产生NiOOH和水;
(2)H2S燃烧时H2S与O2反应生成S2和水;
(3)在酸性条件下,HSO3-与Cr2O72-反应产生Cr3+、SO42-和水。
(1)在空气中加热Ni(OH)2,Ni(OH)2和O2反应产生NiOOH和水,根据电子守恒和原子守恒,可得反应方程式为4Ni(OH)2+O2![]() 4NiOOH+2H2O;
4NiOOH+2H2O;
(2)H2S燃烧生成的SO2与H2S进一步反应,硫元素转化为S2,则反应的化学方程式为:4H2S+2SO2=3S2+4H2O;
(3)在酸性条件下,HSO3-与Cr2O72-发生氧化还原反应产生Cr3+、SO42-和水,反应的离子方程式为:3HSO3-+Cr2O72-+5H+=3SO42-+2Cr3++4H2O。


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法或化学用语表达正确的是![]()
A.s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动
B.p能级的原子轨道呈哑铃形,随着能层的增加,p能级原子轨道也在增多
C.某原子的电子排布式为![]() 属于激发态
属于激发态
D.![]() 的电子排布式为
的电子排布式为![]()
![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(s)。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol/L。下列判断正确的是( )
xC(g)+2D(s)。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol/L。下列判断正确的是( )
A.该条件下此反应的化学平衡常数约为0.91(L/mol)3
B.A的平均反应速率为0.3mol/(L![]() s)
s)
C.B的转化率为60%
D.若混合气体的密度不再改变时,该反应不一定达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W、R五种元素均位于周期表的前四周期,且原子序数依次增大。元素X的基态原子中电子占据了三种能量不同的原子轨道,且成对电子数是未成对电子数的2倍;元素Y与W同主族,且Y是地壳中含量最多的元素;Z基态原子有12种不同运动状态的电子;元素R基态原子最外层只有1个电子且内层电子全充满。
请回答下列问题:(答题时,X、Y、Z、W、R用所对应的元素符号表示)
(1)基态Y原子的轨道式表示式为![]() ___。
___。
(2)元素Y、W均可形成含18个电子的氢化物,其中Y的氢化物沸点较高,原因是___;
(3)元素Z与同周期相邻两元素第一电离能由高到低的顺序为___。
(4)元素R在周期表中位于___区,R分别与Y、W形成离子化合物R2Y和R2W,其中熔点较高的为___。
(5)R2+与过量的氨水形成的配离子的化学式为[R(NH3)4]2+,在配离子中与R2+形成配位键的原子是___。
(6)X的一种单质(相邻原子间通过共价键形成空间网状结构)、XY2、WY2、ZW对应的晶体熔沸点由高到低的顺序为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】试写出下列反应的离子方程式。
(1)氯化亚铁溶液中加入稀硝酸:______________________________________。
(2)氯化亚铁溶液中加入过氧化氢:________________________________。
(3)用酸性KMnO4标准溶液滴定莫尔盐[FeSO4(NH4)2SO4·xH2O]溶液:___________________________。
(4)硫酸亚铁溶液中加入次氯酸钠溶液:_____________________________。
(5)用酸性重铬酸钾(K2Cr2O7)溶液滴定硫酸亚铁溶液:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,有c(CH3COOH)+c(CH3COO)=0.1 mol·L1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO)与pH的关系如图所示。下列有关溶液中离子浓度关系的叙述不正确的是
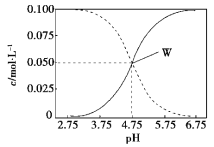
A. pH=5.5的溶液中:c(CH3COO—)>c(CH3COOH)>c(H+)>c(OH)
B. pH=3.5的溶液中:c(Na+)+c(H+)c(OH)+c(CH3COOH)=0.1 mol·L1
C. W点所表示的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH)
D. 向W点所表示的1.0 L溶液中通入0.05 mol HCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)加热搅拌条件下加入NaClO3,将Fe2+氧化成Fe3+,其离子方程式是_______。
(2)CoCO3隔绝空气灼烧可以生成Co2O3,该反应的化学方程式为____________。
(3)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等,除去100 L锅炉水中![]() 含氧气8 g/L的溶解氧,需要肼的质量为__________。
含氧气8 g/L的溶解氧,需要肼的质量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境监测测定水中溶解氧的方法是:①量取25.00mL水样,迅速加入固定剂MnSO4溶液和碱性KI溶液(含KOH),立即塞好瓶塞,反复振荡,使之充分反应,其反应式为:2Mn2++O2+4OH-=2MnO(OH)2(该反应极快)②测定:开塞后迅速加入1mL~2mL浓硫酸(提供H+),使之生成I2,再用0.1000mol/L的Na2S2O3溶液滴定(以淀粉为指示剂),消耗VmL。有关反应式为:MnO(OH)2+2I-+4H+=Mn2++I2+3H2O、I2+2S2O32-=2I-+S4O62-
滴定次数 | 待测液的体积/mL | 0.1000mol·L-1 Na2S2O3的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
试回答:
(1)消耗Na2S2O3的体积平均值为___mL,水中溶解氧的量是(以g/L为单位,保留3位有效数字)___。
(2)滴定(I2和S2O32-反应)以淀粉溶液为指示剂,终点时现象为___。
(3)判断下列操作引起的误差(填“偏大”、“偏小” “无影响”或“无法判断”)
①读数:滴定前平视,滴定后俯视___。
②未用标准液润洗滴定管___。
③配制Na2S2O3溶液时,其固体中含有对反应体系无影响的杂质___。
④待测液的滴定管之前有气泡,取液后无气泡___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在通风橱中进行下列实验:
步骤 |
|
| |
现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
下列说法不正确的是
A. I中气体由无色变红棕色的化学方程式:2NO+O2=2NO2
B. II中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C. 对比I、II中现象,说明稀HNO3的氧化性强于浓HNO3
D. 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com