
【题目】化学与人类生产、生活密切相关,下列叙述正确的是![]()
A.氢氧化铝、碳酸钠都是常见的胃酸中和剂
B.红葡萄酒密封储存时间越长质量越好原因之一是生成了有香味的酯
C.碘酒中的碘因有还原性而起到杀菌消毒作用
D.食盐、食醋、味精是常用的食品添加剂,其主要成分均属于钠盐
科目:高中化学 来源: 题型:
【题目】(1)化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量,已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能:P-P:198kJ·mol-1,P-O:360 kJ·mol-1,O=O:498kJ·mol-1,则反应P4(白磷)与O2反应生成P4O6的热化学反应方程式为____。

(2)肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)═N2O4(l) △H1═-19.5kJ/mol
②N2H4(l)+O2(g)═N2(g)+2H2O(g) △H2═-534.2kJ/mol
写出肼和N2O4反应的热化学方程式_____。
(3)化学反应N2+3H2![]() 2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____。
2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.在固定体积的密闭容器中发生可逆反应![]() ,当混合气体的压强不再改变时,说明已达到化学平衡状态
,当混合气体的压强不再改变时,说明已达到化学平衡状态
B.对于反应![]()
![]() ,改变某一条件,若化学平衡常数增大,则反应速率也一定增大
,改变某一条件,若化学平衡常数增大,则反应速率也一定增大
C.将![]() 的
的![]() 加水稀释,则溶液中
加水稀释,则溶液中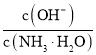 减小
减小
D.常温下向![]() 悬浊液中加入
悬浊液中加入![]() 浓溶液后,溶液中
浓溶液后,溶液中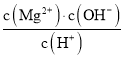 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率且不影响生成氢气的总量,可向盐酸中加适量的( )
①NaOH(s) ②NH4Cl(s) ③H2O ④CH3COONa(s)
A.①③B.②④C.③④D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq) +Cu(s) = Cu2+(aq) +2Ag(s)
设计的原电池如图所示。请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是___________;
(2)电极反应为: 正极: ___________负极: ___________
(3)外电路中的电子是从_______电极流向________电极。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解1升0.2mol/L的CuSO4溶液,持续通电至两极产生气体体积相等时(同条件下测定),停止电解。
(1)全过程中两极共得到的气体在标况下所占的体积___________
(2)全过程中电子转移____________摩尔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个恒压的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g)![]() A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。下列说法中正确的是
A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。下列说法中正确的是
A.平均反应速度:甲<乙B.平衡时C的物质的量:甲>乙
C.平衡时C的转化率:甲>乙D.平衡时混合气体密度:甲<乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com