
在20℃,5.05×105Pa条件下,密闭容器中进行反应2A(g)+xB(g) 4C(g),达平衡时c(A)=1.00mol?L-1,现将压强减小到1.01×105Pa,建立平衡后,c(A)=0.18mol?L-1,则下列说法正确的是 ( )
4C(g),达平衡时c(A)=1.00mol?L-1,现将压强减小到1.01×105Pa,建立平衡后,c(A)=0.18mol?L-1,则下列说法正确的是 ( )
A.系数x >2
B.若增大该体系的压强,平衡向左移动,化学平衡常数变小
C.若增大该体系的压强,平衡向右移动,化学平衡常数不变
D.该反应的化学平衡常数表达式是K=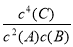
D
【解析】
试题分析:A.在5.05×105Pa条件下达平衡时c(A)=1.00mol?L-1,现将压强减小到1.01×105Pa,压强为原来是五分之一,若平衡不发生移动,则建立平衡后,A的浓度也应该为原来的五分之一,即c(A)=0.200mol/L.但是却是c(A)=0.18mol?L-1。说明减小压强,平衡正向移动。根据平衡移动原理,减小压强,平衡向气体体积增大的方向移动。所以2+x<4.所以x=1.错误。B.若增大该体系的压强,平衡向气体体积减小的方向,即向左移动。但是化学平衡常数只与温度有关。温度不变,化学平衡常数也不变。错误。C.若增大该体系的压强,平衡向气体体积减小的方向,即向左移动,由于温度不变,所以化学平衡常数不变。错误。D.化学平衡常数是可逆反应达到平衡状态时各生成物 幂指数的乘积与各反应物浓度幂指数乘积的比,对该反应来说,其化学平衡常数表达式是K=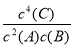 。正确。
。正确。
考点:考查化学平衡常数的表达式、压强对化学平衡移动、化学平衡常数的影响的知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015届安徽省六校教育研究会高三第一次联考化学试卷(解析版) 题型:实验题
聚合硫酸铁又称聚铁,化学式为[Fe2(OH)n(SO4)3-0.5n]m,广泛用于污水处理。实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O),过程如下:
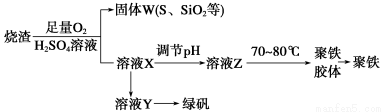
(1)验证固体W焙烧后产生的气体含有SO2的方法是________________。
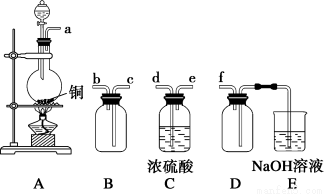
(2)实验室制备、收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各仪器接口,顺序为a→________→________→________→________→f。
装置A中发生反应的化学方程式为___________________。
(3)制备绿矾时,向溶液X中加入过量________,充分反应后,经过滤操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾。过滤所需的玻璃仪器有________________。
(4)欲测定溶液Y中Fe2+的浓度,需要用容量瓶配制KMnO4标准溶液,用KMnO4标准溶液滴定时应选用________滴定管(填“酸式”或“碱式”)。
(5)溶液Z的pH影响聚铁中铁的质量分数。若溶液Z的pH偏小,将导致聚铁中铁的质量分数________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源:2015届安徽望江中学同步课时练(人教选修4)2.3化学平衡移动试卷(解析版) 题型:选择题
如图是关于反应A2(g)+3B2(g)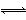 2C(g)(正反应为放热反应)的平衡移动图像,影响平衡移动的原因可能是( )
2C(g)(正反应为放热反应)的平衡移动图像,影响平衡移动的原因可能是( )
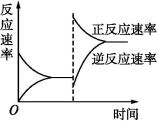
A.升高温度,同时加压
B.降低温度,同时减压
C.增大反应物浓度,同时减小生成物浓度
D.增大反应物浓度,同时使用催化剂
查看答案和解析>>
科目:高中化学 来源:2015届安徽望江中学同步课时练(人教选修4)1.3化学反应热的计算(解析版) 题型:填空题
为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应的措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得,5 g甲醇(CH3OH,液态)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5 kJ的热量,试写出甲醇燃烧的热化学方程式: 。
(2)已知化学键的键能为:
化学键 | H—H | N—H |
|
键能/( kJ·mol-1) | 436 | 391 | 945 |
又知反应N2(g)+3H2(g) 2NH3(g) ΔH=a kJ·mol-1。试根据表中所列键能数据估算a的值为 。
2NH3(g) ΔH=a kJ·mol-1。试根据表中所列键能数据估算a的值为 。
(3)已知:C(石墨,s)+O2(g) CO2(g) ΔH=-393 kJ·mol-1
CO2(g) ΔH=-393 kJ·mol-1
2H2(g)+O2(g) 2H2O(l) ΔH=-571.6 kJ·mol-1
2H2O(l) ΔH=-571.6 kJ·mol-1
2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l) ΔH=-2 599 kJ·mol-1
4CO2(g)+2H2O(l) ΔH=-2 599 kJ·mol-1
根据盖斯定律,计算298 K时C(石墨,s)和H2(g)反应生成1 mol C2H2(g)的焓变为 。
查看答案和解析>>
科目:高中化学 来源:2015届安徽师大附中高二下学期期中考查化学试卷(解析版) 题型:填空题
金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:WO3 (s) + 3H2 (g)  W (s) + 3H2O (g)请回答下列问题:
W (s) + 3H2O (g)请回答下列问题:
(1)上述反应的化学平衡常数表达式为 。
(2)某温度下反应达平衡时,H2与水蒸气的体积比为3:5,则H2的平衡转化率 。
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
温度 | 25℃ ~ 550℃ ~ 600℃ ~ 700℃ |
主要成份 | WO3 W2O5 WO2 W |
500℃时,固体物质的主要成分为 ;
第二阶段反应的化学方程式为 ;
假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为 。
钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2 (g) 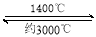 WI4 (g)。下列说法正确的有 。
WI4 (g)。下列说法正确的有 。
A.灯管内的I2可循环使用
B.WI4在灯管壁上分解,使灯管的寿命延长
C.WI4在灯丝上分解,产生的W又沉积在灯丝上
D.接通电源后,WI4的分解速率加快,W和I2的化合速率减慢
查看答案和解析>>
科目:高中化学 来源:2015届安徽师大附中高二下学期期中考查化学试卷(解析版) 题型:选择题
下列事实能用勒沙特列原理解释的是( )
①由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
②实验室中用氯化钠固体与浓硫酸共热制取氯化氢气体
③用排饱和食盐水法收集Cl2
④温度控制在500℃有利于合成氨反应
⑤工业制
取金属钾Na(l)+ KCl(l)  NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来
NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来
A.②③⑤ B.①③⑤ C.①②③④⑤ D.①②③⑤
查看答案和解析>>
科目:高中化学 来源:2015届安徽师大附中高二下学期期中考查化学试卷(解析版) 题型:选择题
已知常温下,N2(气)和H2(气)生成2mol NH3(气)放出92.4 kJ热量。现有甲、乙两个容积相同且恒容的密闭容器,在常温下:①向密闭容器甲中通入1 molN2和3 mol H2,达到平衡时放出热量Q1kJ。②向密闭容器乙中通入0.5 mol N2和1.5 mol H2,达到平衡时放出热量Q2kJ。则下列关系式正确的是( )
A.Q1=2Q2=92.4 B.92.4 >Ql>2Q2 C.92.4=Q1>2Q2 D.92.4 >Q1=2Q2
查看答案和解析>>
科目:高中化学 来源:2015届宁夏高三上学期第一次月考理综试卷(解析版) 题型:选择题
为实现下列实验目的,依据下表提供的主要仪器,所用试剂合理的是
选项 | 实验目的 | 主要仪器 | 试剂 |
A | 分离Br2和CCl4的混合物 | 分液漏斗、烧杯 | Br2和CCl4的混合物、蒸馏水 |
B | 实验室制取H2 | 试管、带导管的橡皮塞 | 锌粒、稀HNO3 |
C | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 | 葡萄糖溶液、蔗糖溶液、 银氨溶液 |
D | 测定NaOH溶液的浓度 | 滴定管、锥形瓶、烧杯 | NaOH溶液、 0.100 0 mol·L-1盐酸 |
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都市2012级临诊考试化学试卷(解析版) 题型:填空题
(8分)甲醇(CH3OH)被称为21世纪的新型燃料,以煤为原料制备甲醇的流程如下:
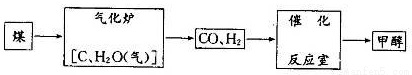
(1) 气化炉中主要反应的化学方程式为 。
(2)已知CO、H2、甲醇(l)的燃烧热分别为:—285.8 kJ/mol、—283 kJ/mol、—726.5 kJ/mol;
则CO和H2 合成甲醇的热化学方程式为__ __
(3) -定条件下,在催化反应室中发生反应.CO(g)+2H2(g) =CH3OH(g)△H<0;
CO 的平衡转化率与温度、压强的关系如图所示。回答下列问题:
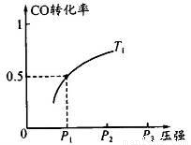
①工业上,上述反应温度不宜过高,原因是_ ___;
②若反应是1 mol CO与2 mol H2在2L容积中进行,则
T1、P1下,该反应的平衡常数为__ __;
维持温度、容积不变,催化反应室再增加l mol CO与2 mol
H2,达到新平衡时,CO的转化率____(填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com