
����Ŀ����ԭ�������ĵ��������ֶ�����Ԫ�أ�����ĸ��ʾ��ԭ�Ӱ뾶����Դ�С��������ۻ�����۵ı仯��ͼ1��ʾ�� 
�����жϳ���Ԫ�ػش����⣺
��1��f��Ԫ�����ڱ���λ���� ��
��2��d��e���γ�ԭ�Ӹ�����Ϊ1��1�Ļ�����û�����ĵ���ʽΪ �� 0.10mol�û�����������ˮ��Ӧʱת�Ƶĵ�����Ϊ
��3������Ԫ�ؿ������R��zx4f��gd4��2 �� ��ʢ��10mL1mol/L R��Һ���ձ��еμ�1mol/LNaOH��Һ���������ʵ�����NaOH��Һ����仯ʾ��ͼ��ͼ2��
����m�η�����Ӧ�����ӷ���ʽΪ ��
������10mLlmol/L R��Һ�иļ�20mLl.2mol/L Ba��OH��2��Һ����ַ�Ӧ����Һ�в����ij��������ʵ���Ϊ ��
���𰸡�
��1���������ڢ�A��
��2��![]() ��6.02��1022
��6.02��1022
��3��NH4++OH��=NH3?H2O��0.022mol
���������⣺��ͼ�еĻ��ϼۡ�ԭ�Ӱ뾶�Ĵ�С��ԭ����������֪x��HԪ�أ�y��CԪ�أ�z��NԪ�أ�d��OԪ�أ�e��NaԪ�أ�f��AlԪ�أ�g��SԪ�أ�h��ClԪ�أ���1��f��AlԪ�أ���Ԫ�����ڱ���λ���ǵ������ڢ�A�壬���Դ��ǣ��������ڢ�A�壻��2���ɱ�������Ԫ�ص�ԭ�Ӱ�1��1��ɵĻ�����Ⱥ����Ӽ��ֺ��Ǽ��Թ��ۼ�����ΪNa2O2 �� �����ʽΪ ![]() ������������OԪ�ػ��ϼ�Ϊ��1�ۣ���Ӧ�зֱ��Ϊ��2�ۡ�0�ۣ���������������ԭ��Ӧ��0.10mol�û�����������ˮ��Ӧʱת�Ƶĵ�����Ϊ6.02��1022 �� ���Դ��ǣ�
������������OԪ�ػ��ϼ�Ϊ��1�ۣ���Ӧ�зֱ��Ϊ��2�ۡ�0�ۣ���������������ԭ��Ӧ��0.10mol�û�����������ˮ��Ӧʱת�Ƶĵ�����Ϊ6.02��1022 �� ���Դ��ǣ� ![]() ��6.02��1022����3����R��NH4Al��SO4��2 �� m������м����������ƣ��������ʵ������䣬��NH4+��OH����Ӧ����NH3H2O�����ӷ���ʽΪNH4++OH��=NH3H2O��
��6.02��1022����3����R��NH4Al��SO4��2 �� m������м����������ƣ��������ʵ������䣬��NH4+��OH����Ӧ����NH3H2O�����ӷ���ʽΪNH4++OH��=NH3H2O��
���Դ��ǣ�NH4++OH��=NH3H2O����10mL 1molL��1 NH4Al��SO4��2��Һ��Al3+ ���ʵ���Ϊ0.01mol��NH4+�����ʵ���Ϊ0.01mol��SO42�������ʵ���Ϊ0.02mol��20mL 1.2 molL��1Ba��OH��2��Һ��Ba2+���ʵ���Ϊ0.024mol��OH��Ϊ0.048mol��
��SO42��+Ba2+=BaSO4������֪SO42�����㣬�ʿ��Եõ�0.02mol BaSO4 ��
Al3 | + | 3OH�� | = | Al��OH��3�� |
0.01mol | 0.03mol | 0.01mol |
��Ӧʣ��OH��Ϊ0.048mol��0.03mol=0.018mol��
NH4+ | + | OH�� | = | NH3H2O |
0.01mol | 0.01mol |
��Ӧʣ��OH��Ϊ0.018mol��0.01mol=0.008mol��
Al��OH��3 | + | OH�� | = | AlO2�� | + | 2H2O |
0.008mol | 0.008mol |
�ʵõ�Al��OH��3����Ϊ0.01mol��0.008mol=0.002mol
�����յõ�����Ϊ0.02mol+0.002mol=0.022mol��
���Դ��ǣ�0.022mol��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�ת���ڸ�����������ʵ�ֵ����� ��
A. NaCl(aq)![]() NaHCO3(s)
NaHCO3(s)![]() Na2CO3(s)
Na2CO3(s)
B. CuCl2![]() Cu(OH)2
Cu(OH)2![]() Cu
Cu
C. Al![]() NaAlO2(aq)
NaAlO2(aq) ![]() NaAlO2(s)
NaAlO2(s)
D. MgO(s)![]() Mg(NO3)2(aq)
Mg(NO3)2(aq)![]() Mg(s)
Mg(s)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʫ�����ס��а��ġ�����ʮ�š��������������ƣ�����С��¯����������ѩ������һ����?�����к��л�ѧ���̵�����һ��?( )
A. ��һ�� B. �ڶ��� C. ������ D. ���ľ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȡ��ˮ�е�I2 ��������Ϊ��ȡ�������� ��
A. �ƾ� B. �� C. CCl4 D. ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ��һ���ܴ���������ǣ� ��
A. pH=1����Һ�У� Fe2+��NO3-��SO42-��Na+
B. ��ˮ�����c(H+)=1��10-14 mol��L-1����Һ�У�Ca2+��K+��Cl-��HCO3-
C.  ��1012����Һ�У�NH4+��Al3+��NO3-��Cl-
��1012����Һ�У�NH4+��Al3+��NO3-��Cl-
D. c(Fe2+) =0.1 mol��L-1����Һ�У�K+��ClO-��SO42-��SCN-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������У���һ����A��B�����Ϻ�����Ӧ��xA(g)+yB(g)![]() zC(g)+mD(s)��ƽ��ʱ��A��Ũ��Ϊ0.5mol/L�������¶Ȳ��䣬���������ݻ�����ԭ�����������ٴ�ƽ��ʱ�����A��Ũ��Ϊ0.3mol/L���������й��ж���ȷ���ǣ� ��
zC(g)+mD(s)��ƽ��ʱ��A��Ũ��Ϊ0.5mol/L�������¶Ȳ��䣬���������ݻ�����ԭ�����������ٴ�ƽ��ʱ�����A��Ũ��Ϊ0.3mol/L���������й��ж���ȷ���ǣ� ��
A. x+y>z+m B. B��ת����һ����С C. ƽ��������Ӧ�����ƶ� D. ���������ܶ�һ����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����д�ʩ����ʵ��������������ԭ�����͵��ǣ�������
A. ���Ƶ���ˮ�ڹ�������ɫ��dz B. H2��I2��HIƽ��������ѹ����ɫ����
C. �ںϳɰ��ķ�Ӧ�У����»��ѹ�����ڰ��ĺϳ� D. ����ɫNO2��ѹ����ɫ�ȱ�����dz
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ԴԶ����������˵���ӻ�ѧ�ӽ�����������
A. �����ճ����������Խ�Ů������������ʫ�а����˶��������
B. ����֮�������� ˵�����������ζ
C. ����ʯ�ң��������Ϊ������ ��μ������漰�ֽⷴӦ
D. ���ٱ����Ӻ����������������������Ʋ�����ij�ɷֿ�����������ά
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�������5minʱ��ͭ�缫��������21.6g��
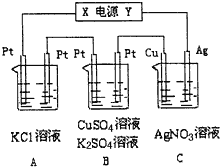
��1����Դ�缫Y����Ϊ__________���������������������� ����
��2����������Һ��pH�仯��A_________��B________������������������С����������������
��3��A�з�����Ӧ�����ӷ���ʽΪ��_________________����A��KCl��Һ�����Ҳ��200mL��������ҺOH-��Ũ�ȵ���_______��
��4��B�������ĵ缫��ӦʽΪ____________________����ͨ��5minʱB�й��ռ�2.24L���壨���������Һ���Ϊ200mL����ͨ��ǰ����ͭ��Һ�����ʵ���Ũ��ԼΪ______��
��5������Cװ�õ���ȡ������������ͭ��������д�������ĵ缫��Ӧʽ____________
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com