
 ����һ����Ҫ�Ļ���ԭ�ϣ�Ҳ����Ҫ�Ĺ�ҵ��Ʒ���ڹ�ũҵ������������������Ҫ���ã�
����һ����Ҫ�Ļ���ԭ�ϣ�Ҳ����Ҫ�Ĺ�ҵ��Ʒ���ڹ�ũҵ������������������Ҫ���ã����� ��1������ˮ���ƣ�Ҳ�ܷ������룺NH3+NH3=NH4++NH2-����2.3g������Ͷ��1.0LҺ���л���NH2-���ٽ�Һ���ĵ��룬����Һ����Ӧ����NaNH2����ϻ�ѧ����ʽ���㣻
��2����Pt�缫��Һ�����е��ɲ���H2��N2�������ϰ�����笠����ӵõ�������������
��3����������ԭNO����û����Ⱦ������Ϊ������ˮ��
��4�����N2Ϊ0.10mol��H2Ϊ0.30mol��NH3Ϊ0.10mol�����ݷ���ʽ֪���μӷ�Ӧ���������ʵ���=0.15mol����H2��ƽ��ת����=$\frac{�μӷ�Ӧ���������ʵ���}{������ʼ���ʵ���}$��100%��ƽ����c��N2��=0.10mol/L��c��H2��=0.30mol/L��c��NH3��=0.10mol/L���ڸ��¶��µ�ƽ�ⳣ��K=$\frac{{c}^{2}��N{H}_{3}��}{c��{N}_{2}����{c}^{3}��{H}_{2}��}$��
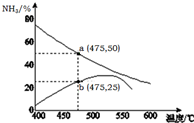
��5������ͼ֪��a��ƽ�����ߡ�b�Ǿ���һ��ʱ�䷴Ӧ������ߣ����¶���Ҫʹ�÷�Ӧ�ﵽƽ��״̬��Ӧ��������������ƽ�������ƶ���
��� �⣺��1����2.3g������Ͷ��1.0LҺ���з�����ӦΪ��2Na+2NH3=2NaNH2+H2�����ٽ�Һ���ĵ��룬���ݣ�NH3+NH3=NH4++NH2-��[NH4+][NH2-]=l.0��l0-30����Ӧ����NH2-���ʵ���Ϊ0.1mol��Ũ��Ϊ0.1mol/L��������Һ��NH4+��Ũ��l.0��l0-29mol/L��
�ʴ�Ϊ��1.0��l0-29mol/L��
��2����Pt�缫��Һ�����е��ɲ���H2��N2�������ϰ�����笠����ӵõ��������������缫��ӦʽΪ2NH3+2e-=H2+2NH2- �� 2NH4++2e-=H2+2NH3��
�ʴ�Ϊ��2NH3+2e-=H2+2NH2- �� 2NH4++2e-=H2+2NH3��
��3����������ԭNO����û����Ⱦ������Ϊ������ˮ����Ӧ����ʽΪ4NH3+6NO$\frac{\underline{\;����\;}}{\;}$5N2+6H2O��
�ʴ�Ϊ��4NH3+6NO$\frac{\underline{\;����\;}}{\;}$5N2+6H2O��
��4�����N2Ϊ0.10mol��H2Ϊ0.30mol��NH3Ϊ0.10mol�����ݷ���ʽ֪���μӷ�Ӧ���������ʵ���=0.15mol����H2��ƽ��ת����=$\frac{�μӷ�Ӧ���������ʵ���}{������ʼ���ʵ���}$��100%=$\frac{0.15mol}{0.3mol+0.15mol}$��100%=33.3%��ƽ����c��N2��=0.10mol/L��c��H2��=0.30mol/L��c��NH3��=0.10mol/L���ڸ��¶��µ�ƽ�ⳣ��K=$\frac{{c}^{2}��N{H}_{3}��}{c��{N}_{2}����{c}^{3}��{H}_{2}��}$=$\frac{0.1{0}^{2}}{0.10��0.3{0}^{3}}$=3.70��
�ʴ�Ϊ��33.3%��3.70��
��5������ͼ֪��a��ƽ�����ߡ�b�Ǿ���һ��ʱ�䷴Ӧ������ߣ����¶���Ҫʹ�÷�Ӧ�ﵽƽ��״̬��Ӧ��������������ƽ�������ƶ���������Ӧ���ʴ����淴Ӧ���ʣ��ʴ�Ϊ������
���� ���⿼�黯ѧƽ���йؼ��㼰���ԭ����Ϊ��Ƶ���㣬���ؿ���ѧ������������������ȷ��ѧƽ����㷽�������ԭ���ǽⱾ��ؼ����ѵ��ǣ�5���⣬���������Ũ����Դ�Сȷ����Ӧ������Ŀ�Ѷ��еȣ�


 ��������ϵ�д�
��������ϵ�д� ���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
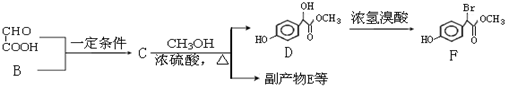
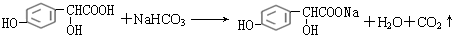 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ���ں����ø�ѹ������ػ����Ϸ�չ������һ�ֽ����⻯������أ�MH-Ni��أ��������й�˵������ȷ���ǣ�������
��ͼ���ں����ø�ѹ������ػ����Ϸ�չ������һ�ֽ����⻯������أ�MH-Ni��أ��������й�˵������ȷ���ǣ�������| A�� | �ŵ�ʱ������ӦΪ��NiOOH+H2O+e-=Ni��OH��2+OH- | |
| B�� | ��صĵ��Һ��ΪKOH��Һ | |
| C�� | ���ʱ������ӦΪ��MH+OH-=M+H2O+e- | |
| D�� | MH��һ�ഢ����ϣ������ܶ�Խ��ص������ܶ�Խ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
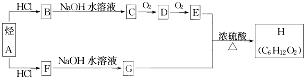
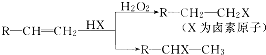
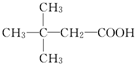 �����ýṹ��ʽ��ʾ��
�����ýṹ��ʽ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ˮ�У�Cl2+H2O=2H++Cl-+ClO- | |
| B�� | ����������Һ������������Һ��������Һ�����ԣ�2HSO4-+Ba2++2OH-=BaSO4��+2H2O+SO42- | |
| C�� | ��˫��ˮ�м���ϡ�����KI��Һ��H2O2+2H++2I-=I2+2H2O | |
| D�� | ��ͭ���������CuSO4��Һ��2Cu2++2H2O$\frac{\underline{\;���\;}}{\;}$2Cu+O2��+4H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ӻ�ˮ����ȡþ | B�� | �þƾ������Ǽ��Ƽ� | ||
| C�� | ������ͨ�������ʯ������Ư�� | D�� | ʯ�ͷ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
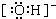
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
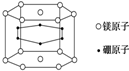
| A�� | 22% | B�� | 70% | C�� | 66.7% | D�� | 33.3% |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com