
【题目】亚硝酸钠是一种食品添加剂,具有防腐和抗氧化作用。某同学对亚硝酸钠进行了相关探究。
(一)查阅资料
①亚硝酸钠(NaNO2)为无色、无味的结晶。
②HNO2是一种弱酸,酸性比醋酸略强,性质不稳定,易分解生成NO和NO2;能被常见的强氧化剂氧化;但在酸性溶液中它也是一种氧化剂,如能把I-氧化成I2。
③AgNO2是一种微溶于水、易溶于酸的浅黄色固体。
(二)问题讨论
(1)人体正常的血红蛋白中应含Fe2+,误食亚硝酸盐(如NaNO2)会致使机体组织缺氧,出现青紫而中毒,原因是________。若发生中毒时,你认为下列物质有助于解毒的是________。
A.鸡蛋清 B.胃舒平 [主要成分是Al(OH)3] C.小苏打 D.维生素C
(2)由于亚硝酸钠和食盐性状相似,曾多次发生过将NaNO2误当食盐食用的事件。要区别NaNO2和NaCl两种固体,你需用的试剂是__________。
(三)实验测定
为了测定某样品中NaNO2的含量,某同学进行如下实验:①称取样品a g,加水溶解,配制成100 mL溶液。②取25.00 mL溶液于锥形瓶中,用0.02 mol/L KMnO4标准溶液(酸性)进行滴定,滴定结束后消耗KMnO4溶液 V mL。
(3)上述实验①所需玻璃仪器除玻璃棒、胶头滴管之外还有__________。
(4)在进行滴定操作时,KMnO4溶液盛装在_________滴定管中(填“酸式”、“碱式”)。当滴入最后一滴溶液,________时达到滴定终点。
(5)滴定过程中发生反应的离子方程式是________;测得该样品中NaNO2的质量分数为_______。
(6)若滴定管未用KMnO4标准溶液润洗就直接注入,则测定结果_________;若滴定过程中刚出现颜色变化就停止滴定,则测定结果___________ (填“偏大”、“偏小”、“无影响”)。
【答案】 血红蛋白中Fe2+被NO2-氧化为Fe3+,导致血红蛋白失去运氧功能 D HNO3酸化的AgNO3溶液(或酚酞溶液或KI淀粉试液和稀硫酸。其他合理试剂均可) 烧杯、100mL容量瓶 酸式 锥形瓶中无色溶液变成粉红色,且30s内不褪色 5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O ![]() % )偏大 偏小
% )偏大 偏小
【解析】(二)(1)由资料可知,亚硝酸根可表现出氧化性,所以误食亚硝酸盐(如NaNO2)会致使机体组织缺氧,出现青紫而中毒,原因是血红蛋白中Fe2+被NO2-氧化为Fe3+,导致血红蛋白失去运氧功能。若发生中毒时,服用还原性强的物质如维生素C有助于解毒。
(2)由于亚硝酸钠和食盐性状相似,曾多次发生过将NaNO2误当食盐食用的事件。要区别NaNO2和NaCl两种固体,可利用氯离子的检验方法,或根据资料,利用亚硝酸盐的氧化性或亚硝酸的弱酸性设计出不同的方案,需用的试剂是HNO3酸化的AgNO3溶液(检验氯离子)或酚酞溶液(亚硝酸根水解显碱性)或KI淀粉试液和稀硫酸(把I-氧化成I2,碘遇淀粉变蓝)。 (三) (3)上述实验①所需玻璃仪器除玻璃棒、胶头滴管之外还有烧杯、100mL容量瓶。
(4)在进行滴定操作时,酸性和强氧化性的溶液要装在酸式滴定管中。KMnO4溶液有强氧化性,所以盛装在酸式滴定管中。高锰酸钾溶液稀溶液显红色,它被还原的产物几乎是无色的,所以可以用过量的一滴高锰酸钾溶液作为滴定终点的指示剂,即当滴入最后一滴溶液,锥形瓶中无色溶液变成粉红色,且30s内不褪色时达到滴定终点。
(5) 为了测定某样品中NaNO2的含量,某同学进行如下实验:①称取样品a g,加水溶解,配制成100 mL溶液。②取于锥形瓶中,用KMnO4标准溶液(酸性)进行滴定,滴定结束后消耗KMnO4溶液 V mL。
滴定过程中发生反应的离子方程式是5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O,因此,25.00 mL样品溶液中,n(NO2-)=![]() V
V![]() L=5
L=5![]() V mol,由此求得a g样品中,m(NaNO2)= 5
V mol,由此求得a g样品中,m(NaNO2)= 5![]() V mol
V mol![]() 69g/mol=1.38
69g/mol=1.38![]() V g,测得该样品中NaNO2的质量分数为
V g,测得该样品中NaNO2的质量分数为![]() %。
%。
(6)若滴定管未用KMnO4标准溶液润洗就直接注入,则管内残存的蒸馏水会把标准液稀释,导致标准液用量偏大,所以测定结果偏大;若滴定过程中刚出现颜色变化就停止滴定,此时还没有真正到达滴定终点,在临近滴定终点时,由于反应物浓度较小,所以反应速率较慢,则变红就停止滴定所用的标准液偏小,测定结果偏小。


科目:高中化学 来源: 题型:
【题目】根据下列反应流程填空:
已知:A是烯烃中分子量最小的,可做果实的催熟剂; C中每个碳上各有一个羟基;

(1)A的名称是_________ B的名称是_________条件Ⅰ是________________;条件Ⅱ是______________________
(2)填反应类型:B→C___________;D→A __________________A →E______________
(3)写方程式: B→C___________ D→A____________________ A → E______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将燃着的硫化氢气体通入盛有一定量O2的集气瓶内,下列3个反应发生的先后顺序是( )
①2H2S+O2→2S+2H2O ②2H2S+SO2→3S+2H2O ③2H2S+3O2→2SO2+2H2O.
A. ③②① B. ③①② C. ①③② D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.实验室里要配制500 mL 0.2 mol/L的硫酸钠溶液。
(1)请填写下列空白:
A.计算、称量、溶解:在天平上称出________g硫酸钠固体,把它放在烧杯里,用适量的蒸馏水溶解。
B.转移:把得到的溶液冷却后小心地沿着________注入________中。
C.洗涤:用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤液也小心转入容量瓶中。
D.定容:继续向容量瓶中加蒸馏水至液面距刻度线1~2 cm ,改用_______小心滴加蒸馏水至溶液凹液面底部与刻度线相切。
E.摇匀:将瓶塞塞紧,充分摇匀。
F.贴标签、装试剂瓶:将配好的溶液倒入试剂瓶中,贴上标签,并洗涤容量瓶。
(2)下列情况会使所配溶液浓度偏高的是________(填字母)。
a.某同学定容时俯时容量瓶刻度线
b.没有进行上述的操作步骤C
c.摇匀后发现液面低于刻度线又加水了
d.进行B操作时将少量液体洒到外
II. 用质量分数为98%的浓硫酸配制100ml3.0mol/L稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积②量取一定体积的浓硫酸③溶解④转移、洗涤⑤定容⑥摇匀 回答下列问题
(1)若所用浓硫酸密度为1.84g/cm3,则该浓硫酸的物质的量浓度为_____,配制上述稀硫酸所需浓硫酸的体积是_____(小数点后保留一位)。
(2)为了保证实验的准确性,在第③和第④步操作之间还应该加多一步什么操作_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理来解释的是
A. 将混合气中的氨气液化分离,有利于合成氨的反应
B. 用过量氮气与氢气反应可以提高氢气的转化率
C. 密闭容器中发生反应H2(g)+I2(g)![]() 2HI(g),增大压强时容器中颜色加深
2HI(g),增大压强时容器中颜色加深
D. 加压有利于SO2与O2反应生成SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制l. 0 mol L-1的NaOH溶液240 mL;
(1)配制溶液时,一般可以分为以下几个步骤:
①称量②计算③溶解④倒转摇匀⑤转移⑥洗涤⑦定容⑧冷却
其正确的操作顺序为______________(填写序号)。本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、还有_______________________。
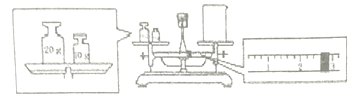
(2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。
烧杯的实际质量为___________g,要完成本实验该同学应称出______________g NaOH。
(3)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是____________。
①没有洗涤烧杯和玻璃棒 ②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水 ④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017海南]已知反应CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是
CO2(g)+H2(g) ΔH<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是
A.升高温度,K减小 B.减小压强,n(CO2)增加
C.更换高效催化剂,α(CO)增大 D.充入一定量的氮气,n(H2)不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com