
����Ŀ��һ���¶��£����ݻ�Ϊ2 L���ܱ�������ͨ���������巢����ѧ��Ӧ����Ӧ�и����ʵ����ʵ����仯����ͼ��ʾ���Ը÷�Ӧ���ƶϺ�������( )
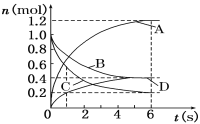
A���÷�Ӧ�Ļ�ѧ����ʽΪ3B��4D ![]() 6A��2C
6A��2C
B����Ӧ���е�1 sʱ��v(A)��v(D)
C����Ӧ���е�6 sʱ��B��ƽ����Ӧ����Ϊ0.05 mol/(L��s)
D����Ӧ���е�6 sʱ�������ʵķ�Ӧ�������
���𰸡�C
��������
���������A������ͼ��A��DΪ�����B��CΪ��Ӧ����ݻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ����A��D��B��C��ϵ��֮��1.2��0.4��(1��0.4)��(1��0. 2)=6��2��3��4����˷�Ӧ����ʽΪ3B+4C![]() 6A+2D���ʴ���B����ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�v(A)��v(D)=3��1���ʴ���C�����ݻ�ѧ��Ӧ���ʵĶ��壬v(B)=(1��0.4)/(2��6)mol/(L��s)=0.05 mol/(L��s)������ȷ��D����ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ��ʴ���
6A+2D���ʴ���B����ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�v(A)��v(D)=3��1���ʴ���C�����ݻ�ѧ��Ӧ���ʵĶ��壬v(B)=(1��0.4)/(2��6)mol/(L��s)=0.05 mol/(L��s)������ȷ��D����ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ��ʴ���


 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����к����ۡ�NaCl��Na2SO4��CaCl2�Ļ����Һ��ѡ���ʵ����Լ��ͷ��������ᴿ��NaCl���塣��Ӧ��ʵ��������£�
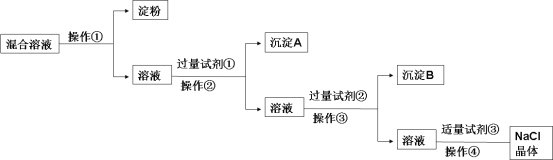
��1�������������ý��岻��ͨ�� ���ѵ��۽������Һ���з��롣
��2��д������ʵ������������Լ��Ļ�ѧʽ��
�Լ���___________________���Լ���_____________________��
��3���ж��Լ����ѹ����IJ����ǣ�__________________��
��4�������Լ��������ķ����ǣ�__________________��
��5���Լ��������ã��û�ѧ����ʽ��ʾ����__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ�鼰��ɫ������������������
A��ˮԡ���������£���ѿ��������Լ�������Ӧ����ש��ɫ����
B����������Һ��˫�����Լ�����ɫ
C���˵Ŀ�ǻ��Ƥϸ����������Ⱦɫ���Կ���������ɫ��������
D�����������£��������Ǻ������������óʺ�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ú���Al2O3��SiO2������FeOxFe2O3�������Ʊ�Al2��SO4��318H2O����������������
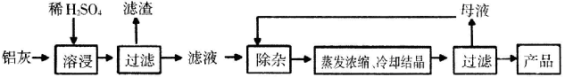
��һ�������£�MnO4-����Mn2����Ӧ����MnO2)
��֪�������������������PH

��1��H2SO4�ܽ�Al2O3�����ӷ���ʽ��____________��
��2��������Һ�л�����Fe2+�ķ�����______________��
��3�������������������¼������裺��I������Һ�м������KMnO4��Һ��������Һ��pHΪ3.2 ��II�����ȣ�����������ɫ���������ã��ϲ���Һ���Ϻ�ɫ��(��������MnSO4���Ϻ�ɫ��ʧ�����ˡ�
������I ��Ŀ���ǣ�_________��������Һ��pHΪ3.2��Ŀ����__________��
������II�ij����м���ŨHCl�����ȣ��л���ɫ�������ɣ�д���䷴Ӧ����ʽ______��
���������м���MnSO4��Ŀ����__________�������ӷ�Ӧ����ʽ��ʾ��
��4���Ӷ��ѭ��ʹ�ú�ĸҺ�пɻ��յ���Ҫ������________���ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��������ͼװ�òⶨij��п��Ʒ��п���������������Dz������Ϻ��֪�ô�п��Ʒ�е������ɷֲ�����ϡ���ᷴӦ������д����ʵ�鱨�档
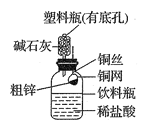
��1��ʵ��Ŀ�ģ� ��
��2��ʵ�鲽�裺
����ȡ10.0g��п����ͭ���У���ͼʾװ����װ�Ƶ�������ҩƷ������Ϊ120.0g��
����ͭ������������ϡ�����У��йط�Ӧ�Ļ�ѧ����ʽΪ ��
����Ӧ��ȫ�Ƶ�װ��������Ϊ119.8g�����п��п����������Ϊ ��
��3������̽��������֪��ʯ����NaOH��CaO�Ļ��������ڸ���������壩
����ʵ�������ü�ʯ�ң�������õĴ�п��п������������ ������ƫ��������ƫС��������Ӱ��������
��������п����ij�������ʵ�ʯ��ʯ��Ʒ������Ҳ����ϡ���ᷴӦ�����жϸ�ʵ�鷽���ܲ�������ʯ��ʯ��Ʒ��CaCO3���������IJⶨ����˵������____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ����Ҫ����Դ�������Ʊ�һϵ�����ʣ�
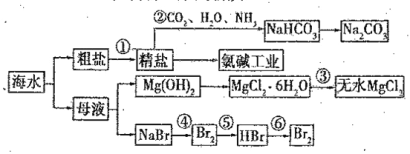
����˵����ȷ������ ��
A���������У�Ӧ��ͨCO2 ����ͨNH3
B���������ɽ�MgCl2��6H2O�����ڿ�����ֱ�Ӽ�����ˮ
C������������������Ӧ�У���Ԫ�ؾ�������
D����ȥ�����е� SO42-��Ca2+ ��Mg2+ �����ʣ������Լ�����ز���˳������ǣ�NaOH��Һ��BaCl2 ��Һ��Na2CO3 ��Һ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽���������Ƶ����ȶ��ԣ�ij�о���ѧϰС�齫��ˮ�������Ƹ����������ȣ����������Ⱥ�Ĺ�����������ͼ��ʾ��ʵ��װ�ý���ʵ�顣��ش������й����⣺
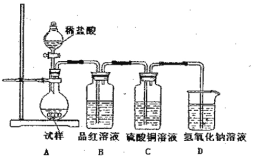
��1���������ϣ���ˮ�������Ƹ����������ȵ�600���ſ��ֽܷ⣬�ҷֽ����ֻ�����ƺ����ֹ�������������¶ȵ�����600������������ȴ����������������μ�ϡ�������������ڵμ�ϡ���������������HSO3-����������Ũ�ȱ�������Ϊ ��
��2����������¶�Ϊ700������������ȴ����������л����μ�ϡ�������������۲쵽��ƿ�г��ֵ���ɫ���������д���������������Ӧ�����ɻ�ɫ���������ӷ���ʽΪ ����ʱ��B��C��װ���п��ܹ۲쵽������Ϊ ��
��3������2���еμӶ����������ƿ�ڳ�Cl-����������һ��Ũ�Ƚϴ����������X����Ϊ�������������X������ȡ������������ˮ�����Һ��Ȼ����������ʵ�鷽��������������X������Ϊ�����ķ����� ������������������������˵����һ��������������ԭ�� ��
�����ף�ȡ����������Һ���Թ��У��ȼ�ϡHNO3���ټ�BaCl2��Һ���а�ɫ�������ɣ�֤�������Ӵ��ڡ�
�����ң�ȡ����������Һ��Һ����������ϡHCl���ټ�BaCl2��Һ,����ɫ�������ɣ�֤�������Ӵ��ڡ�
��4��д��Na2SO3������ȵ�600�������ֽ����ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڻ��������������У�����Ŀǰ��ҵ����ʵ�ʵ���( )
A��ʯ��ҵ�У����ø���ķ�����ʯ�ͷֳɲ�ͬ�е㷶Χ�IJ�Ʒ
B�����Ṥҵ�У�Ϊ�˼ӿ찱���������ʣ�ͨ��ʹ������ý������
C�����ҵ�У����ͨ�������Ͷ�����̼��ѭ�����ã������ԭ�ϵ�������
D���ϳɰ���ҵ�У����ø�ѹ����������ϳɰ���Ӧ��ƽ�ⳣ��������ԭ��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڷ�Ӧ������˵����ȷ������ ��
A��Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s)����H =��216kJ/mol��E��Ӧ����E������
B��CaCO3(s)=CaO(s)+CO2(g)����H =+178.5kJ/mol��E��Ӧ����E������
C��HI(g) ![]() 1/2H2(g)+ 1/2I2(s)����H = ��26.5kJ/mol���ɴ˿�֪1mol HI���ܱ������зֽ����Էų�26.5kJ������
1/2H2(g)+ 1/2I2(s)����H = ��26.5kJ/mol���ɴ˿�֪1mol HI���ܱ������зֽ����Էų�26.5kJ������
D��H+��aq��+OH-��aq��=H2O��l������H = ��57.3kJ/mol����1molNaOHˮ��Һ�뺬0.5mol H2SO4��Ũ�����Ϻ����57.3 kJ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com