
【题目】A、B 两种元素为同一族第三周期和第四周期元素,若 A 元素的原子序数为 x,则 B 元素的原子序数可能为( )
①x+2 ②x+8 ③x+18 ④x+32
A.③B.②C.②③D.①②
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法错误的是
A. 11 g D![]() O所含的电子数为5NA
O所含的电子数为5NA
B. 常温下,5.6 g铁与浓硝酸反应转移的电子数为0.3NA
C. 甲烷燃料电池正极消耗标况下11.2L O2时,电路中通过的电子数为2NA
D. 3H2(g)+N2(g)![]() 2NH3(g) ΔH=-92 kJ·mol-1,当放出热量为92 kJ时,转移电子数为6NA
2NH3(g) ΔH=-92 kJ·mol-1,当放出热量为92 kJ时,转移电子数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从报废后的锂电池(主要成分为LiCoO2,此外含铁、铝、铜、锰、镍等)中回收有关物质,回收工艺流程如下:
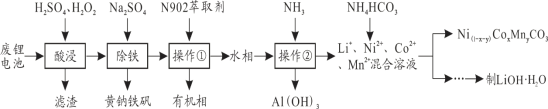
(1)操作②的名称为_______________,操作①的目的是___________________________。
(2)写出酸浸过程中LiCoO2发生氧化还原反应的化学方程式_______________________。
(3)室温下,各物质的Ksp如下表所示:(已知:lg2=0.3、1g6=0.8)
物质 | Al(OH)3 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 |
Ksp | 1×10-35 | 2×10-13 | 6×10-15 | 4×10-15 |
若水相中各金属离子浓度均为0.1mol/L,且离子浓度小于1.0×10-5mol/L,即认为该离子已完全除去,操作②需调节溶液pH的取值范围为_________。(保留1位小数)
(4)某锂离子电池正极材料含有LiNi1/3Co1/3Mn1/3O2,其中Ni、Co的化合价分别为+2、+3,则Mn的化合价为_______。该材料可通过回收的Ni(1-x-y)CoxMnyCO3与LiOH·H2O烧结得到,反应中不能隔绝空气,其原因是_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是原子序数依次增大的五种短周期主族元素,其中A的原子序数是B和D原子序数之和的1/4,C元素的单质与热水缓慢反应,且该单质可做铝热反应的引燃剂,甲和丙是D元素的两种常见氧化物,乙是B元素的单质,0.005mol/L丁溶液的pH=2,它们之间的转化关系如图所示(部分反应物省略),下列叙述正确的是
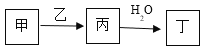
A. C、D的简单离子均能促进水的电离
B. C、E两元素形成化合物中既含有离子键又含共价键
C. A、D分别与B元素形成的化合物都是大气污染物
D. E的氧化物水化物的酸性大于D的氧化物水化物的酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. CH3CH2CH(CH3)CH3的名称为3一甲基丁烷
B. CH3CH2CH2CH2CH3和CH3CH2CH(CH3)CH3互为同素异形体
C. ![]() 和
和![]() 为同一物质
为同一物质
D. CH3CH2OH和CH2OHCHOHCH2OH具有相同的官能团,互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤废气中的氮氧化物(NOx)、CO2、SO2等气体,常用下列方法处理,以实现节能减排、废物利用等。
已知:25 ℃时,Kb(NH3·H2O)=1.8×10-5;H2SO3:Ka1=1.5×10-2,Ka2=1.0×10-7
(1)处理烟气中的SO2常用液吸法。室温条件下,将烟气通入浓氨水中得到(NH4)2SO3溶液,0.1mol/L(NH4)2SO3溶液的pH____(填“>”“<”或“=”)7。将烟气通入 (NH4)2SO3溶液可以继续吸收SO2 ,用离子方程式表示出能吸收二氧化硫的原因_________。
(2)用活性炭可以还原处理氮氧化物,有关反应为C(s)+2NO(g) ![]() N2(g)+CO2(g)。在恒容条件下,能判断该反应一定达到化学平衡状态的依据是 _______(填选项编号)。
N2(g)+CO2(g)。在恒容条件下,能判断该反应一定达到化学平衡状态的依据是 _______(填选项编号)。
A.单位时间内生成2n mol NO(g)的同时消耗n mol CO2(g)
B.混合气体的密度不再发生改变
C.反应体系的压强不再发生改变
D.混合气体的平均相对分子质量不再改变
(3)有科学家经过研究发现,用CO2和H2在210~290℃,催化剂条件下可转化生成甲醇蒸汽和水蒸气。
①230℃,向容器中投入0.5molCO2和1.5molH2,当转化率达80%时放出热量19.6kJ能量,写出该反应的热化学方程式_______________________________________。
②一定条件下,往2L恒容密闭容器中充入1.0molCO2和3.0molH2,在不同催化剂作用下,相同时间内CO2的转化率随温度变化如图1所示:
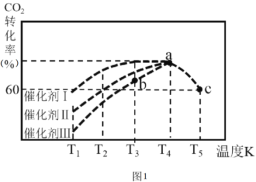
催化剂效果最佳的是催化剂 ______ (填“I”,“Ⅱ”,“Ⅲ”)。b点v(正)___v(逆) (填“>” ,“< ”,“=”)。此反应在a点时已达平衡状态,a点的转化率比c点高的原因是_______。已知容器内的起始压强为100kPa,则图中c点对应温度下反应的平衡常数Kp=________。(保留两位有效数字) (Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
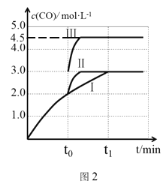
(4)一定条件下,CO2和H2也可以发生反应CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH<0,一定温度下,在3 L容积可变的密闭容器中,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ或曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是____。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是________。
CO(g)+H2O(g) ΔH<0,一定温度下,在3 L容积可变的密闭容器中,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ或曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是____。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋氯芬酸(J)是一种新型、强效解热、镇痛、抗关节炎药物,其合成路线如下图所示(部分反应条件省略):
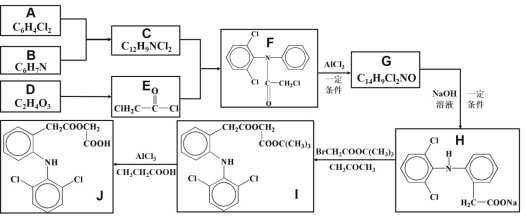
已知:①![]()
②![]()
③![]()
请回答:
(1)化合物D的名称为__________________;
(2)化合物F的分子式为________________;
(3)写出![]() 的方程式____________________________________________;
的方程式____________________________________________;
(4)![]() 的反应类型为_________________;
的反应类型为_________________;
(5)下列关于物质性质说法不正确的是_____________
A.化合物D可以发生氧化、取代、缩聚反应
B.化合物B具有碱性
C.化合物C中所有原子均可分布在同一平面
D.醋氯芬酸(J)在Ni的催化作用下与H2加成,最多可消耗8molH2
(6)已知C的同分异构体有多种,写出同时满足下列条件的同分异构体____________;(要求写出其中三种)
① 红外光谱表征分子中含有两个苯环结构 ②核磁共振氢谱显示只有5种不同环境的氢原子
(7)以苯和乙烯为原料,利用题目所给信息,写出合成 ![]() 的路线(用流程图表示,无机试剂任选)________________
的路线(用流程图表示,无机试剂任选)________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中错误的是
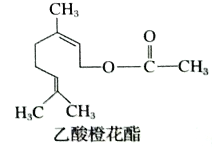
A. 分子式为C12H22O2
B. 能使酸性KMnO4溶液褪色,能发生加成反应和取代反应
C. 1mol该有机物水解时只能消耗1 mol NaOH
D. 1mol该有机物在一定条件下和H2反应,共消耗H2为2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质中只有A、B、C三种单质,A的焰色反应为黄色,主要以G形式存在于海水中,F是一种淡黄色的固体,H是一种常见的无色液体,I是造成温室效应的“元凶”,各物质间的转化关系图如下:
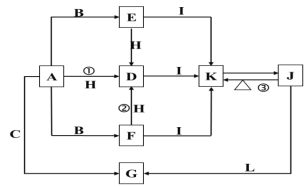
回答下列问题:
(1)A是:_____,C是:_____,L是:______,I是:____(填化学式)。
(2)写出反应①②③的化学反应方程式:
①:____________________________________;
②:____________________________________;
③:____________________________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com