
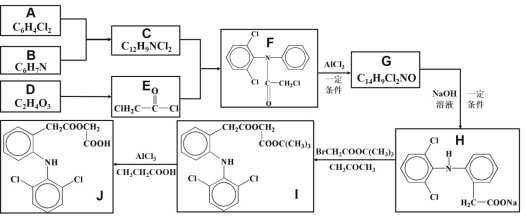
【题目】醋氯芬酸(J)是一种新型、强效解热、镇痛、抗关节炎药物,其合成路线如下图所示(部分反应条件省略):
已知:①![]()
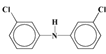
②![]()
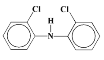
③![]()
请回答:
(1)化合物D的名称为__________________;
(2)化合物F的分子式为________________;
(3)写出![]() 的方程式____________________________________________;
的方程式____________________________________________;
(4)![]() 的反应类型为_________________;
的反应类型为_________________;
(5)下列关于物质性质说法不正确的是_____________
A.化合物D可以发生氧化、取代、缩聚反应
B.化合物B具有碱性
C.化合物C中所有原子均可分布在同一平面
D.醋氯芬酸(J)在Ni的催化作用下与H2加成,最多可消耗8molH2
(6)已知C的同分异构体有多种,写出同时满足下列条件的同分异构体____________;(要求写出其中三种)
① 红外光谱表征分子中含有两个苯环结构 ②核磁共振氢谱显示只有5种不同环境的氢原子
(7)以苯和乙烯为原料,利用题目所给信息,写出合成 ![]() 的路线(用流程图表示,无机试剂任选)________________
的路线(用流程图表示,无机试剂任选)________________
【答案】2-羟基乙酸(或α-羟基乙酸) C14H10Cl3NO 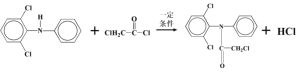 取代反应 CD
取代反应 CD ![]()
![]()
![]()
【解析】
本题首先利用倒推法并结合原子守恒,根据F的结构简式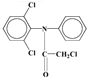 、E的结构
、E的结构![]() ,结合C的分子组成可知,C和E发生取代反应生成F和HCl,则C的结构简式为
,结合C的分子组成可知,C和E发生取代反应生成F和HCl,则C的结构简式为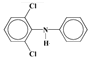 ;由此推出A和B中均含有一个苯环,结合A和B的分子式及C的结构简式,可知A和B发生取代生成C和H2,则A的结构简式为
;由此推出A和B中均含有一个苯环,结合A和B的分子式及C的结构简式,可知A和B发生取代生成C和H2,则A的结构简式为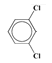 、B的结构简式为
、B的结构简式为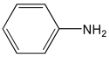 ;F在AlCl3作催化剂的作用下发生类似信息①的反应,产物G在NaOH溶液中碱化后得到的H为
;F在AlCl3作催化剂的作用下发生类似信息①的反应,产物G在NaOH溶液中碱化后得到的H为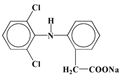 ,则G的结构简式为
,则G的结构简式为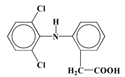 ;由E的结构简式为
;由E的结构简式为![]() ,结合D的分子式C2H4O3可知其结构简式为HOCH2COOH,据此分析解题即可。
,结合D的分子式C2H4O3可知其结构简式为HOCH2COOH,据此分析解题即可。
利用倒推法并结合原子守恒,根据F的结构简式 、E的结构
、E的结构![]() ,结合C的分子组成可知,C和E发生取代反应生成F和HCl,则C的结构简式为
,结合C的分子组成可知,C和E发生取代反应生成F和HCl,则C的结构简式为 ;由此推出A和B中均含有一个苯环,结合A和B的分子式及C的结构简式,可知A和B发生取代生成C和H2,则A的结构简式为
;由此推出A和B中均含有一个苯环,结合A和B的分子式及C的结构简式,可知A和B发生取代生成C和H2,则A的结构简式为 、B的结构简式为
、B的结构简式为 ;F在AlCl3作催化剂的作用下发生类似信息①的反应,产物G在NaOH溶液中碱化后得到的H为
;F在AlCl3作催化剂的作用下发生类似信息①的反应,产物G在NaOH溶液中碱化后得到的H为 ,则G的结构简式为
,则G的结构简式为 ;由E的结构简式为
;由E的结构简式为![]() ,结合D的分子式C2H4O3可知其结构简式为HOCH2COOH;(1)化合物D的结构简式为HOCH2COOH,则名称为2-羟基乙酸(或α-羟基乙酸);(2)化合物F的结构简式
,结合D的分子式C2H4O3可知其结构简式为HOCH2COOH;(1)化合物D的结构简式为HOCH2COOH,则名称为2-羟基乙酸(或α-羟基乙酸);(2)化合物F的结构简式 ,则其分子式为C14H10Cl3NO;(3)C(
,则其分子式为C14H10Cl3NO;(3)C(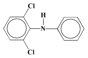 )和E(
)和E(![]() )发生取代反应生成F和HCl,发生反应的化学方程式为
)发生取代反应生成F和HCl,发生反应的化学方程式为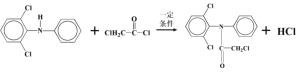 ;(4)F在AlCl3作催化剂的作用下发生类似信息①的反应,生成
;(4)F在AlCl3作催化剂的作用下发生类似信息①的反应,生成 ,可知F
,可知F![]() 的反应类型为取代反应;(5)A.化合物D的结构简式为HOCH2COOH,分子组成含有醇羟基,可发生催化氧化、与羧酸发生酯化反应,即取代反应,另外还含有羧基,可以发生缩聚反应生成聚合酯,故A正确;B.化合物B的结构简式为
的反应类型为取代反应;(5)A.化合物D的结构简式为HOCH2COOH,分子组成含有醇羟基,可发生催化氧化、与羧酸发生酯化反应,即取代反应,另外还含有羧基,可以发生缩聚反应生成聚合酯,故A正确;B.化合物B的结构简式为![]() ,分子结构中含有氨基,显碱性,故B正确;C.化合物C的结构简式为
,分子结构中含有氨基,显碱性,故B正确;C.化合物C的结构简式为 ,分子组成中N原子为sp3杂化,为立体结构,则分子内所有原子不可能分布在同一平面内,故C错误;D.醋氯芬酸(J)的结构简式为
,分子组成中N原子为sp3杂化,为立体结构,则分子内所有原子不可能分布在同一平面内,故C错误;D.醋氯芬酸(J)的结构简式为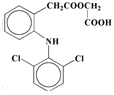 ,分子组成内含有二个苯环,在Ni的催化作用下与H2加成,最多可消耗6molH2,故D错误;故答案为CD;(6)C为
,分子组成内含有二个苯环,在Ni的催化作用下与H2加成,最多可消耗6molH2,故D错误;故答案为CD;(6)C为 ,其同分异构体有多种,其中同时满足① 红外光谱表征分子中含有两个苯环结构、②核磁共振氢谱显示只有5种不同环境的氢原子,说明分子结构对称性较强,例如:
,其同分异构体有多种,其中同时满足① 红外光谱表征分子中含有两个苯环结构、②核磁共振氢谱显示只有5种不同环境的氢原子,说明分子结构对称性较强,例如:![]() 、
、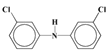 、
、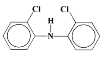 或
或![]() 均符合;(7)结合信息①合成
均符合;(7)结合信息①合成![]() 只需要有
只需要有![]() 在AlCl3催化剂作用下即可生成
在AlCl3催化剂作用下即可生成![]() ,则需要在考虑在苯环上先引入烃基即可,即
,则需要在考虑在苯环上先引入烃基即可,即![]() 与CH2ClCH2Cl在AlCl3催化剂作用下即可生成
与CH2ClCH2Cl在AlCl3催化剂作用下即可生成![]() ,再与NaCN发生取代反应并水解得到羧基,即得到
,再与NaCN发生取代反应并水解得到羧基,即得到![]() ,最后与SOCl2在催化剂作用下生成酰氯,得到
,最后与SOCl2在催化剂作用下生成酰氯,得到![]() ,故以苯和乙烯为原料,合成
,故以苯和乙烯为原料,合成 ![]() 的路线为
的路线为![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列各组离子,在强酸性溶液中可以大量共存的是
A. Na+、Ca2+、SO42- B. Ag+、K+、NO3-
C. Ba2+、HCO3-、NO3- D. Na+、NO3-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,前者属于电解质,后者属于非电解质的是( )
A. NaCl晶体、BaSO4 B. 铜、二氧化硫
C. 液态的醋酸、酒精 D. 熔融的KNO3、硫酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B 两种元素为同一族第三周期和第四周期元素,若 A 元素的原子序数为 x,则 B 元素的原子序数可能为( )
①x+2 ②x+8 ③x+18 ④x+32
A.③B.②C.②③D.①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同情况下测得A(g)+3B(g)![]() 2C(g)+2D(g)的下列反应速率,其中反应速率最大的是
2C(g)+2D(g)的下列反应速率,其中反应速率最大的是
A. υ(D)=0.01 molL-1s-1 B. υ(C)=0.5 molL-1min-1
C. υ(B)=0.6 molL-1min-1 D. υ(A)=0.2molL-1min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图是研究二氧化硫性质的微型实验装置(实验时用另一表面皿扣在上面)。现用75%硫酸溶液和亚硫酸钠晶体反应制取SO2气体并进行实验,实验现象很明显。下列说法中错误的是

A.品红溶液褪色
B.紫色石蕊溶液先变红后褪色
C.酸性KMnO4溶液紫色褪去
D.含酚酞的NaOH溶液红色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH<0。在其他条件一定,只改变某一条件时,下列分析不正确的是
2SO3(g) ΔH<0。在其他条件一定,只改变某一条件时,下列分析不正确的是

A. 图Ⅰ表示的是t1时刻增大压强对反应速率的影响
B. 图Ⅱ表示的是t1时刻加入催化剂对反应速率的影响
C. 图Ⅲ表示的是温度对平衡的影响,且甲的温度小于乙的温度
D. 图Ⅲ表示的是催化剂对化学平衡的影响,乙使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期中的18种元素具有重要的用途,在现代工业中备受青睐。
(1)钛原子的价电子排布式为______________________,TiCl4沸点136℃,熔点-25℃,晶体类型为___________晶体。
(2)铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是______________________。
(3)与As同主族的短周期元素是N、P。AsH3中心原子轨道杂化的类型_________________;一定压强下将AsH3、NH3和PH3的混合气体降温时液化顺序是______________________,理由是______________________。
(4)铬是一种硬而脆抗腐蚀性强的金属,常用于电镀和制造特种钢。下图1为铬的晶胞结构图,则铬晶胞属于___________堆积;该晶胞中原子的体积占晶胞体积的百分率为___________。

(5)钴晶体的一种晶胞(如图2所示)的边长为anm,密度为ρg·cm-3,NA表示阿伏加德罗常数的值,则钴原子半径为___________mm,钴的相对原子质量可表示为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有未知浓度的Ba(OH)2和NaOH混合溶液,量取四份该溶液分别通入等量的CO2(已折算成标准状况下的体积,不考虑CO2在水中的溶解),生成沉淀的物质的量如下表:
实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
CO2体积(mL) | 2352 | 2352 | 2352 | 2352 |
样品体积(mL) | 20.0 | 30.0 | 40.0 | 50.0 |
沉淀物质的量(×10-2mol) | 1.50 | 4.50 | 6.00 | 7.50 |
(1)该混合溶液中Ba(OH)2的物质的量浓度=_____________。
(2)实验Ⅲ最后所得溶液中碳酸钠的物质的量=___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com