
| A、汽油、苯、乙醇都属于烃类物质 |
| B、含5个碳原子的有机物,分子中最多可形成5个碳碳单键 |
| C、等物质的量的乙醇和乙酸完全燃烧时所需氧气的质量相等 |
| D、二氧化硫和乙烯都能使溴水褪色,二者反应原理相同 |


科目:高中化学 来源: 题型:
| A、电子层数逐渐增多 |
| B、最高价氧化物的水化物的碱性减弱,酸性增强 |
| C、最高正化合价数值逐渐增大 |
| D、从硅到氯,最低负化合价从-4到-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、254g I2(g)中通入2g H2(g),反应放热9.48kJ |
| B、1mol固态碘与1mol气态碘所含的能量相差l7.00kJ |
| C、反应(Ⅰ)的产物比反应(Ⅱ)的产物稳定 |
| D、反应(Ⅰ) 拆开1mol I-I键与1mol H-H键需要的总能量小于拆开2mol H-I键需要的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、168g | B、42g |
| C、126g | D、60g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯酚钠溶液中通入少量CO2 2C6H5ONa+CO2+H2O→2C6H5OH+Na2CO3 | ||
B、乙酸乙酯在酸性条件下水解 CH3COOCH2CH3+H218O
| ||
C、溴乙烷的消去反应 C2H5Br+NaOH
| ||
D、乙醛和银氨溶液反应 CH3CHO+2Ag(NH3)2OH
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在硅酸钠溶液中滴入稀盐酸,溶液变浑浊,说明Cl元素的非金属性强于Si元素 |
| B、Zn与稀硫酸反应时,滴加少量CuSO4溶液,反应速率加快,说明CuSO4在该反应中起催化剂作用 |
| C、用酚酞作指示剂,盐酸滴定Na2CO3溶液,达到滴定终点时,离子浓度关系为:c(Na+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+) |
| D、将NaAlO2溶液与NaHCO3溶液混合,出现白色沉淀,是两种溶液水解相互促进的结果 |
查看答案和解析>>
科目:高中化学 来源: 题型:
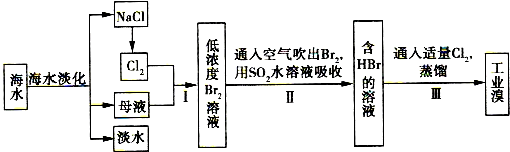
查看答案和解析>>
科目:高中化学 来源: 题型:
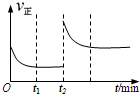 一定温度下,在一个10L密闭容器中只投反应物发生某可逆反应,其平衡常数表达式为K=
一定温度下,在一个10L密闭容器中只投反应物发生某可逆反应,其平衡常数表达式为K=| c(CO)?c(H2) |
| c(H2O) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com