
 的酸性废水,最终使铬元素以Cr(OH)3沉淀的形式除去。某科研小组用该原理处理污水,设计装置如图所示。下列说法一定不正确的是( )
的酸性废水,最终使铬元素以Cr(OH)3沉淀的形式除去。某科研小组用该原理处理污水,设计装置如图所示。下列说法一定不正确的是( )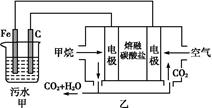
| A.燃料电池中若有1.6 g CH4参加反应,则甲中C电极理论上生成气体体积为8.96 L |
| B.实验时若污水中离子浓度较小,导电能力较差,可加入适量的Na2SO4 |
C.该燃料电池正极的电极反应式为:O2+4e-+2CO2=2C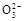 |
D.甲中阳极附近溶液中的离子反应方程式是:Cr2 +6Fe2++14H+=2Cr3++6Fe3++7H2O +6Fe2++14H+=2Cr3++6Fe3++7H2O |
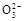 ,负极反应为:CH4-8e-+4C
,负极反应为:CH4-8e-+4C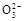 =5CO2+2H2O,C正确;B项,Na2SO4是电解质,可增强导电性,同时对污水中阴、阳离子的放电都没有影响,正确;甲中Fe溶解:Fe-2e-=Fe2+,生成的Fe2+具有还原性,所以将Cr2
=5CO2+2H2O,C正确;B项,Na2SO4是电解质,可增强导电性,同时对污水中阴、阳离子的放电都没有影响,正确;甲中Fe溶解:Fe-2e-=Fe2+,生成的Fe2+具有还原性,所以将Cr2 还原,依题干中信息知:该还原过程要消耗H+,形成Cr3+,进而形成Cr(OH)3沉淀,配平方程式即可,D正确。
还原,依题干中信息知:该还原过程要消耗H+,形成Cr3+,进而形成Cr(OH)3沉淀,配平方程式即可,D正确。

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源:不详 题型:单选题
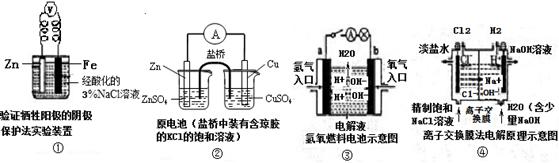
| A.装置①中烧杯内中加入黄色的K3[Fe(CN)6]溶液,一段时间后看不到Fe电极附近有蓝色沉淀生成,该装置可看作金属的析氢腐蚀 |
| B.装置②盐桥中的Cl—向硫酸铜溶液移动 |
| C.装置③中外电路电流方向:b极 →a极 |
| D.装置④中阳极反应:2 Cl——2e- = Cl2 ↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
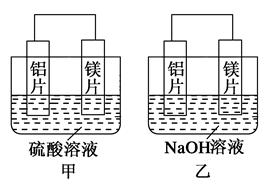
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属性不一定比铝的金属性强 |
| C.该实验说明金属活动性顺序表已过时,没有实用价值了 |
| D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 MgxMo3S4,下列说法错误的是( )
MgxMo3S4,下列说法错误的是( )| A.放电时Mg2+向正极迁移 |
| B.放电时正极反应为Mo3S4+2xe-=Mo3S42x- |
| C.充电时Mo3S4发生氧化反应 |
| D.充电时阴极反应为Mg2++2e-=Mg |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
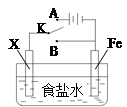
| A.若X为锌棒,开关K置于A处,可减缓铁的腐蚀,这种方法称为牺牲阴极的阳极保护法 |
B.若X为铜棒,开关K置于A处,装置中发生的总反应为2NaCl+2H2O 2NaOH+Cl2↑+H2↑ 2NaOH+Cl2↑+H2↑ |
| C.若X为碳棒,开关K置于B处,在铁棒附近滴入铁氰化钾溶液可看到溶液变血红色 |
| D.若X为碳棒,开关K置于B处,向食盐水中滴入酚酞溶液可看到碳棒附近先变红 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电镀时,通常把待镀的金属制品作阳极 |
| B.氯碱工业是电解熔融的NaCl,在阳极能得到Cl2 |
C.如图中电子由Zn极流向Cu,盐桥中的Cl-移向CuSO4溶液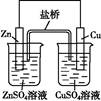 |
| D.氢氧燃料电池(酸性电解质)中O2通入正极,电极反应为:O2+4H++4e-=2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是( )| A.电池放电是化学能转化成电能的过程 |
B.放电时正极反应为:Fe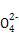 +4H2O+3e- +4H2O+3e-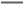 Fe(OH)3+5OH- Fe(OH)3+5OH- |
| C.充电时电池的负极接外电源的正极 |
| D.充电时电解质溶液中的阴离子向阳极定向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
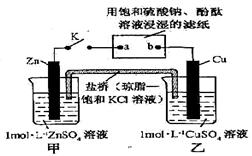
A.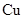 电极上发生还原反应 电极上发生还原反应 |
B.电子沿Zn a a b b Cu路径流动 Cu路径流动 |
| C.片刻后甲池中c(SO42—)增大 |
| D.片刻后可观察到滤纸b点变红色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com