
【题目】人们习惯上把电解饱和食盐水的工业叫做氯碱工业. 如图表示电解饱和NaCl溶液的装置,X、Y是石墨棒.实验开始时,在两边同时各滴入几滴酚酞溶液,请回答以下问题: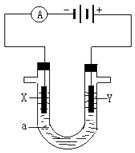
①X极上的电极反应式是 , 在X极附近观察到的现象是;
②Y电极上的电极反应式是 , 检验该电极反应产物的方法是 .
③电解NaCl溶液的离子方程式是 .
【答案】["2H++2e﹣═H2↑","放出气体,溶液变红","2Cl﹣﹣2e﹣═Cl2↑","把湿润的淀粉碘化钾试纸放在Y电极附近,试纸变蓝色","2Cl﹣+2H2O ![]() Cl2↑+H2↑+2OH﹣"]
Cl2↑+H2↑+2OH﹣"]
【解析】解:①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e﹣=H2↑,在X极附近观察到的现象是放出气体,溶液变红,
所以答案是:2H++2e﹣═H2↑;放出气体,溶液变红;
②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl﹣﹣2e﹣=Cl2↑,检验氯气的方法是把湿润的淀粉碘化钾试纸放在Y电极附近,试纸变蓝色,
所以答案是:2Cl﹣﹣2e﹣═Cl2↑;把湿润的淀粉碘化钾试纸放在Y电极附近,试纸变蓝色;
③电解氯化钠溶液得到氯气、氢气和氢氧化钠,离子方程式为2Cl﹣+2H2O ![]() Cl2↑+H2↑+2OH﹣,
Cl2↑+H2↑+2OH﹣,
所以答案是:2Cl﹣+2H2O ![]() Cl2↑+H2↑+2OH﹣.
Cl2↑+H2↑+2OH﹣.


 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】下列反应适用于工业生产的是
A.电解熔融氯化铝可得到金属铝B.光照氯气和氢气的混合物生产盐酸
C.氯气与石灰乳作用制漂白粉D.二氧化锰和浓盐酸共热,制取氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于0.1 mol/L碳酸钠溶液的叙述正确的是( )
A.溶液中阴离子的物质的量为0.1 mol
B.加水稀释时水解平衡向正反应方向移动,溶液中所有离子浓度均减小
C.升高温度,水解平衡向正反应方向移动
D.加入氢氧化钠固体,可以使溶液中c(Na+):c(CO ![]() 2﹣)=2:1
2﹣)=2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空: 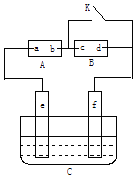
①电源A上的a为极
②欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为: , 电极f上发生的反应为 , 槽中盛放的镀液可以是溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧锌锰于电池内部的黑色物质A主要含有MnO2、MnOOH、NH4Cl、ZnCl2、炭粉,用A制备高纯MnCO3的流程圈如下:
![]()
(1)锌锰干电池的负极材料是__________(填化学式)。
(2)第I步操作得滤渣的成分是______;第II步在空气中灼烧的目的除了将MnOOH转化为MnO2外,另一作用是__________。
(3)步骤I中制得MnSO4溶液,该反应的化学方程式为____________。用草酸(H2C2O4)而不用双氧水(H2O2)作还原剂的原因是_________。
(4)已知:MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;Mn(OH)2开始沉淀时pH为7.7。
第IV步多步操作可按以下步骤进行:
操作l:加入NH4HCO3溶液调节溶液pH<7.7,充分反应直到不再有气泡产生;
操作2:过滤,用少量水洗涤沉淀2~3次;
操作3:检测滤液;
操作4:用少量无水乙醇洗涤2~3次;
操作5:低温烘干。
①操作1发生反应的离子方程式为_________;若溶液pH>7.7,会导致产品中混有____(填化学式)。
②操作3中,检测MnCO3是否洗净的方法是___________。
③操作4用少量无水乙醇洗涤的作用是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大约占细胞鲜重总量97%的元素主要是
A.C、H、O、N、P、SB. C、H、O、N、P、K
C.C、H、O、N、Cu、MgD.N、P、S、K、Ca、Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中是因为发生加成反应而褪色的是( )
A. 苯使溴水褪色 B. 乙炔通入酸性KMnO4溶液后使之褪色
C. 乙烯通入溴水后使溴水褪色 D. 甲苯与酸性KMnO4溶液混合后使之褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com