
����Ŀ����������Ҿ������õĽ��ȡ���ʹ�����ס�����ʪ���ã���������ҵĺϳ�·�����£�
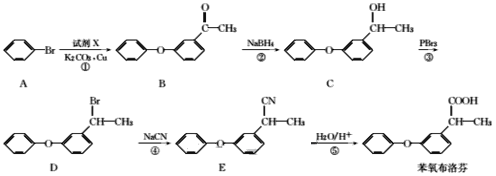
�ش��������⣺
(1)����������й����ŵ�����Ϊ___��
(2)̼ԭ��������4����ͬ��ԭ�ӻ����ʱ����̼��Ϊ����̼��A-D���������У���������̼���л���Ϊ___������ĸ����
(3)��Ӧ�ڵķ�Ӧ������___��
(4)�����̢ٷ�������ȡ����Ӧ������һ�ֲ���ΪHBr����A����B������Ӧ�Ļ�ѧ����ʽΪ___��
(5)�л���M��C��Ϊͬ���칹�壬M��������������
I.����FeCl3��Һ������ɫ��Ӧ��1molM������2molNaOH��
��.M��������6�ֲ�ͬ��ѧ�������⣬�˴Ź�������Ϊ3��2��2��2��2��3���ҷ����к���![]() �ṹ��
�ṹ��
M�Ľṹ��___�֣�д������һ�ֽṹ��ʽ��___��
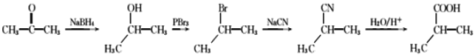
(6)��������֪ʶ����������Ϣ��д���Ա�ͪ(CH3COCH3)Ϊԭ���Ʊ�2һ������ĺϳ�·������ͼ�����Լ����ã�___��
���𰸡��Ѽ����Ȼ� CD ��ԭ��Ӧ(д�ӳɷ�ӦҲ�÷�) 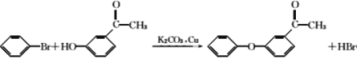 2
2 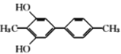 ��
��
��������
�ϳɱ�������ң����屽Ϊԭ�ϣ����Լ�X������Ӧ����B��������(4)��֪����һ����ΪHBr���ɴ˿��Ƴ��Լ�XΪ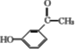 �������ķ�ӦΪȡ����Ӧ����B��C���ʻ�ת��Ϊ���ǻ�����C��D��-OHת��Ϊ-Br����D��E��-Brת��Ϊ-CN����E�����-CNת��Ϊ-COOH��
�������ķ�ӦΪȡ����Ӧ����B��C���ʻ�ת��Ϊ���ǻ�����C��D��-OHת��Ϊ-Br����D��E��-Brת��Ϊ-CN����E�����-CNת��Ϊ-COOH��
(1)�ӱ�������ҵĽṹʽ�п��Կ����������������ŵ�����Ϊ�Ѽ����Ȼ�����Ϊ���Ѽ����Ȼ���
(2)A-D���������У�A��Bû������̼ԭ�ӣ�C�е���-OH����̼ԭ��Ϊ����̼ԭ�ӣ�D����-Br����̼ԭ��Ϊ����̼ԭ�ӡ���Ϊ��CD��
(3)��Ӧ���У�NaBH4���ʻ�ת��Ϊ���ǻ�����Ӧ�����ǻ�ԭ��Ӧ����Ϊ����ԭ��Ӧ(д�ӳɷ�ӦҲ�÷�)��
(4)�����̢ٷ�������ȡ����Ӧ������һ�ֲ���ΪHBr����A����B������Ӧ�Ļ�ѧ����ʽΪ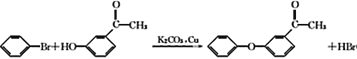 ����Ϊ��
������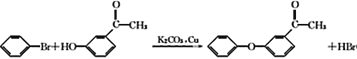 ��
��
(5)����������I.����FeCl3��Һ������ɫ��Ӧ��1molM������2molNaOH����.M��������6�ֲ�ͬ��ѧ�������⣬�˴Ź�������Ϊ3��2��2��2��2��3���ҷ����к���![]() �ṹ�����л���M��C��Ϊͬ���칹�壬����Ӧ����2��-CH3��2��-OH����2��-OHλ��ͬһ�������ĶԳ�λ�ã�2��-CH3ҲӦ����һ���ĶԳ��ԣ��ɴ˿�ȷ������������ͬ���칹��Ľṹ��ʽΪ
�ṹ�����л���M��C��Ϊͬ���칹�壬����Ӧ����2��-CH3��2��-OH����2��-OHλ��ͬһ�������ĶԳ�λ�ã�2��-CH3ҲӦ����һ���ĶԳ��ԣ��ɴ˿�ȷ������������ͬ���칹��Ľṹ��ʽΪ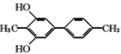 ��
��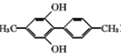 ����2�֡���Ϊ��2��
����2�֡���Ϊ��2�� ��
�� ��
��
(6)�����������ͼ�ṩ����Ϣ����ͪ(CH3COCH3)��ת��Ϊ�����������PBr3����ת��Ϊ2-����飬����HCN����ȡ����Ӧ������(CH3)2CHCN�����������������ת��Ϊ2һ�����ᡣ��ϳ�·������ͼΪ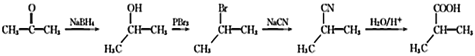 ����Ϊ��
������ ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС�����������װ�ý���ʵ�飬�ڡ�������Һ���������������������±���
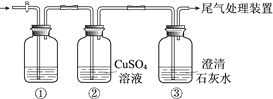
ʵ�� | ���� | ���� |
�� | ��ʢ��Na2S��Һ�Ģ��г���ͨ��CO2������ | ���в�����ɫ��������Һ��pH���ͣ� ���в�����ɫ���ǣ��û�������ð���� |
�� | ��ʢ��NaHCO3��Һ�Ģ��г���ͨ��H2S���������� | ����ͬʵ��� |
���ϣ�CaS��ˮ��ȫˮ��
������ʵ��ó��Ľ�������ȷ����
A.���а�ɫ������CaCO3
B.������ҺpH���͵�ԭ���ǣ�H2S+Cu2+ == CuS��+2H+
C.ʵ�����з����ķ�Ӧ�ǣ�CO2+H2O+ S2== CO32+ H2S
D.��ʵ���͢��ܱȽ�H2CO3��H2S���Ե�ǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾװ�ÿ��Խ���������CO2ת��Ϊȼ������CO.����˵���У���ȷ����( )
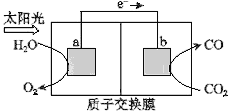
A.��װ�ù���ʱ��H����b������a�����ƶ�
B.��װ����ÿ����1 mol CO��ͬʱ����1 mol O2
C.�缫a���淢����ԭ��Ӧ
D.�ù����ǽ�̫����ת��Ϊ��ѧ�ܵĹ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����û�ѧ��ȼ�ռ������������ȼ�������ʡ���ѧ��ȼ�ռ����Ļ���ԭ���ǽ���������(��Fe2O3��FeO��)��ȼ�������ֱ�ӽӴ��Ĵ�ͳȼ�շ�Ӧ�ֽ�Ϊ�������̷�Ӧ��ȼ�����������Ӵ������������������е��������ݸ�ȼ�ϡ��ش��������⣺
��.��Fe2O3���������Ļ�ѧ��ȼ��ѭ��ת����Ӧ�IJ����Ȼ�ѧ����ʽ���£�ѭ��ת����ԭ����ͼ��ʾ��
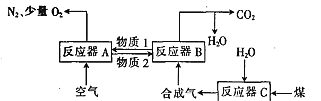
��C(s) ��H2O(g) = CO(g)�� H2(g) ��H = akJmol-1
��CO(g)�� H2(g) �� O2(g) = CO2(g) ��H2O(g) ��H = bkJmol-1
(1)д��ͼ���ܷ�Ӧ���Ȼ�ѧ����ʽ��_____________________________
(2)��������Ӧ��A��õ���β��___________(������������������)ֱ��������ҵ�ϳɰ���ԭ������ԭ����_____________________��
��.��FeO�������������ַ�Ӧ��lgKp [K����ƽ���ѹ(ƽ���ѹ=��ѹ�����ʵ�������)����ƽ��Ũ��]���¶ȵĹ�ϵ��ͼ��ʾ��
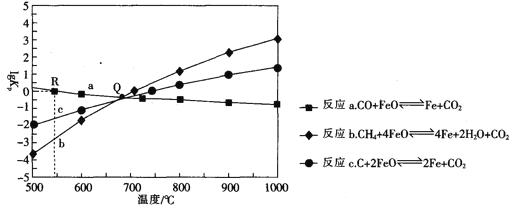
(3)ͼ���漰�ķ�Ӧ�У��������ȷ�Ӧ���Ƿ�Ӧ_________________(����ĸ)��
(4)R���Ӧ�¶��£���ij�����ܱ�������ͨ��1molCO��������������FeO��ֻ������ӦCO(g)�� FeO(s) ![]() CO2(g) ��Fe(s)����CO��ƽ��ת����Ϊ______________.
CO2(g) ��Fe(s)����CO��ƽ��ת����Ϊ______________.
��.��T���£���ij�����ܱ������м���1molCH4(g)��4mol FeO(s)���з�Ӧ��CH4(g) �� 4FeO(s) ![]() 4Fe(s) ��2H2O(g) ��CO2(g)����Ӧ��ʼʱѹǿΪP0����Ӧ������10minʱ�ﵽƽ��״̬����ô�ʱ����������ѹǿ����ʼѹǿ��2����
4Fe(s) ��2H2O(g) ��CO2(g)����Ӧ��ʼʱѹǿΪP0����Ӧ������10minʱ�ﵽƽ��״̬����ô�ʱ����������ѹǿ����ʼѹǿ��2����
(5)T���£��÷�Ӧ��Kp = _____________________.
(6)����ʼʱ��������м���1molCH4(g)��4molFeO(s)��1mol H2O(g)��0.5molCO2(g)����ʱ��Ӧ��__________________(��������Ӧ�������淴Ӧ��)������С�
(7)�����������䣬������������Ϊ��ѹ�ܱ����������ʱCH4��ƽ��ת����___________(��������������С������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Դ�Ŀ��������þ��й�����ǰ������ˮ��pHһ����7.5~8.6֮�䡣ij�غ�ˮ����Ҫ���ӵĺ������±���
�ɷ� | Na+ | K+ | Ca2+ | Mg2+ | Cl�� | SO42�� | HCO3�� |
����/mgL��1 | 9360 | 83 | 160 | 1100 | 16000 | 1200 | 118 |
��1����ˮ�������Ե�ԭ���ǣ������ӷ���ʽ��ʾ����____________���ú�ˮ��Ca2+�����ʵ���Ũ��Ϊ__________mol/L ��
��2�����������ǽ��귢չ������һ�ֽϺõĺ�ˮ������������ԭ������ͼ��ʾ�����������������ӽ���Ĥֻ����������������ͨ�����缫��Ϊ���Ե缫��

�� ��ʼʱ�����ĵ缫��ӦʽΪ________________��
�� ���һ��ʱ�䣬____���������������������������ˮ������ɷ�Ϊ_____���ѧʽ����
�� ��ˮ�ij���Ϊa��b��c�е�__________���ڡ�
��3����ˮ���Ԫ�ش����dz��ḻ���Ӻ�ˮ����ȡ﮵��о�����DZ����������컯ѧ��Դ����Ҫԭ�ϣ���LiFePO4���ij�缫�Ĺ���ԭ����ͼ��ʾ��

�õ�ص����Ϊ�ܴ��� Li+�Ĺ�����ϡ�
������ͼ�е�С�ڵ��ʾ_____�������ӷ��ţ������ʱ�õ缫��ӦʽΪ_______��
��4�����ú�����Դ�ɻ��MnO2 ��MnO2�������Ʊ�������أ���MnO2��KOH��Ϻ��ڿ����м������ڣ��õ���ɫ������أ�K2MnO4��������������������������ɸ�����ء����Ʊ�������������ͬ�����������Ϳ����������Ϊ_________�����������������������20%�ƣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����֪̼�H2CO3��Ki1��4.3��10��7��Ki2��5.6��10��11�����H2C2O4��Ki1��5.9��10��2��Ki2��6.4��10��5
��0.1mol��L��1Na2CO3��Һ��pH____0.1mol��L��1Na2C2O4��Һ��pH����������������С����������������
��̼������Һ�Լ��Ե�ԭ����_____________________________ ��������Ҫ�����ӷ���ʽ��ʾ��
��������Ũ�ȵIJ�����Һ��̼����Һ�������ϣ���Һ�и�������Ũ�ȴ�С��˳����ȷ����______������ĸ����
a��c��H����>c��HC2O4-��>c��HCO3-��>c��CO32-��
b��c��HCO3-��>c��HC2O4-��>c��C2O42-��>c��CO32-��
c��c��H����>c��HC2O4-��>c��C2O42-��>c��CO32-��
d��c��H2CO3��>c��HCO3-��>c��HC2O4-��>c��CO32-��
��2���ð�ˮ��ȥSO2��
��֪25����NH3��H2O��Kb��1.8��10��5��H2SO3��Ka1��1.3��10��2��Ka2��6.2��10��8������ˮ��Ũ��Ϊ2.0mol��L��1����Һ�е�c��OH������________mol��L��1����SO2ͨ��ð�ˮ�У���c��OH��������1.0��10��7mol��L��1ʱ����Һ�е�c��SO32-��/c��HSO3-����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ������ȷ����
A. NaHCO3��ˮ�⣺HCO3����H2O![]() H3O����CO32��
H3O����CO32��
B. ����ĵ��룺CH3COOH��CH3COO����H��
C. H2��ȼ����Ϊ285.8 kJ/mol�����ʾH2ȼ���ȵ��Ȼ�ѧ����ʽΪ��H2(g)��1/2O2(g)��H2O(g) ��H����285.8 kJ/mol
D. ̼��Ƶ��ܽ�ƽ�⣺CaCO3(s)![]() Ca2��(aq)��CO32��(aq)
Ca2��(aq)��CO32��(aq)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ʵ����ʵ�����ƽ�ⷽ��ʽ����ȷ����
ʵ����ʵ | ���ƽ�� | |
A | ����NaHCO3ʹ��ˮ��Ư��������ǿ | Cl2+H2O |
B | ����FeCl3��Һʱ���������� | Fe3++3OH�� |
C | ����CO2��������ˮpH��5.6 | H2O+CO2 |
D | CaCO3������������ | CaCO3(s) |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����³�ѹ�£�ij�����л���ײ���(MOFA)��CO2���г��ߵ��������������ܴ�CO2�뻷������ķ�Ӧ���乤��ԭ����ͼ��ʾ������˵���������
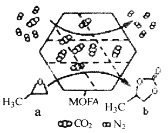
A.����a������̼ԭ�Ӻ���ԭ�Ӿ���ȡsp3�ӻ�
B.b��һ�ȴ�����3��
C.a����b�ķ�Ӧ����Ϊȡ����Ӧ�����м��Թ��ۼ��γ�
D.�ò��ϵ��������þ���ѡ���ԣ����ô˷��ɼ���CO2���ŷ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com