
【题目】请根据表格中提供的甲、乙、丙、丁四种元素的相关信息完成下列问题:
元素 | 甲 | 乙 | 丙 | 丁 |
原子序数 | 11 | ③ | ||
元素符号 | ② | S | ||
原子结构示意图 | ① |
| ||
元素周期表中的位置 | 第三周期 ⅢA族 | ④ |
(1)填写表格中各序号所对应的空白:①_________________②__________________
③_________________④_________________。
(2)甲、乙、丙、丁四种元素中,原子半径最大的是_______(填元素符号),丁元素的最高正价为____价(填化合价)。
(3)最高价氧化物对应水化物的碱性:甲_______________乙(填“>”或“<”),简单气态氢化物的稳定性:丙_______________丁(填“>”或“<”)。
(4)元素乙的最高价氧化物对应水化物,既能与元素甲的最高价氧化物对应水化物反应,又能中和过多的胃酸。
请分别写出上述反应的离子方程式:_____________;______________。
(5)丁单质通入冷的消石灰中可制得漂白粉,写出该反应的化学方程式:_____________________。
【答案】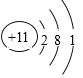 Al 16 三周期VIIA族 Na +7 > < Al (OH)3 + OH- = AlO
Al 16 三周期VIIA族 Na +7 > < Al (OH)3 + OH- = AlO![]() +2 H2O Al (OH)3 + 3H+= Al3++3 H2O 2 Cl2 + 2 Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2 H2O
+2 H2O Al (OH)3 + 3H+= Al3++3 H2O 2 Cl2 + 2 Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2 H2O
【解析】
甲的原子序数是11,应为Na元素;乙为第三周期ⅢA族元素,则乙为Al元素;丙的元素符号为S,则为硫元素,核电荷数是16;丁的原子结构示意图为![]() ,则为Cl元素,再结合元素周期律分析解题。
,则为Cl元素,再结合元素周期律分析解题。
由分析知:甲为Na元素、乙为Al元素、丙为S元素、丁为Cl元素;
(1①甲为Na元素,其原子结构示意图为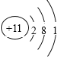 ;②为铝元素,元素符号为Al;③乙为硫元素,原子序数是16;④丁为氯元素,其在元素周期表中的位置是三周期VIIA族;
;②为铝元素,元素符号为Al;③乙为硫元素,原子序数是16;④丁为氯元素,其在元素周期表中的位置是三周期VIIA族;
(2)同周期主族元素,核电荷数越大,原子半径越小,则甲、乙、丙、丁四种元素中,原子半径最大的是Na;丁为氯元素,元素的最高正价为+7价;
(3)元素的金属性越强,其最高价氧化物对应水化物的碱性越强,Na比Al金属性强,则最高价氧化物对应水化物的碱性:甲>乙;氯元素的非金属性比硫元素强,HCl比H2S稳定,即简单气态氢化物的稳定性:丙<丁;
(4)Al(OH)3既能与强碱反应,又能与强酸反应,发生反应的离子方程式分别是;Al (OH)3+ OH-= AlO![]() +2 H2O、Al (OH)3+ 3H+= Al3++3 H2O;
+2 H2O、Al (OH)3+ 3H+= Al3++3 H2O;
(5)Cl2通入冷的消石灰中可制得漂白粉,发生反应的化学方程式为2 Cl2+ 2 Ca(OH)2= CaCl2+ Ca(ClO)2+ 2H2O。


科目:高中化学 来源: 题型:
【题目】己知断裂1molH2(g)中的H—H键需吸收436kJ 能量,断裂1molO2中的共价键需吸收496kJ能量,且氢气在氧气中燃烧的能量变化如图所示。下列说法正确的是
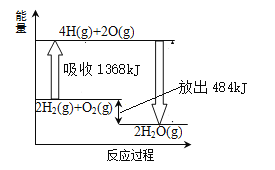
A.H2O(g)=H2(g)+1/2O2(l) △H=+242kJ/mol
B.H2(g)+1/2O2(g)= H2O(l) △H<-242kJ/mol
C.形成1molH2O(g)中的化学键需吸收926kJ
D.2H2(g)+ O2 (g)= 2H2O (g) △H=-1852kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A是石油裂解气的主要产物之一,其产量常用于衡量一个国家石油化工发展水平的标志。下列是有机物 A~G之间的转化关系:
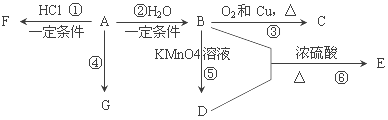
请回答下列问题:
(1)A的官能团的名称是_________;C的结构简式是_____;
(2)B是一种具有特殊香味的液体,由A→B的反应方程式为_____,该反应类型是_____;
(3)G 是一种高分子化合物,其结构简式是_____;
(4)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射物质F(沸点12.27°C)进行应急处理。写出由A制F的化学反应方程式_____。
(5)D的结构简式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。
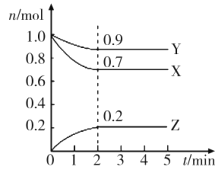
根据图中数据填空:
(1)该反应的化学方程式为___。
(2)若X、Y、Z均为气体,2min时反应达到平衡,此时体系内压强与开始时的压强之比为___。
(3)若X、Y、Z均为气体,则达平衡时,容器内混合气体的平均相对分子质量比起始投料时___ (填“增大”“减小”或“相等”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G(盐酸阿扎司琼,Azasetronhydrochchoride)主要用于治疗和预防肿瘤术后以及化疗引起的恶心、呕吐。G的合成路线设计如图:
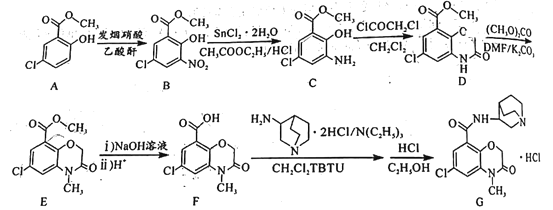
回答下列问题:
(1)A中含有的官能团名称为__。
(2)A生成B、B生成C的反应类型分别为__、__,D的分子式为__。
(3)上述合成路线中,互为同分异构体的物质是__(填字母序号)。
(4)E生成F的第一步反应的化学方程式为__。
(5)X为A的同分异构体,写出两种满足以下条件的X的结构简式__。
①含有苯环,且苯环上有4个取代基;
②有四种不同化学环境的氢,个数比为2:2:2:1;
③能发生银镜反应,还能与氯化铁溶液发生显色反应。
(6)以![]() 和(CH3O)2CO为原料制备
和(CH3O)2CO为原料制备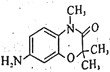 ,写出合成路线:__(无机试剂和有机溶剂任选)。
,写出合成路线:__(无机试剂和有机溶剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TPE(四苯基乙烯)及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛。TPE的结构简式如下图,下列关于TPE的说法正确的是( )
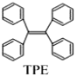
A.TPE的分子式为C26H22
B.TPE能发生加成反应,氧化反应,不能发生取代反应
C.TPE与化合物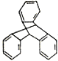 互为同分异构体
互为同分异构体
D.TPE的一氯代物有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物说法正确的是( )
A.可用酸性高锰酸钾溶液鉴别乙醇、环己烯与溴苯
B.![]() 是由小分子CH2==CH—CH3 和CH2==CH2 发生加聚反应的产物
是由小分子CH2==CH—CH3 和CH2==CH2 发生加聚反应的产物
C.石油裂解和油脂皂化都是由高分子化合物生成小分子物质的过程
D.淀粉与纤维素互为同分异构体,二者水解的最终产物相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香料G的一种合成工艺如下图所示。
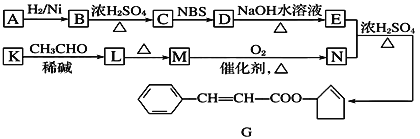
核磁共振氢谱显示A有两个峰,其强度之比为1∶1。
已知:![]()
![]()
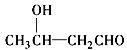
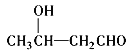
![]()
请回答下列问题:
(1)A的结构简式为________ ,G中官能团的名称为________。
(2)检验M已完全转化为N的实验操作是___________________。
(3)有学生建议,将M→N的转化用KMnO4(H+)代替O2,你认为是否合理______(填“是”或“否”)原因是________________________(若认为合理则不填此空)。
(4)写出下列转化的化学方程式,并标出反应类型:
K→L______________________________,反应类型________。
(5)F是M的同系物,比M多一个碳原子。满足下列条件的F的同分异构体有________种。(不考虑立体异构)
①能发生银镜反应 ②能与溴的四氯化碳溶液加成 ③苯环上只有2个对位取代基
(6)以丙烯和NBS试剂为原料制备甘油(丙三醇),请设计合成路线(其他无机原料任选) ___________________________。
请用以下方式表示:A![]() B
B![]() 目标产物
目标产物
查看答案和解析>>
科目:高中化学 来源: 题型:
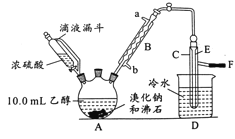
【题目】实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理为H2SO4(浓)+NaBr![]() NaHSO4+HBr↑、CH3CH2OH+HBr
NaHSO4+HBr↑、CH3CH2OH+HBr![]() CH3CH2Br+H2O。有关数据和实验装置如(反应需要加热,图中省去了加热装置):
CH3CH2Br+H2O。有关数据和实验装置如(反应需要加热,图中省去了加热装置):
乙醇 | 溴乙烷 | 溴 | |
状态 | 无色 液体 | 无色 液体 | 深红棕色 液体 |
密度/g·cm-3 | 0.79 | 1.44 | 3.1 |
沸点/℃ | 78.5 | 38.4 | 59 |
(1)A中放入沸石的作用是__,B中进水口为__口(填“a”或“b”)。
(2)实验中用滴液漏斗代替分液漏斗的优点为__。
(3)氢溴酸与浓硫酸混合加热发生氧化还原反应的化学方程式__。
(4)给A加热的目的是__,F接橡皮管导入稀NaOH溶液,其目的是吸收__和溴蒸气,防止__。
(5)C中的导管E的末端须在水面以下,其原因是__。
(6)将C中的镏出液转入锥形并瓶中,连振荡边逐滴滴入浓H2SO41~2mL以除去水、乙醇等杂质,使溶液分层后用分液漏斗分去硫酸层;将经硫酸处理后的溴乙烷转入蒸镏烧瓶,水浴加热蒸馏,收集到35~40℃的馏分约10.0g。
①分液漏斗在使用前必须__;
②从乙醇的角度考虑,本实验所得溴乙烷的产率是__(精确到0.1%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com