
【题目】香料G的一种合成工艺如下图所示。
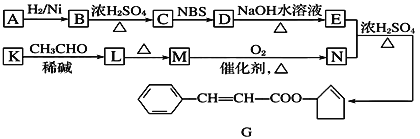
核磁共振氢谱显示A有两个峰,其强度之比为1∶1。
已知:![]()
![]()
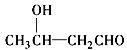
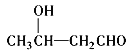
![]()
请回答下列问题:
(1)A的结构简式为________ ,G中官能团的名称为________。
(2)检验M已完全转化为N的实验操作是___________________。
(3)有学生建议,将M→N的转化用KMnO4(H+)代替O2,你认为是否合理______(填“是”或“否”)原因是________________________(若认为合理则不填此空)。
(4)写出下列转化的化学方程式,并标出反应类型:
K→L______________________________,反应类型________。
(5)F是M的同系物,比M多一个碳原子。满足下列条件的F的同分异构体有________种。(不考虑立体异构)
①能发生银镜反应 ②能与溴的四氯化碳溶液加成 ③苯环上只有2个对位取代基
(6)以丙烯和NBS试剂为原料制备甘油(丙三醇),请设计合成路线(其他无机原料任选) ___________________________。
请用以下方式表示:A![]() B
B![]() 目标产物
目标产物
【答案】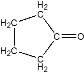 碳碳双键、酯基 取少量M于试管中,滴加稀NaOH至溶液呈碱性,再加新制的Cu(OH)2加热,若没有砖红色沉淀产生,说明M已完全转化为N(其他合理答案均可) 否 KMnO4(H+)在氧化醛基的同时,还可以氧化碳碳双键
碳碳双键、酯基 取少量M于试管中,滴加稀NaOH至溶液呈碱性,再加新制的Cu(OH)2加热,若没有砖红色沉淀产生,说明M已完全转化为N(其他合理答案均可) 否 KMnO4(H+)在氧化醛基的同时,还可以氧化碳碳双键 ![]()
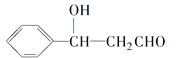 加成反应 6
加成反应 6 ![]()

【解析】
结合已知信息分析,C的结构中一定含有碳碳双键,D的结构中一定含有溴原子;C是通过A加氢生成B后,B在浓硫酸的条件下反应生成的,所以推测B为醇,B生成C即醇的消去反应,那么A中含有羰基,A加氢后生成羟基;D的结构中由于含有溴原子,所以推测,D生成E的反应即卤素原子的水解反应,E中则含有羟基;E与N是在浓硫酸加热的条件下反应生成的G,G的结构中又含有酯基,所以暂时推测E与N的反应为酯化反应;那么由G的结构逆推N即为![]() ;结合已知信息,K的结构中含有醛基,L则含有羟基和醛基,M则含有碳碳双键和醛基;再根据N的结构逆推,可得M为
;结合已知信息,K的结构中含有醛基,L则含有羟基和醛基,M则含有碳碳双键和醛基;再根据N的结构逆推,可得M为![]() ,L为
,L为![]() ,K即为苯甲醛
,K即为苯甲醛![]() 。再由G的结构逆推E为
。再由G的结构逆推E为![]() ,那么D为
,那么D为![]() ,C为
,C为![]() ,B为
,B为![]() ,则A即为
,则A即为![]() ,A的结构也符合分子中有两种个数相同的等效氢。据此解答。
,A的结构也符合分子中有两种个数相同的等效氢。据此解答。
(1)通过分析可知,A即为环戊酮,结构简式为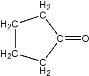 ;由G的结构可知,含有的官能团名称为:碳碳双键和酯基;
;由G的结构可知,含有的官能团名称为:碳碳双键和酯基;
(2)通过分析可知,M为![]() ,G为
,G为![]() ,所以需要检验是否还有醛基即可,因此,首先加NaOH将溶液调至碱性,再加新制氢氧化铜悬浊液,加热观察是否有砖红色沉淀出现即可;
,所以需要检验是否还有醛基即可,因此,首先加NaOH将溶液调至碱性,再加新制氢氧化铜悬浊液,加热观察是否有砖红色沉淀出现即可;
(3)通过分析可知,M为![]() ,M的结构中含有的碳碳双键也可以被酸性高锰酸钾氧化,所以不能用酸性高锰酸钾溶液代替氧气;
,M的结构中含有的碳碳双键也可以被酸性高锰酸钾氧化,所以不能用酸性高锰酸钾溶液代替氧气;
(4)通过分析可知,K为![]() ,L为
,L为![]() ,K与乙醛生成L的反应即已知信息中的第二个反应,所以方程式为
,K与乙醛生成L的反应即已知信息中的第二个反应,所以方程式为![]() +CH3CHO
+CH3CHO![]()
![]() ,该反应为加成反应;
,该反应为加成反应;
(5)通过分析可知,M为![]() ,由题意可知,F为M的同系物且比M多1个碳,苯环上也只有2个对位的取代基,所以:若两个取代基一个是-CH3,另一个则可能是
,由题意可知,F为M的同系物且比M多1个碳,苯环上也只有2个对位的取代基,所以:若两个取代基一个是-CH3,另一个则可能是![]() 或
或![]() ;若两个取代基一个是-CHO,另一个则可能是
;若两个取代基一个是-CHO,另一个则可能是![]() 或
或![]() 或
或![]() ;若两个取代基一个是-CH2-CHO,则另一个是-CH=CH2;综上所述,共计6种结构;
;若两个取代基一个是-CH2-CHO,则另一个是-CH=CH2;综上所述,共计6种结构;
(6)由已知信息可知,丙烯在经过NBS处理后,会在碳碳双键碳的邻碳上引入Br原子,再继续与溴单质加成后,可得到每个碳原子上均有一个溴原子的结构,再利用卤代烃的水解反应即可,因此合成路线为:![]()
 。
。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】分子组成为C9H12苯的同系物,已知苯环上只有一个取代基,下列说法中正确
A.该有机物不能发生加成反应,但能发生取代反应
B.该有机物不能使酸性高锰酸钾溶液褪色,但能使溴水褪色
C.该有机物分子中的所有原子可能在同一平面上
D.该有机物的一溴代物最多有6种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据表格中提供的甲、乙、丙、丁四种元素的相关信息完成下列问题:
元素 | 甲 | 乙 | 丙 | 丁 |
原子序数 | 11 | ③ | ||
元素符号 | ② | S | ||
原子结构示意图 | ① |
| ||
元素周期表中的位置 | 第三周期 ⅢA族 | ④ |
(1)填写表格中各序号所对应的空白:①_________________②__________________
③_________________④_________________。
(2)甲、乙、丙、丁四种元素中,原子半径最大的是_______(填元素符号),丁元素的最高正价为____价(填化合价)。
(3)最高价氧化物对应水化物的碱性:甲_______________乙(填“>”或“<”),简单气态氢化物的稳定性:丙_______________丁(填“>”或“<”)。
(4)元素乙的最高价氧化物对应水化物,既能与元素甲的最高价氧化物对应水化物反应,又能中和过多的胃酸。
请分别写出上述反应的离子方程式:_____________;______________。
(5)丁单质通入冷的消石灰中可制得漂白粉,写出该反应的化学方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铍铜是力学、化学综合性能良好的合金,广泛应用于制造高级弹性元件。以下是从某废旧铵铜元件(含BeO25%、CuS71%、少量FeS和SiO2)中回收铍和铜两种金属的流程。
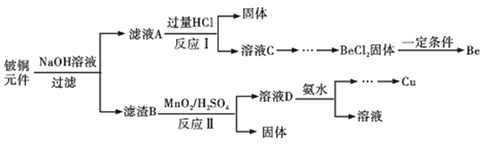
已知:
Ⅰ.铍、铝元素处于周期表中的对角线位置,化学性质相似
Ⅱ.常温下:Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=2.1×10-13
(1)滤渣B的主要成分为______(填化学式);
(2)写出反应Ⅰ中含铍化合物与过量盐酸反应的化学方程式______;
(3)MnO2能将金属硫化物中的硫元素氧化为单质硫,写出反应Ⅱ中CuS发生反应的离子方程式______,若用浓HNO3溶解金属硫化物缺点是______(任写一条);
(4)从BeCl2溶液中得到BeCl2固体的操作是______。
(5)溶液D中含c(Cu2+)=2.2molL-1、c(Fe3+)=0.008molL-1、c(Mn2+)=0.01molL-1,逐滴加入稀氨水调节pH可依次分离首先沉淀的是______(填离子符号),为使铜离子开始沉淀,常温下应调节溶液的pH大于______;
(6)取铍铜元件1000g,最终获得Be的质量为72g,则Be的产率是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应aA(g)+bB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应是________热反应,且a+b________p(填“>”“<”或“=”)。
(2)减压时,A的质量分数________(填“增大”“减小”或“不变”,下同),正反应速率________,逆反应速率________。
(3)若加入B(体积不变),则A的转化率________,B的转化率________。
(4)若升高温度,则平衡时,B、C的浓度之比![]() 将________。
将________。
(5)若加入催化剂,平衡时气体混合物的总物质的量________。
(6)若B是有色物质,A、C均为无色物质,则加入A(体积不变)时混合物的颜色________,加入C(体积不变)时混合物的颜色________,而维持容器内气体的压强不变,充入氖气时,混合物的颜色_______(填“变浅”“变深”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.1mol铵根离子中含有的电子数为9NA
B.38.5gCCl4中含有的共用电子对数为NA
C.16gO3单质中含有的分子个数为NA
D.通常状况下,11.2 LCl2通入足量的NaOH溶液中,转移的电子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在试管A中加入3mL乙醇,然后边振荡试管边慢慢加入2mL浓硫酸和2mL乙酸,按下图所示连接好装置进行实验,以制取乙酸乙酯。
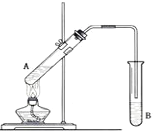
(1)试管B中盛放的溶液是_____________,其作用是:_____________
(2)反应的化学方程式是____________
(3)分离产物用的仪器是___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物![]() (X)、
(X)、![]() (Y)、
(Y)、![]() (Z)的分子式均为C5H6。下列说法正确的是( )
(Z)的分子式均为C5H6。下列说法正确的是( )
A.X、Y、Z均能使酸性高锰酸钾溶液褪色
B.Z的同分异构体只有X和Y两种
C.Z的二氯代物只有两种(不考虑立体异构)
D.Y分子中所有碳原子均处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:反应Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2H2(g)![]() CH3OH(g) △H3=-90.77kJ·mol-1
CH3OH(g) △H3=-90.77kJ·mol-1
回答下列问题:
(1)反应Ⅱ的△H2=______________。
(2)反应Ⅲ能够自发进行的条件是__________ (填“较低温度”、“ 较高温度”或“任何温度”)
(3)恒温,恒容密闭容器中,对于反应Ⅰ,下列说法中能说明该反应达到化学平衡状态的是________。
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1
D.甲醇的百分含量不再变化
(4)对于反应Ⅰ,不同温度对CO2的转化率及催化剂的效率影响如图所示,下列有关说法不正确的是__________。

A.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1
B.温度低于250℃时,随温度升高甲醇的产率增大
C.M点时平衡常数比N点时平衡常数大
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(5)若在1L密闭容器中充入3molH2和1molCO2发生反应Ⅰ,250℃时反应的平衡常数K=______;若要进一步提高甲醇体积分数。可采取的措施有_________________。
(6)下图是电解Na2CO3溶液的装置图。

阴极的电极反应式为________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com