
【题目】某温度下,反应N2O4(g) ![]() 2NO2(g)(△H>0)在密闭容器中达到平衡.下列说法不正确的是
2NO2(g)(△H>0)在密闭容器中达到平衡.下列说法不正确的是
A. 加压时(体积变小),平衡向逆反应方向移动,将使正反应速率增大
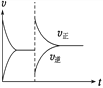
B. 某时刻改变条件速率时间如右图,改变的条件是恒容时增大N2O4的浓度
C. 保持体积不变,加入少许N2O4,平衡向正反应方向移动,再达平衡时颜色变深
D. 保持压强不变,加入少许N2O4,混合气体的相对平均分子质量不变
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】X、Y和Z均为短周期主族元素,原子序数依次增大,X的单质为密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最外层电子数相同。回答下列问题:
(1)Y元素的名称为________。Z的离子结构示意图为_________。
元素Y的简单离子和元素Z的简单离子,半径较大的是________(写出离子符号)。
(2)X和Y组成的化合物中,既含极性共价键又含非极性共价键的是______(写化学式),该物质核外电子总数为______。
(3)化合物Z2Y2的电子式为___________。
(4)X的单质与Y的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正极电极反应式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如表:下列说法正确的是( )
2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如表:下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A. 该温度下此反应的平衡常数K=1.44
B. 其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
D. 0~2min的平均速率ν(Z)=2.0×10﹣3molL﹣1min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草纲目拾遗》中在药物名“鼻冲水”条目下写到:贮以玻璃瓶,紧塞其口,勿使泄气,则药力不减.气甚辛烈,触人脑,非有病不可嗅;在“刀创水”条目下写到:治金创,以此水涂伤口,即敛合如故.这里所说的“鼻冲水”、“刀创水”分别指的是( )
A.氢氟酸、食盐水
B.氨水、碘酒
C.石灰水、硝酸
D.稀硫酸、食醋
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅单质及其化合物应用范围很广。
(1)制备硅半导体材料必须先得到高纯硅,工业上可以按如下步骤制备高纯硅。
Ⅰ.高温下用碳还原二氧化硅制得粗硅;
Ⅱ.粗硅与干燥的氯气在450~500 ℃条件下反应制得SiCl4;
Ⅲ.SiCl4液体经精馏提纯后与过量H2在1 100~1 200 ℃条件下反应制得高纯硅。
已知SiCl4沸点为57.6 ℃,能与H2O强烈反应。
请回答下列问题:
①第Ⅲ步反应的化学方程式为____________________________________。
②整个制备纯硅的过程中必须严格控制在无水无氧的条件下。SiCl4在潮湿的空气中因水解而产生白色烟雾,其生成物是_______;H2还原SiCl4过程中若混入O2,可能引起的后果是________________________________________。
(2)二氧化硅被大量用于生产玻璃。工业上用SiO2、Na2CO3和CaCO3共283 kg在高温下完全反应时放出CO2 44 kg,生产出的玻璃可用化学式Na2SiO3·CaSiO3·xSiO2表示,则其中x=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们对原子结构的认识有一个不断深入的过程,下列先后顺序中符合史实的是
①道尔顿提出的原子论
②卢瑟福的原子结构行星模型
③波尔提出的原子力学模型
④汤姆生提出的葡萄干面包原子模型
A.①②④③ B.①④②③ C.②①④③ D.①③②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
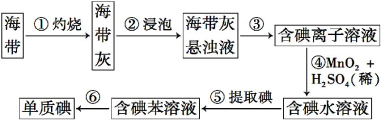
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是_________(从下列仪器中选出所需的仪器,用标号字母填写空白处)。
A.烧杯
B.坩埚
C.表面皿
D.泥三角
E.酒精灯
F.干燥器
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘的苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 。
(3)步骤④反应的离子方程式是 。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是 。
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期原子序数依次增大的元素A、B、C、D、E中,A的基态原子核外3个能级上有电子,且每个能级上的电子数相等,B原子核外电子有7种不同的运动状态,C元素原子核外的M层中只有2对成对电子,D+与C2-的电子数相等,E元素位于元素周期表的ds区,且基态原子价电层电子均已成对。
回答下列问题:
(1)E2+的价层电子排布图为________________。
(2)五种元素中第一电离能最小的是________(填元素符号),CAB-离子中,A原子的杂化方式是________。
(3)AB-、D+和E2+三种离子组成的化学物质D2E(AB)4,其中化学键的类型有________________,该化合物中存在一个复杂离子,该离子的化学式为________,配位体是________。
(4)C和E两种元素组成的一种化合物的晶胞如图所示。

①该化合物的化学式为________,E的配位数为________,C采取________(填“简单立方”、“体心立方”、“六方最密”或“面心立方最密”)堆积;
②列式表示该晶体的密度:________g·cm-3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com