
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:

回答下列问题:
(1)NaClO2中Cl的化合价为_______。
(2)写出“反应”步骤中生成ClO2的化学方程式_______。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为________、________。“电解”中阴极反应的主要产物是______。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2。此吸收反应中,氧化剂与还原剂的物质的量之比为________,该反应中氧化产物是_________。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为____。(计算结果保留两位小数)
【答案】(1)+3价;(2)2NaClO3+SO2+H2SO4=ClO2+2NaHSO4;
(3)NaOH溶液 ;Na2CO3溶液 ;ClO2-(或NaClO2);
(4)2:1; O2;
(5)1.57g。
【解析】
试题分析:(1)在NaClO2中Na为+1价,O为-2价,根据正负化合价的代数和为0,可得Cl的化合价为+3价。(2)NaClO3和SO2在H2SO4酸化条件下生成ClO2,其中NaClO2是氧化剂,还原产物为NaCl,根据电子守恒和原子守恒,此反应的化学方程式为2NaClO3+SO2+H2SO4=2NaHSO4+ClO2↑。(3)食盐溶液中混有Mg2+和Ca2+,可利用过量NaOH溶液除去Mg2+,利用过量Na2CO3溶液除去Ca2+,向NaCl溶液加入ClO2,进行电解,阳极发生反应2Cl--2e-=Cl2↑,反应产生Cl2, 阴极发生反应产生NaClO2,可见“电解”中阴极反应的主要产物是NaClO2;(4)根据图示可知:利用含有过氧化氢的NaOH溶液ClO2气体,产物为NaClO3,则此吸收反应中,氧化剂为ClO2,还原产物为NaClO2,还原剂是H2O2,氧化产物是O2,每1mol的H2O2转移2mol电子,反应方程式是:2NaOH+2ClO2+H2O2=2NaClO2+O2+2H2O,可知氧化剂和还原剂的物质的量之比为2:1,该反应中氧化产物O2。(5)每1克NaClO2的物质的量为n(NaClO2)=1g÷90.5g/mol=![]() mol,其获得电子的物质的量是n(e-)=
mol,其获得电子的物质的量是n(e-)=![]() mol×4=4/90.5mol,1molCl2获得电子的物质的量是2mol,根据电子转移数目相等,可知其相对于氯气的物质的量为n=
mol×4=4/90.5mol,1molCl2获得电子的物质的量是2mol,根据电子转移数目相等,可知其相对于氯气的物质的量为n=![]() mol×4÷2=
mol×4÷2=![]() mol,则氯气的质量为
mol,则氯气的质量为![]() mol×71g/mol=1. 57g。
mol×71g/mol=1. 57g。


科目:高中化学 来源: 题型:
【题目】硼及其化合物在工业上有许多用途。工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5·H2O和Fe3O4。
(1)铁元素位于元素周期表中的第 族,在水溶液中常以Fe2+、Fe3+的形式存在,其中 更稳定。
(2)以硼酸为原料可制得NaBH4 ,B原子的杂化方式为 。
(3)工业上冶炼铝不用氯化铝,因为氯化铝易升华,其双聚物Al2Cl6结构如图所示。1mol该分子中含 个配位键,该分子 (填“是”或“否”)平面型分子。
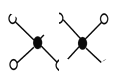
(4)Al单质为面心立方晶体,其晶胞的边长a=0.405nm,列式表示Al单质的密度:____g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

(1)该浓盐酸中HCl的物质的量浓度为 mol·L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 。
A.溶液中HCl的物质的量 | B.溶液的浓度 |
C.溶液中Cl-的数目 | D.溶液的密度 |
(3)某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol·L-1的稀盐酸。
①该学生需要量取 mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响? (填“偏大”“偏小”或“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面: 。
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水: 。
(4)硅单质是一种重要的非金属单质,其用途是 (举一例)
(5)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为 (填代号)。

(6)某H2中含有2.40 molCO2,该混合气体通入2.00 L NaOH溶液中,CO2被完全吸收。如果NaOH完全反应,该NaOH溶液的浓度为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将锌,铜通过导线相连,置于稀硫酸中构成原电池,完成下填空

(1)锌为:________极(填“正”或“负”)电极反应式为:_______________,
(2)反应过程中电流的方向为:____________
A 由铜流向锌 B 由锌流向铜
(3)若有锌片质量减少了0.65g,则转移了____________mol电子发生转移,铜片上产生气体的体积(标况下)为:________________L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.1 mol葡萄糖能水解生成2 mol CH3CH2OH和2 mol CO2
B.在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会因盐析产生沉淀
C.利用油脂在碱性条件下的水解,可以制甘油和肥皂
D.植物油和矿物油都不能使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E都是元素周期表中的前20号元素,原子序数依次增大,B、C、D同周期,A、D原子中某p能级均排有5个电子,E和其他元素既不在同周期也不在同主族,B、C、D的最高价氧化物的水化物两两混合均能发生反应生成盐和水。
根据以上信息,回答下列问题。
(1)A和D的氢化物中,沸点较低的是________(填化学式);该物质固态时属于________晶体;A和D的电负性较大的是________(填元素符号);B和C的第一电离能较小的是________(填元素符号);
A和B的离子中,半径较小的是________(填离子符号);构成C单质晶体的微粒以________键相结合。
(2)写出B、C的最高价氧化物的水化物相互反应的离子方程式:________________________。
(3)A和E可组成离子化合物,其晶胞结构如图所示:
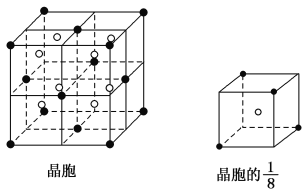
阳离子(用“●”表示)位于大立方体的顶点或面心;阴离子(用“○”表示)均位于小立方体的中心。与一个“○”距离最近的“●”有________个,与一个“●”距离最近的“●”有________个,该化合物的化学式是________。
(4)已知晶胞的![]() 的体积为2.0×10-23cm3,求A和E组成的离子化合物的密度,请列式并计算,结果保留一位小数。
的体积为2.0×10-23cm3,求A和E组成的离子化合物的密度,请列式并计算,结果保留一位小数。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,吸收的热量用于克服分子间作用力的是( )
A.加热氯化钠晶体使之熔化
B.加热碘化氢气体使之分解
C.加热硅晶体使之熔化
D.液氨受热蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:2A+3B![]() 2C。开始时C的浓度为amol·L-1,2min后C的浓度变为2amol·L-1,A和B的物质的量浓度均变为原来的1/2,则下列说法中不正确的是( )
2C。开始时C的浓度为amol·L-1,2min后C的浓度变为2amol·L-1,A和B的物质的量浓度均变为原来的1/2,则下列说法中不正确的是( )
A.用B表示的反应速率是0.75a mol/(L·min)
B.反应开始时,c(B)=3amol·L-1
C.反应2min后,c(A)=0.5amol·L-1
D.反应2min后,c(B)=1.5amol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂一空气电池是高能量密度的新型电池,结构如图所示。下列说法正确的是( )

A.固体电解质只有Li+可通过
B.电池反应为![]()
C.充电时,水性电解液的pH将升高
D.放电时,若外电路有0. 1mol e -通过时,理论上将消耗1.12 LO2(标准状况)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com