
【题目】某兴趣小组用下图装置研究原电池的工作原理。

(1)甲中K断开时,装置中发生反应的离子方程式为_____________;K闭合时,Cu棒上的现象为__________,它为原电池的___(填“正”或“负”)极,电极反应式为_______,外电路电流的方向由___到______(填“Cu”或“Zn”)。
(2)乙图为氢氧燃料电池构造示意图,其中通入氢气的一极为电池的____填“正”或“负”)极,发生____(填“氧化”或“还原”)反应。
(3)某同学欲把反应Fe+2FeCl3=3FeCl2设计成原电池,请写出负极的电极反应式: _________________。
【答案】Zn+2H+=Zn2++H2↑ 有气泡产生 正 2H++2e=H2↑ Cu Zn 负 氧化 Fe-2e=Fe2+
【解析】
由装置分析可知,甲中K断开时,未构成原电池,Zn直接与稀硫酸反应生成氢气;K闭合时,构成原电池,Zn为负极;乙为氢氧燃料电池,燃料电池中通入氧气的极为正极,发生还原反应,据此分解结合原电池知识解答问题。
(1)甲中K断开时,未构成原电池,Zn直接与稀硫酸反应生成氢气,发生反应的离子方程式为Zn+2H+=Zn2++H2↑;K闭合时,构成原电池,Zn为负极,Zn失去电子发生氧化反应,电极反应式为Zn-2e-=Zn2+,则Cu为正极,电极表面H+得到电子发生还原反应,电极反应式为2H++2e=H2↑,可观察到Cu棒上产生气泡,外电路电流方向由正极到负极,即由Cu到Zn,故答案为:Zn+2H+=Zn2++H2↑;有气泡产生;正;2H++2e=H2↑;Cu;Zn;
(2)燃料电池中通入氧气的极为正极,发生还原反应,则通入氢气的一极为电池的负极,发生氧化反应,故答案为:负;氧化;
(3)反应Fe+2FeCl3=3FeCl2中Fe发生氧化反应,应为原电池的负极材料,电解质溶液应选择FeCl3溶液,其中负极的电极反应式为Fe-2e-=Fe2+,故答案为:Fe-2e-=Fe2+。


科目:高中化学 来源: 题型:
【题目】某学习小组按如下实验过程证明了海带中存在的碘元素:
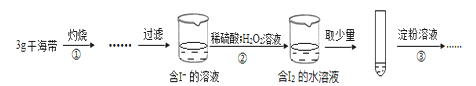
下列说法不正确的是
A.步骤①需要将干海带放入坩埚中灼烧
B.步骤②反应的离子方程式为:2I- +2H++H2O2=I2+2H2O
C.步骤③操作后,观察到试管中溶液变为蓝色,可以说明海带中含有碘元素
D.若步骤②仅滴加稀硫酸后放置一会儿,步骤③操作后,试管中溶液不变成蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中还原剂是___________________(填化学式),被2 mol FeSO4还原的过氧化钠为_________mol
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:__________________________
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是____________,被氧化的离子的物质的量分别是_____________________________________________
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+被氧化时,c为_____________(用含a、b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是研究铁被海水腐蚀的实验装置。图2中M是某种与铁片紧贴的金属,下列说法正确的是

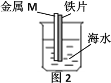
A.图1铁片靠近烧杯底部的部分,腐蚀更严重
B.若M是锌片,可保护铁
C.若M是铜片,可保护铁
D.M是铜或是锌都不能保护铁,是因没有构成原电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生下列反应aA(g)![]() cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
A. 平衡向正反应方向移动B. a<c+d
C. D的体积分数变大D. A的转化率变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积均为0.5L的恒容密闭容器中发生反应:CO(g)+Cl2(g)COCl2(g),其中容器Ⅰ中5min时到达平衡。
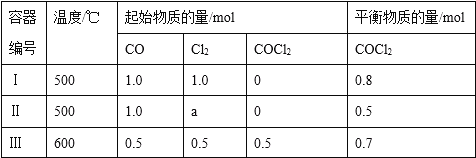
下列说法中正确的是( )
A. 容器Ⅰ中前5min的平均反应速率v(CO)=0.16molL﹣1min﹣1
B. 该反应正反应为吸热反应
C. 容器Ⅱ中起始时Cl2的物质的量为0.55mol
D. 若起始时向容器Ⅰ加入CO0.8mol、Cl20.8mol,达到平衡时CO转化率大于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法不正确的是
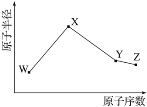
A.对应简单离子半径:X<W
B.对应简单气态氢化物的稳定性:Y<Z
C.化合物XZW既含离子键也含共价键
D.Y的氧化物能与Z或X的最高价氧化物对应的水化物反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将铁钉放入纯水中,一段时间后,铁钉表面有铁锈生成,下列说法正确的是
![]()
A.铁钉与水面交接处最易腐蚀
B.铁钉发生吸氧腐蚀,铁做阴极
C.铁发生的反应是:Fe-3e→Fe3+
D.水上和水下部分的铁钉不发生电化腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟代硼酸钾(KBe2BO3F2)是激光器的核心材料,我国化学家在此领域的研究走在了世界的最前列。回答下列问题:
(1)氟代硼酸钾中各元素原子的第一电离能大小顺序是F>O> ___。基态K+电子占据最高能级的电子云轮廓图为____形。
(2) NaBH4是有机合成中常用的还原剂,其中的阴离子空间构型是____,中心原子的杂化形式为____。NaBH4中存在____(填标号)。
a. 离子键 b. 氢键 c. σ键 d. π键
(3) BeC12中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的BeCl2的结构式为 ___,其中Be的配位数为_____。
(4)第三周期元素氟化物的熔点如下表:
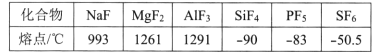
解释表中氟化物熔点变化的原因:____。
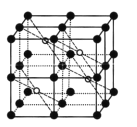
(5) CaF2的一种晶胞如图所示。Ca2+占据F-形成的空隙,其空隙率是____。若r(F-)=x pm,r(Ca2+) =y pm,设阿伏加德罗常数的值为NA,则CaF2的密度ρ=_____ g.cm-3(列出计算表达式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com