
����Ŀ���������(K2FeO4)��һ�����͡���Ч�������ɫˮ����������Cl2��O2��ClO2��KMnO4�����Ը�ǿ��������Ⱦ����ҵ�������Ƶø������ƣ�Ȼ���ڵ����£������������Һ�м���KOH�����ͣ�ʹ�������������
(1)�ɷ��Ʊ��������Ƶ���Ҫ��ӦΪ��2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2�����÷�Ӧ�л�ԭ����___________________(�ѧʽ)����2 mol FeSO4��ԭ�Ĺ�������Ϊ_________mol
(2)ʪ���Ʊ��������(K2FeO4)�ķ�Ӧ��ϵ������������Fe(OH)3��ClO����OH����FeO42-��Cl����H2O��д�������������Ƹ�����ص����ӷ�Ӧ����ʽ��__________________________
����֪��2Fe3����2I��=2Fe2����I2��2Fe2����Br2=2Fe3����2Br����
(1)����1 mol FeI2��2 mol FeBr2����Һ��ͨ��2 mol Cl2����ʱ��������������____________�������������ӵ����ʵ����ֱ���_____________________________________________
(2)����a mol FeI2��b mol FeBr2����Һ��ͨ��c mol Cl2����I����Fe2��������ʱ��cΪ_____________(�ú�a��b�Ĵ���ʽ��ʾ)��
���𰸡�FeSO4 Na2O2 4 2Fe(OH)3 + 3ClO- + 4OH- = 2FeO42- + 3Cl- + 5H2O I-��Fe2+ n(I-)=2mol n(Fe2+)=2mol c=(3a+b)/2
��������
��1���÷�Ӧ�еõ��ӵ������ǹ������ƣ�ʧ���ӵ������ǹ������ƺ����������������������ǹ������ƣ���ԭ���ǹ������ƺ�����������2 mol FeSO4ʧȥ����8mol��1mol Na2O2����ԭ�õ�����Ϊ2mol���ʱ�2 mol FeSO4��ԭ�Ĺ�������Ϊ![]() ��
��
��2�������������������������Ƿ�Ӧ����ݸ�����غ�������������Ԫ�ػ��ϼ۵ı仯֪���������ǻ�ԭ�������������õ��ӷ�Ӧ��Ԫ�صĻ��ϼ۽��ͣ��������������л��ϼ۱仯����һ��Ԫ�����ȣ��Ҵ��������������Ӧ���������������������ӷ���ʽΪ2Fe(OH)3��3ClO����4OH��= 2FeO42����3Cl����5H2O��
��1����������ԭ��Ӧ�л�ԭ���Ļ�ԭ��ǿ�ڻ�ԭ������Ի�ԭ��ǿ��˳����I����Fe2����Br���������������������ĵ���I����Ȼ����Fe2���������Br�������ݵ��ӵĵ�ʧ�غ��֪��2molCl2������2molI����2molFe2����
��2�����ݵ��ӵĵ�ʧ�غ��֪��2c��2a����a��b����2b����c��![]() ��
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����Ƶ�˵���д������
A. ��������ǿ�Ļ�ԭ��
B. �ƿ��Դ�����ͭ��Һ�л�ԭ��ͭ����
C. ����������ȼ�ղ��������İ���
D. ��Ԫ������Ȼ���ж����Ի���̬����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����þ������þ��������ɰ����(Na2B4O7��10H2O)ʱ�ķ���������Ҫ�ɷ���MgO,������Na2B4O7��CaO��Fe2O3��FeO��MnO��SiO2�����ʡ�����þ��Ϊԭ����ȡMgSO4��7H2O�Ĺ����������£�
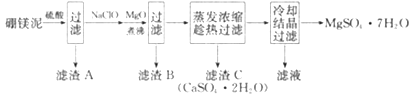
�ش��������⣺
(1)Na2B4O7��10H2O��B�Ļ��ϼ�Ϊ_______��Na2B4O7���Ʊ�ǿ��ԭ��NaBH4,д��NaBH4�ĵ���ʽ��_______��
(2)����A�г�����H3BO3�⡣������_______����������ʱNa2B4O7������Ӧ�Ļ�ѧ����ʽΪ_______��
(3)����B�к��в�����ϡ����,������ʱ������Ũ����ĺ�ɫ���壬д�����ɺ�ɫ��������ӷ���ʽ��_______;����MgO��Ŀ����_______��
(4)����������,�����ϵ��NaBO2��ҺҲ���Ƶ����⻯�ƣ���缫��ӦʽΪ_______������Ч�⺬����(����ÿ�˺��ԭ���Ļ�ԭ�����൱�ڶ��ٿ�H2�Ļ�ԭ����)�������������ԭ���Ļ�ԭ��������NaBH4����Ч�⺬��Ϊ_______(����2λ��Ч����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʮ�����ʣ���H2�� ���� ����CaO���� ����CO2 ����H2SO4 ����Ba(OH)2�������ڵ�KNO3�� �ఱˮ ����ϡ���� ����Al2(SO4)3
(1)����ʮ������������������֮��ɷ������ӷ�Ӧ��H++OH��=H2O�������ӷ�Ӧ��Ӧ�Ļ�ѧ����ʽΪ____________________________________��
(2)����ˮ�еĵ��뷽��ʽΪ___________________________��
(3)�������ڵ���ʵĹ���____________�֡�
(4)�������Ģ�ͨ�����Һ�з�Ӧ�����ӷ���ʽΪ___________________________��
(5)��ƽ�� �� �ᷢ����Ӧ�Ļ�ѧ����ʽ������˫���ŷ������÷�Ӧ�е���ת�Ƶķ������Ŀ____Al + ___HNO3 = ___Al(NO3)3 + ___NO�� +__ ______ ������8.1g Al������Ӧʱ��ת�Ƶ��ӵ����ʵ���Ϊ__________mol��HNO3����������������������ʵ���֮��Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ��Һ�п��ܺ���Mg2+��Ba2+��Cl-��HCO3-�е�һ�ֻ������ӡ�Ϊȷ����ɷ֣���������ʵ�飺
ʵ��1��ȡ10mL��ɫ��Һ���μ�����ϡ��������������
ʵ��2����ȡ10mL��ɫ��Һ������������Na2SO4��Һ���а�ɫ�������ɡ�
ʵ��3����ʵ��1�����Һ����ƿ�У�����ƿ����μ���NaOH��Һ���μӹ����в������������������NaOH��Һ������Ĺ�ϵ����ͼ��ʾ��

�ش��������⣺
(1)ԭ��Һ�в����ڵ�������__________�����ڵ�������________________��������ڵ������ӵķ�����________________________________________
(2)ʵ��3�У�ͼ����OA�η�Ӧ�����ӷ���ʽΪ____________________________��
(3)����ͼ�����ԭ��Һ��Mg2+�����ʵ���Ũ��_______��(д���������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪25��ʱ��RSO4(s)+CO32-(aq)![]() RCO3(s)+SO42-(aq)��ƽ�ⳣ��K=1.75��104��Ksp(RCO3)=2.80��10-9��������������ȷ����
RCO3(s)+SO42-(aq)��ƽ�ⳣ��K=1.75��104��Ksp(RCO3)=2.80��10-9��������������ȷ����
A. ��c(CO32-)=c(SO42-)�Ļ��Һ�еμ�RCl2��Һ����������RSO4����
B. ��Ũ�Ⱦ�Ϊ6��10-6mol/L��RCl2��Na2CO3��Һ�������Ϻ�ɵõ�RCO3����
C. 25��ʱ��RSO4��KspԼΪ4.9��10-5
D. ��ͬ�¶�����RCO3��ˮ�е�Ksp������Na2CO3��Һ�е�Ksp
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ֽ��ˮ�������������������Ź㷺��Ӧ����ͬʱ������ĭ������е��Լ���ij���������ú�������(�ɷ�ΪA12O3��SiO2������FeO��xFe2O3)�Ʊ�����������Ĺ�����������ͼ��ʾ���ش�������⡣
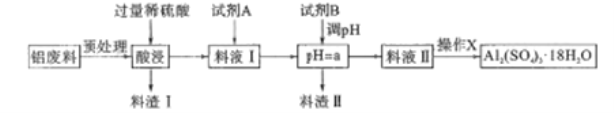
��֪�����������������pH���±���
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
��ʼ����ʱ | 3.6 | 6.3 | 2.3 |
��ȫ����ʱ | 4.9 | 8.3 | 3.2 |
��1������I�ijɷ���__������X��������__��ϴ�ӡ�����ȡ�
��2���Լ�B�����__��a�ķ�Χ��__���ɱ����������Ksp[Fe(OH)3]<_____(�������ȫʱ��������Ũ��С��1��10-5mol/L)��
��3���Լ�A��һ��Һ̬��ɫ����������Һ���з�Ӧ�����ӷ���ʽ_______
��4����ĭ��������������Ϊ�������㣬�ڲ��Dz�������������Ǹ�Ͳ������������ҺӦʢ����______�����У���ĭ���������һ���Լ���С�մ���Һ�������մ���Һ��ԭ����____.
��5�������һ�ּķ���������ȷ�����Ƶõľ�������Ƿ��������ϵ����[Al2(SO4)3��18H2O]��ͬ(д����Ҫ�������̼���):_________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ȳ��硶��Ʒ��ơ��������ҩ��������ҽ��������˷���룬���������F��������ע��Һ�������ڿ�����ʧ������ϳ�·�����£�
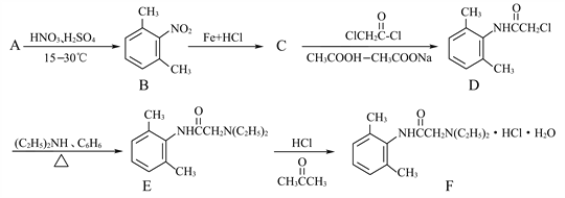
��1���A������______________________��
��2��C�Ľṹ��ʽΪ______________________.
��3��B�ж���ͬ���칹�壬��������������B��ͬ���칹�壨������B����������_______________�֣���д������һ�ֵĽṹ��ʽ_____________________��
�ٱ����Ϲ�������ȡ���� ����̼��������Һ��Ӧ�ɷų�CO2����
��4�������������ǻ���ϸ�������ͷ����������Ҷ�����ɳɷ֡����Լױ�Ϊԭ�ϣ��������й���Ϣ������������ºϳ�·�ߣ�____________
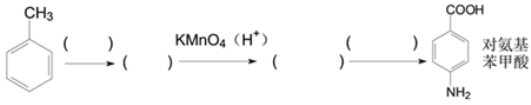
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����-Fenton��������ˮ�����л���Ⱦ�オ��ĸ���������,�䷴Ӧԭ����ͼ��ʾ�����е�������H2O2��Fe2+����Fenton��Ӧ:H2O2+Fe2+![]() Fe3++OH-+��OH,���ɵ��ǻ����ɻ�(��OH)�����������л���Ⱦ�����˵������ȷ����( )
Fe3++OH-+��OH,���ɵ��ǻ����ɻ�(��OH)�����������л���Ⱦ�����˵������ȷ����( )
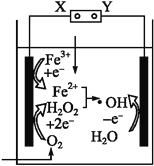
A. ��Դ��X��Ϊ����,Y��Ϊ����
B. �����ĵ缫��ӦʽΪFe2+-e-![]() Fe3+
Fe3+
C. ÿ����1molO2,���������������Ͽɲ���2mol��OH
D. �����ĵ缫��ӦʽΪH2O-e-![]() H++��OH
H++��OH
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com