
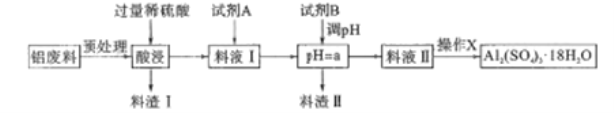
����Ŀ������������ֽ��ˮ�������������������Ź㷺��Ӧ����ͬʱ������ĭ������е��Լ���ij���������ú�������(�ɷ�ΪA12O3��SiO2������FeO��xFe2O3)�Ʊ�����������Ĺ�����������ͼ��ʾ���ش�������⡣
��֪�����������������pH���±���
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
��ʼ����ʱ | 3.6 | 6.3 | 2.3 |
��ȫ����ʱ | 4.9 | 8.3 | 3.2 |
��1������I�ijɷ���__������X��������__��ϴ�ӡ�����ȡ�
��2���Լ�B�����__��a�ķ�Χ��__���ɱ����������Ksp[Fe(OH)3]<_____(�������ȫʱ��������Ũ��С��1��10-5mol/L)��
��3���Լ�A��һ��Һ̬��ɫ����������Һ���з�Ӧ�����ӷ���ʽ_______
��4����ĭ��������������Ϊ�������㣬�ڲ��Dz�������������Ǹ�Ͳ������������ҺӦʢ����______�����У���ĭ���������һ���Լ���С�մ���Һ�������մ���Һ��ԭ����____.
��5�������һ�ּķ���������ȷ�����Ƶõľ�������Ƿ��������ϵ����[Al2(SO4)3��18H2O]��ͬ(д����Ҫ�������̼���):_________________
���𰸡� SiO2 ����Ũ������ȴ�ᾧ������ Al2O3��Al(OH)3 3.6>a![]() 3.2 1��10-37.4 2Fe2++2H++H2O2=2Fe3++2H2O ���� ���ĵ�����������ʱ��С�մ����ɵ�CO2�����մ����ɵ�CO2����2�� ȷ����һ��������������ˮ���ټ�������BaCl2��Һ��������ϴ�ӡ������������ù��������
3.2 1��10-37.4 2Fe2++2H++H2O2=2Fe3++2H2O ���� ���ĵ�����������ʱ��С�մ����ɵ�CO2�����մ����ɵ�CO2����2�� ȷ����һ��������������ˮ���ټ�������BaCl2��Һ��������ϴ�ӡ������������ù��������
��������������������������ú��������Ʊ����������������Ϊ���壬�������̵ķ����������Լ���ѡ���ܶȻ��ļ��㡢���ӷ���ʽ����д������ˮ���Ӧ�á�ʵ�鷽������ơ�������Ԥ������������ϡH2SO4�����Al2O3��������FeO��xFe2O3�ܽ�ת��Ϊ������ˮ��Al2��SO4��3��FeSO4��Fe2��SO4��3��SiO2�������������SiO2��ϡH2SO4����Ӧ������I�ijɷ�ΪSiO2����ҺI�к�Al2��SO4��3��FeSO4��Fe2��SO4��3����H2SO4������Al3+��Fe2+��Fe3+�����������������pH���Լ�A�������ǽ�Fe2+������Fe3+��Ȼ������Լ�B����pH=a��ȥFe3+����ҺIIΪAl2��SO4��3��Һ��
��1��������������������I�ijɷ�ΪSiO2������XΪ��Al2��SO4��3��Һ�л��Al2��SO4��3��18H2O������X�������ǣ�����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����
��2���Լ�B����������pH��ȥFe3+��Ϊ�˲����������ʣ��Լ�B�����Al2O3��Al��OH��3������Al3+��ʼ������pHΪ3.6��Fe3+��ȫ������pHΪ3.2��a�ķ�Χ�ǣ�3.2![]() a
a![]() 3.6�����ݱ�������Fe3+��ȫ����ʱpH=3.2��c��H+��=10-3.2mol/L��c��OH-��=10-10.8mol/L��Ksp[Fe��OH��3]=c��Fe3+����c3��OH-��
3.6�����ݱ�������Fe3+��ȫ����ʱpH=3.2��c��H+��=10-3.2mol/L��c��OH-��=10-10.8mol/L��Ksp[Fe��OH��3]=c��Fe3+����c3��OH-��![]() 1
1![]() 10-5
10-5![]() ��10-10.8��3=1
��10-10.8��3=1![]() 10-37.4��
10-37.4��
��3���Լ�A��Fe2+������Fe3+���Լ�A��һ��Һ̬��ɫ���������Լ�AΪH2O2����ҺI�з�Ӧ�����ӷ���ʽΪ2Fe2++H2O2+2H+=2Fe3++2H2O��
��4������������ǿ�������Σ�����Al3+��ˮ��Al2��SO4��3��Һ�����ԣ��ɸ�ʴ��Ͳ��Al2��SO4��3��ҺӦʢ���ڲ��������С�Al2��SO4��3��Һ��С�մ���NaHCO3����Һ��Ӧ�ķ���ʽΪAl2��SO4��3+6NaHCO3=2Al��OH��3��+6CO2��+3Na2SO4��Al2��SO4��3��Һ���մ���Na2CO3����Һ��Ӧ�ķ���ʽΪAl2��SO4��3+3Na2CO3+3H2O=2Al��OH��3��+3CO2��+3Na2SO4�����ݷ���ʽ�ɼ������ĵ�����������ʱС�մ����ɵ�CO2�����մ����ɵ�O2����2�������Ч��NaHCO3��Na2CO3����������ĭ���������һ���Լ���С�մ���Һ�������մ���Һ��
��5��Ҫȷ�����Ƶõľ�������Ƿ��������ϵ����[Al2(SO4)3��18H2O]��ͬ����ͨ������һ����������Al2��SO4��3��ˮ�������Ƿ������������ͬ���ɴﵽĿ�����罫һ�����ľ�����ȫ����ˮ����������BaCl2��Һ��ַ�Ӧ������������BaSO4������������Al2��SO4��3����������Ҫ�IJ�������Ϊ��ȷ����һ��������������ˮ���ټ�������BaCl2��Һ��������ϴ�ӡ������������ù����������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������E(nl)��ʾij�ܼ������������¸�ʽ����ȷ����(����)
A. E(3s)>E(2s)>E(1s) B. E(3s)>E(3p)>E(3d)
C. E(4f)>E(4s)>E(3d) D. E(5s)>E(4s)>E(4f)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��������ͨ�����û����ֿ����������������ͬ�����ҳ���һ����NO�����ҳ���һ����O2����ǡ��ʹ�������������ܶ���ͬ��������ʹNO��O2��ַ�Ӧ�������ж���ȷ����(������NO2ת��ΪN2O4) ( )
![]()
A.��Ӧǰ�����ҵ�ѹǿ��ͬ
B.��ʼʱ���������еķ�������ͬ
C.��Ӧ�������ڵ��ܶ��뷴Ӧǰ����ͬ
D.��Ӧ����������O2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������(K2FeO4)��һ�����͡���Ч�������ɫˮ����������Cl2��O2��ClO2��KMnO4�����Ը�ǿ��������Ⱦ����ҵ�������Ƶø������ƣ�Ȼ���ڵ����£������������Һ�м���KOH�����ͣ�ʹ�������������
(1)�ɷ��Ʊ��������Ƶ���Ҫ��ӦΪ��2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2�����÷�Ӧ�л�ԭ����___________________(�ѧʽ)����2 mol FeSO4��ԭ�Ĺ�������Ϊ_________mol
(2)ʪ���Ʊ��������(K2FeO4)�ķ�Ӧ��ϵ������������Fe(OH)3��ClO����OH����FeO42-��Cl����H2O��д�������������Ƹ�����ص����ӷ�Ӧ����ʽ��__________________________
����֪��2Fe3����2I��=2Fe2����I2��2Fe2����Br2=2Fe3����2Br����
(1)����1 mol FeI2��2 mol FeBr2����Һ��ͨ��2 mol Cl2����ʱ��������������____________�������������ӵ����ʵ����ֱ���_____________________________________________
(2)����a mol FeI2��b mol FeBr2����Һ��ͨ��c mol Cl2����I����Fe2��������ʱ��cΪ_____________(�ú�a��b�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩ��һ����Ҫ�Ļ���ԭ�ϡ����������У�����ͨ����ϩ�ļӳɷ�Ӧһ���Ƶõ��ǣ� ��
A.CH3COOHB.CH3CH2OHC.CH3CH2ClD.CH2BrCH2Br
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������ϩ��������������ȥ�����л��е�������ϩ�IJ���������( )
A.���������ͨ��ʢ�������ϴ��ƿ
B.���������ͨ��ʢ��������ˮ��ϴ��ƿ
C.���������ͨ��ʢ��ˮ��ϴ��ƿ
D.���������ͨ��ʢ�г���ʯ��ˮ��ϴ��ƿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ���������߷ֱ��ʾ1g C3H6���塢1g M��������ͬ�����������ѹǿ���¶ȵĹ�ϵ���Ը���ͼ�ж�M���������

A��PH3 B��N2 C��C3H4 D��N2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڵ���ʵ�������ȷ����( )
A.�����Ժ�ǿ������
B.������ˮ������״̬���ܵ���Ļ�����
C.������ˮ������״̬�¾�����Ļ�����
D.����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�����Һ�еĸ������ʵ����ʵ���Ũ�Ⱦ�Ϊ0.1 mol/L����H2S��Һ����KHS��Һ����K2S��Һ����H2S��KHS�����Һ�� ����˵����ȷ����
A. ��ҺpH�Ӵ�С��˳���ǣ��� > �� > �� > ��
B. ��KHS��Һ���У�c(H+) + c(K+) = c(OH-) + c(HS-) + c(S2-)
C. c(H2S)�Ӵ�С��˳���ǣ��� > �� > �� > ��
D. ��H2S��KHS�����Һ���У�c(H2S) + c(HS-) + c(S2-) = 2c(K+)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com