
【题目】下图中两条曲线分别表示1g C3H6气体、1g M气体在相同体积的容器中压强和温度的关系,试根据图判断M气体可能是

A.PH3 B.N2 C.C3H4 D.N2O
科目:高中化学 来源: 题型:
【题目】已知: ①亚硝酸钠(NaNO2)是一种食品添加剂,为无色、无气味的同体,具有防腐和抗氧化作用。②AgNO2是一种微溶于水、易溶于酸的浅黄色固体。
I.问题探究
(1)人体正常的血红蛋白中应含Fe2+,误食亚硝酸盐(如NaNO2)会致使机体组织缺氧,出现青紫而中毒,原因是___________。若发生中毒时,你认为下列物质有助于解毒的是____(填字母)。
A.牛奶 B.Mg(OH)2 C.维生素C D.小苏打
(2)由于亚硝酸钠和食盐性状相似,曾多次发生过将NaNO2误当食盐食用的事件。要区别NaNO2和NaCl两种固体,你需用的试剂是_______________。
II.实验测定
为了测定某样品中NaNO2的含量,某同学进行如下实验:
①称取样品ag,加水溶解,配制成100mL溶液。
②取25.00mL溶液于锥形瓶中,用0.0200mol/LKMnO4标准溶液(酸性)进行滴定,滴定结束后消耗KMnO4溶液VmL。
(1)上述实验①所需玻璃仪器除玻璃棒、胶头滴管之外还有________。
(2)在进行滴定操作时,KMnO4溶液盛装在______(填“酸式”或“碱式”)滴定管中。当滴入最后一滴溶液,________时达到滴定终点。
(3)滴定过程中发生反应的离子方程式是________;测得该样品中NaNO2的质量分数为_____。
(4)若滴定管未用KMnO4标准溶液润洗就直接注入,则测定结果______(填“偏大”、“偏小”或“无影响”,下同);若滴定过程中刚出现颜色变化就停止滴定,则测定结果________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有Mg2+、Ba2+、Cl-、HCO3-中的一种或几种离子。为确定其成分,进行以下实验:
实验1:取10mL无色溶液,滴加适量稀盐酸无明显现象。
实验2:另取10mL无色溶液,加入足量的Na2SO4溶液,有白色沉淀生成。
实验3:将实验1后的溶液于锥形瓶中,向锥形瓶中逐滴加入NaOH溶液,滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如右图所示。

回答下列问题:
(1)原溶液中不存在的离子有__________,存在的离子有________________。检验存在的阴离子的方法是________________________________________
(2)实验3中,图像中OA段反应的离子方程式为____________________________。
(3)根据图像计算原溶液中Mg2+的物质的量浓度_______。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
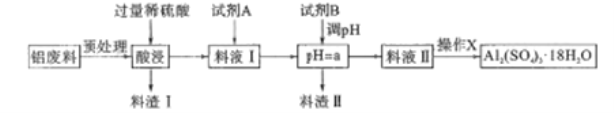
【题目】硫酸铝在造纸、水净化、土壤改良中有着广泛的应用,同时还是泡沫灭火器中的试剂。某化工厂利用含铝废料(成分为A12O3,SiO2及少量FeO·xFe2O3)制备硫酸铝晶体的工艺流程如下图所示,回答相关问题。
又知生成氢氧化物沉淀的pH如下表:
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 3.6 | 6.3 | 2.3 |
完全沉淀时 | 4.9 | 8.3 | 3.2 |
(1)料渣I的成分是__,操作X的内容是__、洗涤、干燥等。
(2)试剂B最好是__,a的范围是__,由表中数据求出Ksp[Fe(OH)3]<_____(设沉淀完全时金属离子浓度小于1×10-5mol/L)。
(3)试剂A是一种液态绿色氧化剂,料液Ⅰ中反应的离子方程式_______
(4)泡沫灭火器容器构造分为内外两层,内层是玻璃容器、外层是钢筒。则硫酸铝溶液应盛放在______容器中,泡沫灭火器中另一种试剂是小苏打溶液而不是苏打溶液的原因是____.
(5)请设计一种简单的方案,用于确定所制得的晶体组成是否与理论上的组成[Al2(SO4)3·18H2O]相同(写出主要操作过程即可):_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下反应会导致溶液导电性减弱最明显的是( )
A.Na2SO4溶液加入BaCl2固体
B.Ba(OH)2溶液中加入CuSO4(少量)固体
C.NaOH溶液通入HCl
D.H2O中加入NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近热播剧《外科风云》中利多卡因药物引发的医疗问题扑朔迷离,盐酸利多卡因(F)葡萄糖注射液,可用于抗心律失常。其合成路线如下:
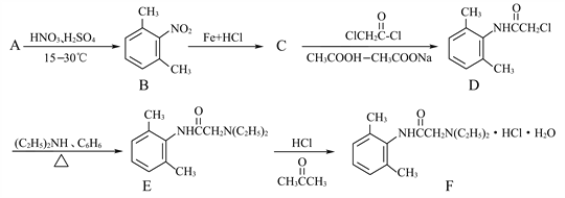
(1)写出A的名称______________________。
(2)C的结构简式为______________________.
(3)B有多种同分异构体,符合以下条件的B的同分异构体(不包括B本身)共有_______________种,请写出其中一种的结构简式_____________________。
①苯环上共有三个取代基 ②与碳酸氢钠溶液反应可放出CO2气体
(4)对氨基苯甲酸是机体细胞生长和分裂所必需的叶酸的组成成分。现以甲苯为原料,结合题干有关信息,补充完成以下合成路线:____________
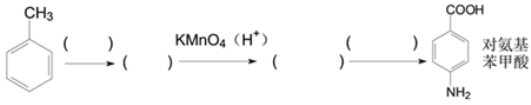
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气中的氮氧化物(NOx)、CO、CO2、SO2 等的含量低高是衡量空气质量优劣的重要指标,对其研究和综合治理具有重要意义。
(1)汽车发动机工作时会引发N2和O2反应。已知:N2中氮氮键的键能是946kJ/mol,O2中氧氧键的键能是498kJ/mol,NO中氮氧键的键能是632kJ/mol。则N2和O2反应生成NO的热化学方程式为_____________。
(2)用CH4催化还原NOx可以消除污染:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(l)。若该反应在恒温恒容容器中达到平衡,下列叙述能作为判断反应达到平衡状态标志的是_____(填标号)。
N2(g)+CO2(g)+2H2O(l)。若该反应在恒温恒容容器中达到平衡,下列叙述能作为判断反应达到平衡状态标志的是_____(填标号)。
A.容器中的压强保持不变
B.容器中氮元素的质量分数不再变化
C.混合气体的平均相对分子质量不再变化
D.n(CH4):n(NO2):n(N2):n(CO2):n(H20)=1:2: 1: 1: 2
(3)为减少CO、CO2对环境造成的影响,采用以下方法将其资源化利用。
①在铝矾土作催化剂、773K条件下,3molCO与1.5molSO2反应生成3molCO2和0.75mol硫蒸气,该反应可用于从烟道气中回收硫,写出该反应的化学方程式_________。
②以CO2为原料采用特殊的电极电解强酸性的CO2水溶液可得到多种燃料,其原理如图所示。电解时其中b极上生成乙烯的电极反应式为_________。
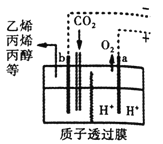
(4)汽车尾气处理催化装置中涉及的反应之一为:2NO(g) +2CO(g)![]() N2(g) +2CO2(g) △H<0
N2(g) +2CO2(g) △H<0
研究表明:在使用等质量的催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某科研小组设计了以下三组实验:
实验编号 | T/K | NO初始浓度/(mol.L-1) | CO初始浓度/(mol.L-1) | 催化剂的比表面积(m2.g-1) |
Ⅰ | 400 | 1.00×10-3 | 3.60×10-3 | 82 |
Ⅱ | 400 | 1.00×10-3 | 3.60×10-3 | 124 |
Ⅲ | 450 | 1.00×10-3 | 3.60×10-3 | 124 |
(注:生成物的起始浓度为0mol/L)
根据下图回答:
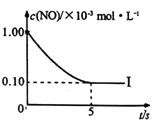
①实验I前5s内用N2 表示的反应速率为________。
②实验I反应的平衡常数KI=_______。
③在图中画出上表中实验Ⅱ、Ⅲ条件下混合气体中NO浓度随时间变化的趋势(标明各条曲线的实验编号) _____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面关于电解质的叙述中错误的是( )
A.在水溶液中和熔融状态下均不导电的化合物叫非电解质
B.电解质、非电解质都指化合物而言,单质不属于此范畴
C.电解质在水中一定能导电,在水中导电的化合物一定是电解质
D.纯水的导电性很差,但水也是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氮化合物在工农业生产中都有重要应用。
(1)氨和肼(N2H4)是两种最常见的氮氢化物。
己知:4NH3(g)+3O2(g) ![]() 2N2(g)+6H2O(g) ΔH1=-541.8kJ/mol,化学平衡常数为K1。N2H4(g)+O2(g)
2N2(g)+6H2O(g) ΔH1=-541.8kJ/mol,化学平衡常数为K1。N2H4(g)+O2(g) ![]() N2(g)+2H2O(g) ΔH2=-534kJ/mol,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为_________,该反应的化学平衡常数K=____(用K1、K2表示)。
N2(g)+2H2O(g) ΔH2=-534kJ/mol,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为_________,该反应的化学平衡常数K=____(用K1、K2表示)。
(2)对于2NO(g)+2CO(g) ![]() N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1molNO和0.3molCO,反应开始进行。
N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1molNO和0.3molCO,反应开始进行。
①下列能说明该反应已经达到平衡状态的是____(填字母代号)。
A.c(CO)=c(CO2) B.容器中混合气体的密度不变
C.v(N2)正=2v(NO)逆 D.容器中混合气体的平均摩尔质量不变
②图1为容器内的压强(P)与起始压强(P0)的比值(P/P0)随时间(t)的变化曲线。0~5min内,该反应的平均反应速率v(N2)= ____,平衡时NO的转化率为____。
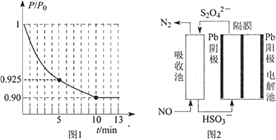
(3)使用间接电化学法可处理燃煤烟气中的NO,装置如图2所示。已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式_________。用离子方程式表示吸收池中除去NO的原理__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com