
【题目】从1L 3mol/L的NaCl溶液中取出100mL溶液,则取出的溶液中含NaCl( )
A.3molB.0.3molC.0.1molD.175.5g
科目:高中化学 来源: 题型:
【题目】下列排列顺序不正确的是
A.原子半径:Si> Na>OB.热稳定性:HF> HCl> H2S
C.碱性:CsOH> KOH> NaOHD.失电子能力:K> Na> Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类正确的是( )
酸 | 碱 | 盐 | 氧化物 | |
A | H2SO4 | Na2CO3 | CaCl2 | H2O |
B | 硝酸 | 烧碱 | 小苏打NaHCO3 | 干冰 |
C | NaHSO4 | 铜绿Cu2(OH)2CO3 | 生石灰 | 熟石灰 |
D | CO2 | 氢氧化铜 | 氯化铵 | 生石灰 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在298K、100kPa时,已知:H2O(g)= ![]() O2(g)+H2(g)△H1H2(g)+Cl2(g)═2HCl(g)△H2
O2(g)+H2(g)△H1H2(g)+Cl2(g)═2HCl(g)△H2
2H2O(g)+2Cl2(g)═4HCl(g)+O2(g)△H3
则△H3与△H1和△H2间的关系正确的是( )
A.△H3=2△H1+2△H2
B.△H3=2△H1﹣△H2
C.△H3=2△H1﹣2△H2
D.△H3=2△H1+△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】侯氏制碱法的原理为:NH3+CO2+H2O+NaCl═NaHCO3↓+NH4Cl,2NaHCO3 ![]() Na2CO3+H2O+CO2↑,实验室模拟该过程包括制备NH3、制取NaHCO3、分离及灼烧NaHCO3四个步骤,下列图示装置能达到实验目的是( )
Na2CO3+H2O+CO2↑,实验室模拟该过程包括制备NH3、制取NaHCO3、分离及灼烧NaHCO3四个步骤,下列图示装置能达到实验目的是( )
A. 制备氨气
制备氨气
B.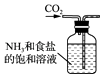 制取NaHCO3
制取NaHCO3
C.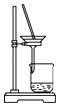 分离NaHCO3
分离NaHCO3
D.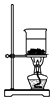 灼烧NaHCO3
灼烧NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于溶液的下列说法正确的是( )
A.等体积、对物质的量浓度的NaX和弱酸HX混合后的溶液中:C(Na+)>c(HX)>c(X﹣)>c(H+)>c(OH﹣)
B.等物质的量浓度的下列溶液:①H2CO3②Na2CO3③NaHCO3④(NH4)2CO3中c(CO32﹣)的大小关系为:②>④>③>①
C.往0.1mol/L CH3COOH溶液中通入少量HCl,醋酸的电离平衡向逆反应方向移动,且溶液中 ![]() 增大
增大
D.Na2CO3溶液中,2c(Na+)=c(CO32﹣)+c(HCO3﹣)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探索工业含铝、铁、铜合金废料的再利用,甲同学设计的实验方案如图: 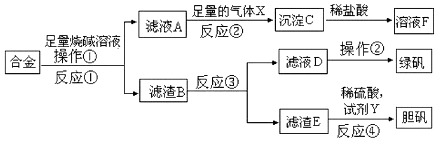
回答下列问题:
(1)操作①的名称为 , 沉淀C的化学式为 .
(2)在滤渣B中滴加稀硫酸时,发现反应速率比同浓度硫酸与纯铁粉反应要快,原因是 .
(3)在滤渣B中滴加的硫酸可用SO2制取,可按以下三步进行: 已知25℃、101kPa时:
2SO2(g)+O2(g)2SO3(g)△H1=﹣197KJ/mol
H2O(g)═H2O(l)△H2=﹣44KJ/mol
2SO2(g)+O2(g)+2H2O(g)═2H2SO4(l)△H3=﹣545KJ/mol
则SO3(g)与H2O(l)反应的热化学方程式是 .
(4)设计实验方案,检测滤液D中含有的金属离子(试剂自选) .
(5)常温下,乙同学将绿矾配成约0.1molL﹣1FeSO4溶液,测得溶液的pH=3,请用离子方程式解释其原因 , 该溶液中c(SO42﹣)﹣c(Fe2+)=molL﹣1(填近似数值).
(6)在滤渣E中加入稀硫酸和试剂Y制胆矾晶体是一种绿色化学工艺,试剂Y为无色液体,则反应④的总反应化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com