
【题目】 I.在实验室利用下列装置,可制备某些气体并验证其化学性质。
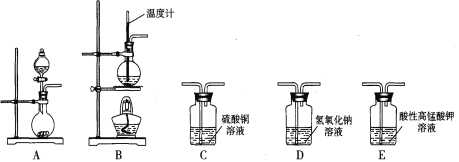
完成下列表格:
序号 | 气体 | 装置连接顺序(填字母) | 制备反应的化学方程式 |
(1) | 乙烯 | __________________ | _________________________ |
(2) | 乙炔 | A→C→E | _________________________ |
II.工业上用乙烯、氯化氢和氯气为原料,经下列各步合成聚氯乙烯(PVC):

A的结构简式是__________________________________________________;
反应④的化学方程式是_________________________________________。
【答案】I.(1)B→D→E(答全,得2分)
![]() (2分)
(2分)
(2)![]() (2分)
(2分)
Ⅱ.CH2ClCH2Cl (2分)
 (2分)
(2分)
【解析】
试题分析:I.(1)在实验室中制取乙烯,需要加热到170℃,应该选择B装置,反应中会发生副反应生成二氧化硫,必须用氢氧化钠溶液除去,所以选择D装置除去二氧化硫杂质,最后用高锰酸钾溶液检验乙烯的性质,所以连接顺序为: B→D→E;实验室利用乙醇能发生消去反应制乙烯:![]() 。(2)实验室制取乙炔的化学反应方程式为:
。(2)实验室制取乙炔的化学反应方程式为:![]() 。Ⅱ.CH2=CH2可与氯气发生加成反应生成CH2Cl-CH2Cl,CH2Cl-CH2Cl发生消去反应生成CH2=CHCl,CH2=CHCl发生加聚反应可生成PVC,反应(4)方程式为
。Ⅱ.CH2=CH2可与氯气发生加成反应生成CH2Cl-CH2Cl,CH2Cl-CH2Cl发生消去反应生成CH2=CHCl,CH2=CHCl发生加聚反应可生成PVC,反应(4)方程式为
 。
。


科目:高中化学 来源: 题型:
【题目】乙烯是重要化工原料,其产量是一个国家石油化工水平的标志。请回答:
(一)乙烯大量用来生产环氧乙烷,生产工艺主要有两种:
【工艺甲】![]()
【工艺乙】![]()
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应。因此,上述生产工艺中,应采用工艺__________(填“甲”或“乙”)更环保、更经济。
(二)某同学设计实验探究工业制乙烯的原理和乙烯的主要化学性质,实验装置如图所示(已知烃类都不与碱反应)。请回答下列问题:
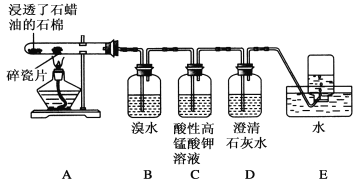
(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应:C16H34![]() C8H18+甲,甲
C8H18+甲,甲![]() 4乙,则甲的分子式为________,乙的结构简式为____________________________________。
4乙,则甲的分子式为________,乙的结构简式为____________________________________。
(2)B装置中的实验现象可能是________,写出反应的化学方程式:________________________,其反应类型是________。
(3)C装置中可观察到的现象是____________,反应类型是________。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置________(填字母)中的实验现象可判断该资料是否真实。为了探究溴与乙烯反应是加成反应而不是取代反应,可以测定装置B中溶液在反应前后的酸碱性,简述其理由: __________________。
(5)通过上述实验探究,检验甲烷和乙烯的方法是________(选填字母,下同);除去甲烷中乙烯的方法是________。
A.气体通入水中
B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶
D.气体通过氢氧化钠溶液
(6)分别燃烧乙烯和甲烷,甲烷火焰明亮而乙烯产生少量黑烟,原因是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究Cl2、SO2同时通入H2O中发生的反应,某化学兴趣小组同学设计了图1所示的实验装置。
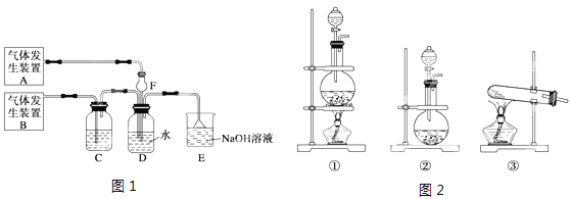
(1)该化学兴趣小组同学为制取Cl2和SO2气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol/L)为原料制取Cl2。请写出制取Cl2的离子方程式:
(2)在此实验中,F仪器的作用是:______________;发生装置B应选择图2三种装置中的___________(填序号)。
(3)D装置中主要反应的离子方程式为 。
(4)为验证通入D装置中过量的气体是Cl2还是SO2气体,兴趣小组的同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰酸钾溶液
④品红溶液 ⑤溴水 ⑥稀硝酸
A.若Cl2过量:取适量D中溶液滴加至盛有 试剂的试管内,发生的现象是: ;(试剂可以多选,请填试剂的序号,下同)。
B.若SO2过量:取适量D中溶液滴加至盛有 试剂的试管内,发生的现象是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效。苹果醋是一种常见的有机酸,其结构简式为![]() 。
。
(1)苹果醋中含有的官能团的名称是________、_____________。
(2)苹果醋的分子式为__________________。
(3)1 mol苹果醋与足量金属钠反应,能生成标准状况下的氢气________L。
(4)苹果醋可能发生的反应是________。
A.与NaOH溶液反应
B.与石蕊溶液作用
C.与乙酸在一定条件下酯化
D.与乙醇在一定条件下酯化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物反应如下图,据此回答下列问题:

(1)乙烯的结构式为: 。
(2)写出反应②④的化学方程式:
② ,反应类型: (1分);
④ ,反应类型: (1分)。
(3)实验室常用下列装置制取乙酸乙酯,请回答相关问题:

①饱和碳酸钠溶液的主要作用是 。
②若要把制得的乙酸乙酯分离出来,应采用的操作是 。
③进行该实验时,最好向试管甲中加入几块碎瓷片,其目的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
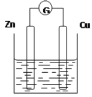
实验后的记录: ①正极的电极反应式:Zn―2e―=Zn2+ ②H+向负极移动 ③电子流动方向Zn→Cu ④在Cu处产生1.12L H2,则电路中一定有0.1mol电子通过 |
(1)在卡片上,叙述合理的是 (填序号)。
(2)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,原因可能是 。
(3)如果把锌片换成石墨,发现电流计指针几乎不能偏转,原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 X、Y、Z、M、Q是中学化学常见的五种元素,原子序数依次增大,其结构或性质信息如下表
元素 | 结构或性质信息 |
X | 其原子最外层电子数是内层电子数的2倍 |
Y | 基态原子最外层电子排布为nsnnpn+1 |
Z | 非金属元素,其单质为固体,在氧气中燃烧时有明亮的蓝紫色火焰 |
M | 单质在常温、常压下是气体。基态原子的M层上有1个未成对的p电子 |
Q | 其与X形成的合金为目前用量最多的金属材料 |
(1)Q元素基态原子的电子排布式是________,Y原子的电子排布图是 。
(2)比较Y元素与氧元素的第一电离能____>____;X和Z形成的化合物XZ2为一种液体溶剂,其化学式是 ,分子中的![]() 键和
键和![]() 键数目之比为_____。
键数目之比为_____。
(3)写出实验室制备M单质的离子方程式 。
(4)M的气态氢化物和氟化氢相比(写化学式)
稳定性强的是_____________,其原因是_____________________;
沸点高的是_____________,其原因是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 12C和14N含有相同的中子数
B. 14C和14N质量数相同,互为同位素
C. 12C和13N中子数相同,质子数不同,互为同位素
D. 12CO和14CO物理性质不同,化学性质基本相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、HCO3-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化如图所示,下列说法正确的是 ( )
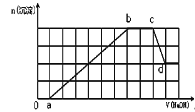
A.ab段发生的离子反应为:Al3++3OH-= Al(OH)3↓, Mg2++2OH-= Mg(OH)2↓
B.原溶液中含有的阳离子必定有H+、NH4+、Al3+、Mg2+
C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
D.d点溶液中含有的溶质只有NaAlO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com