
【题目】有机化合物反应如下图,据此回答下列问题:

(1)乙烯的结构式为: 。
(2)写出反应②④的化学方程式:
② ,反应类型: (1分);
④ ,反应类型: (1分)。
(3)实验室常用下列装置制取乙酸乙酯,请回答相关问题:

①饱和碳酸钠溶液的主要作用是 。
②若要把制得的乙酸乙酯分离出来,应采用的操作是 。
③进行该实验时,最好向试管甲中加入几块碎瓷片,其目的是 。
【答案】(1)![]()
(2)2CH3CH2OH+O2![]() 2CH3CHO+2H2O 氧化反应 CH3COOH+CH3CH2OH
2CH3CHO+2H2O 氧化反应 CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O 酯化反应(或取代反应)(1分)(3)①酯在其中的溶解度小,有利于酯分离、除去粗产品中的乙酸(或乙酸、乙醇)②分液 ③防暴沸(防止剧烈沸腾)
CH3COOCH2CH3+H2O 酯化反应(或取代反应)(1分)(3)①酯在其中的溶解度小,有利于酯分离、除去粗产品中的乙酸(或乙酸、乙醇)②分液 ③防暴沸(防止剧烈沸腾)
【解析】试题分析:(1)根据题给转化关系知,乙烯和水发生加成反应生成乙醇,乙醇在铜作催化剂、加热条件下被氧气氧化生成乙醛,乙醇和D发生酯化反应生成乙酸乙酯,则D是乙酸,乙烯发生加聚反应生成聚乙烯。(1)乙烯的结构式为:![]() ;(2)反应②④的化学方程式和反应类型分别为:2CH3CH2OH+O2
;(2)反应②④的化学方程式和反应类型分别为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O 氧化反应 CH3COOH+CH3CH2OH
2CH3CHO+2H2O 氧化反应 CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O 酯化反应(或取代反应);(3)根据乙酸乙酯的制备实验可知:
CH3COOCH2CH3+H2O 酯化反应(或取代反应);(3)根据乙酸乙酯的制备实验可知:
① 饱和碳酸钠溶液的主要作用是:除去乙酸,溶解乙醇,降低乙酸乙酯的溶解度。②乙酸乙酯和碳酸钠溶液时互不相容的两种液体,故用分液的方法分离;③加入几块碎瓷片,其目的是防止爆沸。


科目:高中化学 来源: 题型:
【题目】中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用。若1 mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
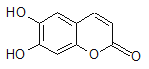
A、2 mol Br2 2 mol NaOH
B、2 mol Br2 3 mol NaOH
C、3 mol Br2 4 mol NaOH
D、4 mol Br2 4 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)冶炼金属的三种常用方法是:A.热分解法 B.热还原剂法 C.电解法。人类用量处在前三位的金属是铁、铝、铜。(填编号)(化学方程式书写每空2分,其余每空1分)
① 冶炼铝用到的方法是 ;
② 冶炼铁和铜的常用方法是 。
③ 写出电解熔融氯化镁制取金属镁的化学反应方程式: 。
(2)保护环境、保护地球已成为人类共同的呼声。(化学方程式书写每空2分,其余每空1分)
① 引起温室效应的主要物质是 ;
②以煤炭为主的能源结构易导致酸雨的形成,形成这类酸雨的气体是 ,形成过程发生的化学反应有: 、 (写出两个)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、D、E、F为原子序数依次增大的五种短周期主族元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B单质在D单质中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A单质在F单质中燃烧,产物溶于水得到一种强酸。用相应的化学用语回答下列问题:
(1)A在周期表中的位置是 。AFD的电子式为 。
(2)BD2的结构式为 ; BD2形成晶体的类型为 。
(3)元素D、E 、F形成的简单离子的半径由大到小为 (用离子符号表示)。
(4)写出实验室制备单质F的离子方程式 。
(5)写出E与D形成的既含离子键又含共价键的化合物与水反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 I.在实验室利用下列装置,可制备某些气体并验证其化学性质。
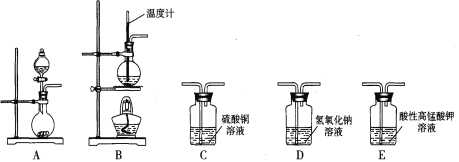
完成下列表格:
序号 | 气体 | 装置连接顺序(填字母) | 制备反应的化学方程式 |
(1) | 乙烯 | __________________ | _________________________ |
(2) | 乙炔 | A→C→E | _________________________ |
II.工业上用乙烯、氯化氢和氯气为原料,经下列各步合成聚氯乙烯(PVC):

A的结构简式是__________________________________________________;
反应④的化学方程式是_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z在元素周期表中的相对位置如下图所示。下列说法一定正确的是
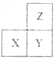
A. 若X为非金属元素,则离子半径:Xn->Ym->Zm-
B. X、Y、Z的单质中,Z单质的熔点最高
C. 最高正化合价:Z>X
D. X、Y、Z的最高价氧化物对应水化物中,Y的碱性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列递变规律不正确的是
A. N a、Mg、Al原子的失电子能力逐渐减弱
B. Si、P、S元素的最高正化合价依次降低
C. C、N、O的原子半径依次减小
D. Cl、Br、I的气态氢化物的稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用NaHCO3和KHCO3组成的混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)。下列分析推理正确的是
盐酸 | 50 mL | 50 mL | 50 mL |
m(混合物) | 9.2 g | 14.2 g | 27.6 g |
V(CO2)(标准状况) | 2.24 L | 3.36 L | 3.36 L |
A.盐酸的物质的量浓度为3.0 mol/L
B.当混合物质量为9.2 g时,50 mL盐酸恰好完全反应
C.混合物中NaHCO3、KHCO3的物质的量之比为1∶2
D.混合物中NaHCO3的质量分数为45.7 %
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com