
【题目】A、B、D、E、F为原子序数依次增大的五种短周期主族元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B单质在D单质中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A单质在F单质中燃烧,产物溶于水得到一种强酸。用相应的化学用语回答下列问题:
(1)A在周期表中的位置是 。AFD的电子式为 。
(2)BD2的结构式为 ; BD2形成晶体的类型为 。
(3)元素D、E 、F形成的简单离子的半径由大到小为 (用离子符号表示)。
(4)写出实验室制备单质F的离子方程式 。
(5)写出E与D形成的既含离子键又含共价键的化合物与水反应的化学方程式 。
【答案】(1) 第一周期IA族 、 ![]()
(2)![]() , 分子晶体
, 分子晶体
(3)Cl﹣>O2—>Na+
(4)MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(5)2Na2O2+2H2O=4NaOH+O2↑
【解析】
试题分析:A、B、C、D、E、F为原子序数依次增大的五种短周期主族元素,非金属元素A最外层电子数与其周期数相同,则A为H元素;E+与D2-具有相同的电子数,则E处于IA族,D处于ⅥA族,则E为Na、D为O元素;B在D中充分燃烧生成其最高价化合物BD2,B的最高正化合价为+4,B的最外层电子数是其所在周期数的2倍,则B处于第二周期,故B为碳元素;C的原子序数介于碳、氧之间,故C为N元素;A在F中燃烧,产物溶于水得到种强酸,则F为Cl;(1)A为H元素,在周期表中的位置是:第一周期IA族.AFD的化学式为HClO,电子式为,![]() ;(2)BD2的化学式为CO2,结构式为O=C=O,属于分子晶体,故答案为:O=C=O;分子晶体;
;(2)BD2的化学式为CO2,结构式为O=C=O,属于分子晶体,故答案为:O=C=O;分子晶体;
(3)元素D、E、F形成的简单离子分别为O2-、Na+、Cl-,电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,故离子半径:Cl->O2->Na+,故答案为:Cl->O2->Na+;
(4)实验室制备氯气的离子方程式:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(5)Na与O形成的既含离子键又含共价键的化合物为Na2O2,与水反应的化学方程式:2Na2O2+2H2O=4NaOH+O2↑。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】中国气象局的数据显示,2013年全国平均雾霾天数为52年来之最。形成雾霾的主要成份为:生产生活中排放的废气、汽车尾气及扬尘等。
(1)己知:CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=-4lkJ/mol,某温度下,向容积为2L的密闭容器中充入2.0molCO(g)和2.0mol H2O(g),在tmin时达到平衡,测得放出了32.8kJ热量,则tmin内用H2表示的平均反应速率为_________,由此可知在该温度下反应CO(g)+H2O(g)
CO2(g)+H2(g)△H=-4lkJ/mol,某温度下,向容积为2L的密闭容器中充入2.0molCO(g)和2.0mol H2O(g),在tmin时达到平衡,测得放出了32.8kJ热量,则tmin内用H2表示的平均反应速率为_________,由此可知在该温度下反应CO(g)+H2O(g)![]() CO2(g)+H2(g)的化学平衡常数为_________(保留小数点后一位)。
CO2(g)+H2(g)的化学平衡常数为_________(保留小数点后一位)。
(2)碱式硫酸铝法烟气脱硫工艺主要有以下三步
①向Al2(SO4)3溶液中投入粉末状石灰石,生成碱式硫酸铝[Al2(SO4)3Al2O3]溶液.
②碱式硫酸铝吸收SO2,Al2(SO4)3Al2O3+3SO2=Al2(SO4)3Al2(SO3)3,请写出Al2(SO4)3Al2O3与过量烧碱溶液反应的化学方程式:_________;
③将Al2(SO4)3Al2 (SO3)3氧化成Al2(SO4)3,可选用氧化剂为_________(填代号).
a.浓硫酸 b.KMnO4溶液 C.5%的H2O2溶液 d.空气
该步反应的目的是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

请回答下列问题:
(1)对青蒿进行干燥破碎的目的是_____________。
(2)操作I需要的玻璃仪器主要有:烧杯、_________,操作Ⅱ的名称是_______________。
(3)操作Ⅲ的主要过程可能是_____________(填字母)。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)用下列实验装置测定青蒿素分子式的方法如下:将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。

①装置E中盛放的物质是______________,装置F中盛放的物质是________________。
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是_______________。
③用合理改进后的装置进行试验,称得:

则测得青蒿素的最简式是__________________。
(5)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与____________(填字母)具有相同的性质。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
(6)某科研小组经多次提取青蒿素实验认为用石油醚做溶剂较为适宜,实验中通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响,其结果如下图所示:

由上图可知控制其他实验条件不变,采用的最佳粒度、时间和温度为_______________。
A.80目、100分钟、50℃ B.60目、120分钟、50℃ C.60目、120分钟、55℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有以下几种有机物:
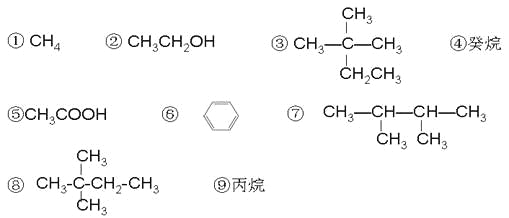
请利用上述给出的物质按要求回答下列问题:
(1)相对分子质量为44的烷烃的结构简式为 ;
(2)分子中含有14个氢原子的烷烃的分子式是 ;
(3)与③互为同分异构体的是 (填序号);
(4)具有特殊气味,常作萃取剂的有机物在铁作催化剂的条件下与液溴发生一取代反应的化学方程式 ;
(5)用“>”表示①③④⑨熔沸点高低顺序: (填序号);
(6)有机物②在加热条件下和CuO反应的化学方程式 ;
(7)在120℃,1.01×105Pa条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃是 (填序号);它与⑧互为 关系;
(8)有机物⑤和②在一定条件下发生反应的化学方程式是 ;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物反应如下图,据此回答下列问题:

(1)乙烯的结构式为: 。
(2)写出反应②④的化学方程式:
② ,反应类型: (1分);
④ ,反应类型: (1分)。
(3)实验室常用下列装置制取乙酸乙酯,请回答相关问题:

①饱和碳酸钠溶液的主要作用是 。
②若要把制得的乙酸乙酯分离出来,应采用的操作是 。
③进行该实验时,最好向试管甲中加入几块碎瓷片,其目的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中,正确的是( )

A. 燃料电池工作时,正极反应为:O2 + 2H2O + 4e-= 4OH-
B. a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出
C. a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
D. a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于某溶液中所含离子的鉴别,下列判断正确的是
A.加入BaCl2溶液,生成白色沉淀,加稀硝酸沉淀不消失,则原溶液中一定含有SO42-
B.加入NaOH溶液,生成的白色沉淀在空气中迅速变为灰绿色,最终变为红褐色,则原溶液中一定含有Fe2+。
C.用洁净的铂丝蘸取溶液在火焰上灼烧,产生黄色的火焰,则原溶液中一定不含有K+
D.加盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定含有CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com