
常温下,下列各溶液的叙述中正确的是
A.NaHSO3与Na2SO3混合溶液中:3c(Na+)=c(HSO3-)+c(SO32-)
B.0.1 mol/L的醋酸钠溶液20 mL与0.1 mol/L盐酸10 mL混合后溶液显酸性:
c(CH3COO-)>c(CH3COOH) >c(Cl-)>c(H+)
C.等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-)
D.向1.00 L 0.3 mol/L NaOH溶液中缓慢通入0.2 mol CO2气体,溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
C
【解析】
试题分析:A.在NaHSO3与Na2SO3混合溶液中:根据物料守恒, c(Na+)=3c(HSO3-)+3c(SO32-)+3c(H2SO3),Na+离子的浓度最大,错误;B.0.1 mol/L的醋酸钠溶液20 mL与0.1 mol/L盐酸10 mL混合后溶液是NaCl、CH3COONa、CH3COOH等物质的量的混合溶液,由于溶液显酸性,说明:CH3COOH的电离作用大于CH3COO-的水解作用,所以c(CH3COO-)>c(CH3COOH);c(Cl-)>c(CH3COOH) ,弱酸的电离作用是微弱的,物质主要以电解质分子的形式存在所以c(CH3COOH) > c(H+),故溶液中离子浓度关系是c(CH3COO-) >c(Cl-)>c(CH3COOH) > c(H+),错误;C.等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)=c(SO42-),由于铵根离子会发生水解作用消耗水电离产生的OH-,最终使溶液显酸性,所以c(SO42-)>c(NH4+), c(H+)>c(OH-)。但是盐的水解作用是微弱的,主要以盐的离子的形式存在,所以c(NH4+)>c(H+),因此溶液中两种浓度关系是c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-),正确;D.向1.00 L 0.3 mol/L NaOH溶液中缓慢通入0.2 mol CO2气体,会发生反应CO2+2NaOH=Na2CO3+H2O NaOH +CO2 =NaHCO3 根据Na元素守恒可得2n(Na2CO3)+n(NaHCO3)=0.3ml;根据C元素守恒可得n(Na2CO3)+n(NaHCO3)=0.2mol,解得n(Na2CO3)=n(NaHCO3)=0.1mol。由于Na2CO3水解程度大于NaHCO3,所以c(HCO3-)>c(CO32-),二者水解是显碱性,所以c(OH-)>c(H+),但是盐的水解程度是微弱的,主要以盐的离子存在,所以c(CO32-)> c(OH-)。故溶液中离子浓度大小关系是c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),错误。
考点:考查溶液中离子浓度的大小比较的知识。


科目:高中化学 来源:2014-2015学年四川省高一10月月考化学试卷(解析版) 题型:选择题
某同学用Na2CO3配制0.10 mol/L Na2CO3溶液的过程如图所示。你认为该同学的错误有
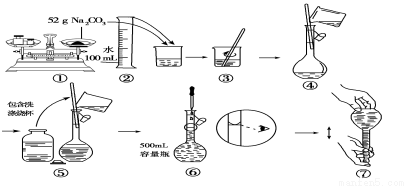
A.①⑤⑥ B.②④⑦ C.①⑥ D.⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川成都树德协进中学高二10月阶段性考试化学试卷(解析版) 题型:填空题
(14分)下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
|
|
| |||||||||||||||
A | B |
|
| C | D |
|
|
| |||||||||
E | F | G |
|
| H | I |
| ||||||||||
|
|
|
|
| J |
|
|
|
| K |
|
|
|
|
| M |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| L |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
试回答下列问题:
(1)写出基态时J的电子排布式 ,L的原子序数为 ,M的简化电子排布式 。
(2)下列关于元素在元素周期表中的位置的叙述正确的是 。
A.K位于元素周期表中第四周期、ⅡB族,属于ds区元素;
B.J位于元素周期表中第四周期、ⅣB族,属于d区元素;
C.F位于元素周期表中第三周期、ⅡA族,属于s区元素;
D.I位于元素周期表中第三周期、ⅦA族,属于ds区元素;
(3)下列有关说法正确的是 。
A.第一电离能G>F>E; B.电负性D>C;
C.原子半径E>B D.最高价含氧酸的酸性I>H
(4)根据对角线规则及已知元素性质,回答下列问题:
①B元素最高价氧化物的水化物与E元素最高价氧化物的水化物的溶液反应的离子方程
式 。
②A元素的单质与氧气在点燃时的化学反应方程式 。
(5)下图是部分元素原子的第一电离能I1随原子序数变化的曲线图。
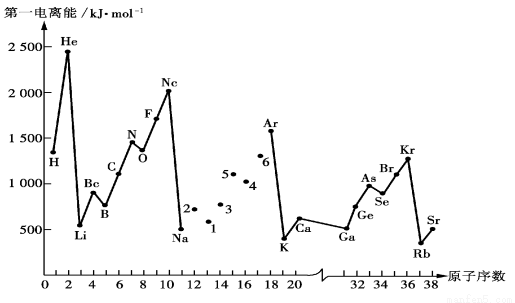
① 认真分析下图中同周期元素第一电离能的变化规律,将Na——Ar之间六种元素用短线连接起来,构成完整的图像。
② 从下图分析可知,同一主族元素原子的第一电离能I1变化规律是
___________________________________________________________________________;
Zn的第一电离能大于Ga的原因是
。
③上图中5号元素在周期表中的位置是____________________________;
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川成都树德协进中学高二10月阶段性考试化学试卷(解析版) 题型:选择题
下列说法中错误的是
A.同一元素的各种同位素的化学性质相似
B.元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
C.除氦外的稀有气体原子的最外层电子数都是8
D.原子及其离子的核外电子层数等于该元素所在的周期数
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川成都树德协进中学高二10月阶段性考试化学试卷(解析版) 题型:选择题
在物质结构研究的历史上,首先提出原子结构有核模型的科学家是
A.汤姆生 B.道尔顿 C.玻尔 D.卢瑟福
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省长春市新高三起点调研考试化学试卷(解析版) 题型:选择题
根据下图的转化关系判断下列说法正确的是(反应条件已略去)

A.反应①②③④⑤均属于氧化还原反应和离子反应
B.反应⑤说明该条件下铝可用于制熔点较高的金属
C.相同条件下生成等量的O2,反应③和④转移的电子数之比为1∶1
D.反应①中氧化剂与还原剂的物质的量之比为1∶4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省长春市新高三起点调研考试化学试卷(解析版) 题型:选择题
下列变化不属于取代反应的是
A.CH3COOC2H5+H2O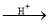 CH3COOH+C2H5OH B.CH3=CH2+H2
CH3COOH+C2H5OH B.CH3=CH2+H2 CH3CH3
CH3CH3
C. +HNO3
+HNO3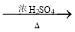
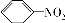 +H2O D.CH4+Cl2
+H2O D.CH4+Cl2 CH3Cl+HCl
CH3Cl+HCl
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省长春外国语学校高二上学期期中化学试卷(解析版) 题型:选择题
下列变化不属于化学变化的是
A.煤的高温干馏
B.煤的气化
C.石油分馏得到汽油、柴油等
D.石油的催化裂化
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省高二上学期期中考试化学试卷(解析版) 题型:填空题
(2分).由氢气和氧气反应生成1mol水蒸气放热241.8KJ,写出该反应的热化学方程式:
_____________________ _ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com