
【题目】可确认发生了化学平衡移动的是( )
A.化学反应速率发生了改变
B.有气态物质参加的可逆反应达到平衡后,改变了压强
C.由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变
D.可逆反应达到平衡后,使用催化剂
【答案】C
【解析】解:A.化学反应速率发生改变,未必能说明化学平衡发生了移动,当正反应速率与逆反应速率仍然相等时,化学平衡不会发生移动;当正反应速率与逆反应速率不相等时,化学平衡就会发生移动,故A错误; B.对于气体总体积反应前后不变的可逆反应(如I2+H2 ![]() 2HI)来说,无论是否建立平衡,其总物质的量即压强都不会发生变化;对于气体总体积反应前后不等的可逆反应(如2SO2+O2
2HI)来说,无论是否建立平衡,其总物质的量即压强都不会发生变化;对于气体总体积反应前后不等的可逆反应(如2SO2+O2 ![]() 2SO3)来说,建立化学平衡状态时,总物质的量要与初始时的总物质的量不等,故压强要改变,故B错误;
2SO3)来说,建立化学平衡状态时,总物质的量要与初始时的总物质的量不等,故压强要改变,故B错误;
C.当平衡混合物各组分的浓度发生不同程度的变化时,就说明化学平衡向某个方向(正反应方向或逆反应方向)进行,即化学平衡发生了移动,故C正确.值得补充的是,当平衡混合物各组分的浓度发生同等程度的变化时,化学平衡未必发生移动,如对于I2+H2 ![]() 2HI来说,当增大加强减小体积时,就不会发生化学平衡的移动,故C正确;
2HI来说,当增大加强减小体积时,就不会发生化学平衡的移动,故C正确;
D.催化剂只能同等程度地改变正反应速率和逆反应速率,当一个可逆反应建立化学平衡状态后,加入催化剂,正反应速率仍然等于逆反应速率,化学平衡不会发生移动,故D错误;
故选C.
【考点精析】关于本题考查的化学平衡状态本质及特征和化学平衡状态的判断,需要了解化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效);状态判断:①v(B耗)=v(B生)②v(C耗):v(D生)=x : y③c(C)、C%、n(C)%等不变④若A、B、C、D为气体,且m+n≠x+y,压强恒定⑤体系颜色不变⑥单位时间内某物质内化学键的断裂量等于形成量⑦体系平均式量恒定(m+n ≠ x+y)等才能得出正确答案.


科目:高中化学 来源: 题型:
【题目】甲、乙两个小组利用酸性KMnO4与H2C2O4溶液反应,设计实验探究影响反应速率的因素(2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2+8H2O) 甲组:利用如图装置,通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小.(实验中所用KMnO4溶液均已加入H2SO4)
序号 | A溶液 | B溶液 |
① | 2ml 0.2mol/LH2C2O4溶液 | 4ml 0.01mol/LKMnO4溶液 |
② | 2ml 0.1mol/LH2C2O4溶液 | 4ml 0.01mol/LKMnO4溶液 |
③ | 2ml 0.2mol/LH2C2O4溶液 | 4ml 0.01mol/LKMnO4溶液和少量MnSO4 |
(1)该实验的目的是探究对化学反应速率的影响.
(2)分液漏斗中A溶液应该加入(填“一次性”或“逐滴滴加”)
(3)实验结束后,读数前为了使两个量气管的压强相等,避免产生压强差,影响测定结果,需要进行的操作是 . 乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率为了探究KMnO4与H2C2O4浓度对反应速率的影响,某同学在室温下完成以下实验
实验编号 | 1 | 2 | 3 | 4 |
水/ml | 10 | 5 | 0 | X |
0.5mol/L H2C2O4/ml | 5 | 10 | 10 | 5 |
0.2mol/L KMnO4/ml | 5 | 5 | 10 | 10 |
时间/s | 40 | 20 | 10 | ﹣﹣﹣ |
(4)X= A.5 B.10 C.15 D.20
4号实验中始终没有观察到溶液褪色,你认为可能的原因是 . 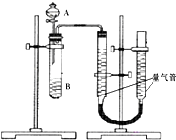
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:

据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是_____.
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式
沉淀固体B______;C________;沉淀D_____;溶液E________.
(3)写出①、②、③、④四个反应方程式
①_________________________;
②________________________;
③________________________;
④________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:

据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是_____.
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式
沉淀固体B______;C________;沉淀D_____;溶液E________.
(3)写出①、②、③、④四个反应方程式
①_________________________;
②________________________;
③________________________;
④________________________.
【答案】 过滤 Al2O3 Al2O3、Fe2O3 Fe2O3 K2SO4、(NH4)2SO4 Al2O3+2NaOH+3H2O=2Na[Al(OH)4] 2KAl(SO4)2+6 NH3.H2O=K2SO4+3(NH4)2SO4+2Al(OH)3↓ Na[Al(OH)4]+HCl=NaCl+H2O+Al(OH)3↓ 2Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O
【解析】KAl(SO4)2溶于水,Al2O3和Fe2O3均不溶于水,混合物A加水溶解后,溶液中是KAl(SO4)2,沉淀C为Al2O3和Fe2O3;由转化关系图可知,向沉淀C中加NaOH溶液,Fe2O3不反应,沉淀D为Fe2O3,Al2O3可与NaOH溶液反应生成NaAlO2,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀,Al(OH)3受热分解生成固体B为Al2O3;向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中E为K2SO4、(NH4)2SO4,经过蒸发、结晶,得到K2SO4和(NH4)2SO4;
(1)溶液和沉淀的分离利用过滤;
(2)由上述分析可知B为Al2O3,C为Al2O3、Fe2O3,D为Fe2O3溶液E为K2SO4、(NH4)2SO4;
(3)反应①为Al2O3+2NaOH+3H2O=2Na[Al(OH)4],
反应②为2KAl(SO4)2+6NH3.H2O=K2SO4+3(NH4)2SO4+2Al(OH)3↓,
反应③为Na[Al(OH)4]+HCl=NaCl+H2O+Al(OH)3↓,
反应④为2Al(OH)3![]() Al2O3+3H2O。
Al2O3+3H2O。
点睛:考查无机物的推断,综合考查元素化合物性质,侧重Al、Fe及其化合物性质的考查,注意氧化铝的两性,明确发生的化学反应为解答的关键,由转化关系图可知,向沉淀C中加NaOH溶液,Fe2O3不反应,沉淀D为Fe2O3,Al2O3可与NaOH溶液反应生成NaAlO2,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀,Al(OH)3受热分解生成固体B为Al2O3;向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中E为K2SO4、(NH4)2SO4,经过蒸发、结晶,得到K2SO4和(NH4)2SO4,然后结合物质的性质及化学用语来解答。
【题型】填空题
【结束】
26
【题目】在常温下,Fe与水并不发生反应,但在高温下,Fe与水蒸气可发生反应。应用如图所示装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下Fe与水蒸气反应的实验。

请回答该实验中的问题。
(1)写出Fe与水蒸气反应的化学方程式:____________________________________。
(2)实验前必须对整套装置进行的操作是__________________________。
(3)圆底烧瓶中盛装的是水,该装置受热后的主要作用是_________________________。
(4)干燥管中盛装的物质可以是________________,作用是_______________。
(5)试管中收集到的气体,若要在处玻璃管口处点燃该气体,则必须对该气体进行__________,目的是:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需1 mol·L-1的CuSO4溶液750 mL,配制时应选用的容量瓶的规格和称取CuSO4固体的质量分别为
A. 容量瓶:500 mL、250 mL各一个; CuSO4:共120.0 g
B. 容量瓶:750 mL、 CuSO4:120.0 g
C. 容量瓶:1 000 mL、CuSO4晶体:250.0 g
D. 容量瓶:1 000 mL、 CuSO4:160.0 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有一份含有杂质MgCl2和KCl的AlCl3溶液M,某小组用下图所示过程对其进行除杂并尽可能的减少AlCl3的损失。请回答下列问题:

(1)沉淀A的化学式为__________,过程①中Al3+发生反应的离子方程式为__________________。
(2)氢氧化钠溶液_____(填“能”或“不能”)用氨水代替,原因是_____________________。
(3)溶液B中大量存在的阳离子是______________,过程②中生成沉淀C的离子方程式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质的名称正确的是
A. 3,3-二甲基丁烷B. 2,3,3-三甲丁烷
C. 2,2-二甲基-3-乙基丁烷D. 2,3-二甲基-4-乙基己烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com