
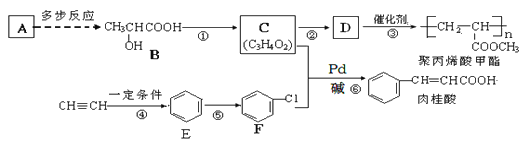
【题目】A(C2H4)是基本的有机化工原料,由A制备聚丙烯酸甲酯(有机玻璃主要成分)和肉桂酸的合成路线(部分反应条件略去)如下图所示:
已知:![]() +CH2=CH-R
+CH2=CH-R![]() +HX(X为卤原子,R为取代基)
+HX(X为卤原子,R为取代基)
回答下列问题:
(1)反应①的反应条件是_______;⑥的反应类型是_____。
(2)B的名称为_______________________________;
(3)由C制取D的化学方程式为__________。
(4)肉桂酸的同分异构体中能同时满足下列条件:①苯环上有两个取代基且苯环上的一氯代物有两种②能发生银镜反应,③能与FeCl3溶液发生显色反应。请写出符合上述要求物质的结构简式:________。
(5)已知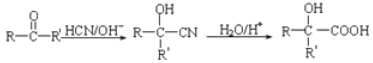 由A制备B的合成路线如下(其中部分反应条件已省略):
由A制备B的合成路线如下(其中部分反应条件已省略):
CH2=CH2→X ![]() Y→Z
Y→Z![]()
![]()
则X→Y反应方程式为______________, Z的结构简式为_______________。
【答案】浓硫酸、加热 取代反应 乳酸 或 2-羟基丙酸 或 α-羟基丙酸 CH2=CHCOOH+CH3OH![]() CH2=CHCOOCH3+H2O
CH2=CHCOOCH3+H2O 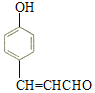 、
、 (写一种即可) 2CH3CH2OH+O2
(写一种即可) 2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O CH3CH(OH)CN
2CH3CHO+2H2O CH3CH(OH)CN
【解析】
由C与F发生题干信息反应,生成肉桂酸,可知,C中必含碳碳双键,因此确定B到C发生了醇的消去反应,C为CH2=CHCOOH,根据产物聚丙烯酸甲酯可知D为CH2=CHCOOCH3,C与甲醇发生酯化反应生成D,D发生加聚反应生成聚甲基丙烯酸甲酯;CH≡CH发生加成反应生成苯,苯发生取代反应生成F(氯苯),C(CH2=CHCOOH)与F(氯苯)发生题干信息反应,生成肉桂酸,据此分析问题。
(1)根据以上分析可知,反应①为醇的消去反应,反应条件是浓硫酸、加热;⑥的反应为CH2=CHCOOH+![]()
![]()
![]() +HCl,因此反应类型是取代反应;
+HCl,因此反应类型是取代反应;
答案:浓硫酸、加热 取代反应
(2)B为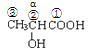 ,名称为乳酸或2-羟基丙酸或α-羟基丙酸;
,名称为乳酸或2-羟基丙酸或α-羟基丙酸;
答案:乳酸或2-羟基丙酸或 α-羟基丙酸
(3)由C制取D发生的是酯化反应,化学方程式为CH2=CHCOOH+CH3OH![]() CH2=CHCOOCH3+H2O;
CH2=CHCOOCH3+H2O;
答案:CH2=CHCOOH+CH3OH![]() CH2=CHCOOCH3+H2O
CH2=CHCOOCH3+H2O
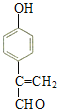
(4)肉桂酸(![]() )的同分异构体中能同时满足下列条件:①苯环上有两个取代基且苯环上的一氯代物有两种,说明两个取代基应该处于对位,②能发生银镜反应,说明有醛基,③能与FeCl3溶液发生显色反应,说明有酚羟基。符合上述要求物质的结构简式为
)的同分异构体中能同时满足下列条件:①苯环上有两个取代基且苯环上的一氯代物有两种,说明两个取代基应该处于对位,②能发生银镜反应,说明有醛基,③能与FeCl3溶液发生显色反应,说明有酚羟基。符合上述要求物质的结构简式为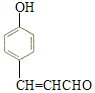 、
、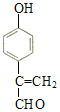 ;
;
答案: 、
、 (写一种即可)
(写一种即可)
(5)根据信息可知乙烯必须先生成C=O,才可以与HCN反应,增加碳原子数,因此确定CH2=CH2先与水发生加成反应生成X(乙醇),乙醇发生催化氧化反应生成乙醛(Y),反应的方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O;按照信息,乙醛与HCN发生加成反应Z(CH3CH(OH)CN),Z在酸性条件下与水反应生成
2CH3CHO+2H2O;按照信息,乙醛与HCN发生加成反应Z(CH3CH(OH)CN),Z在酸性条件下与水反应生成![]() ;
;
答案:2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O CH3CH(OH)CN
2CH3CHO+2H2O CH3CH(OH)CN


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列说法正确的是
A.Na2S2O3与H2SO4溶液混合产生22.4 L气体时转移电子数为2NA
B.标准状况下,22.4 L环丙烷和丙烯的混合气体中所含共用电子对数为9NA
C.常温下,1 L 0.5 mol/L CH3COONH4溶液的pH=7,则溶液中CH3COO-与NH4+的数目均为0.5NA
D.50g质量分数为46%的乙醇溶液与足量的钠反应,放出H2的分子数目为0.25NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强酸性溶液X中可能含有Fe2+、Al3+、NH4+、CO32-、SO32-、SO42-、Cl-中的若干种,现取X溶液进行连续实验,实验过程及产物如下:
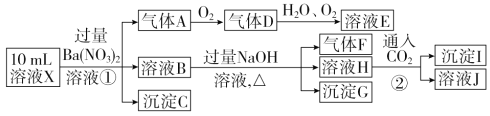
下列说法正确的是
A. X中一定存在Fe2+、Al3+、NH4+、SO42-
B. 溶液E和气体F能发生化学反应
C. X中肯定不存在CO32-、SO32-、Al3+
D. 沉淀I只有Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中药麻黄成分中含有生物碱、黄酮、鞣质、挥发油、有机酚、多糖等许多成分,其中一种有机酚的结构简式如图。下列说法正确的是 ( )
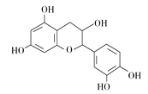
A. 分子中所有碳原子可以处于同一平面
B. 分子式为C15H12O7
C. 1 mol该有机物跟足量浓溴水反应,最多消耗5 mol Br2
D. 1 mol该有机物与NaOH溶液反应最多消耗5 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)3.01×1023个NH4+含有质子的物质的量是____ ,含有电子的物质的量是_____;
(2)200mL 2mol/L的Al2(SO4)3溶液中SO42﹣的物质的量浓度为_____ ;
(3)标准状况下,36g H2和O2组成的混合气体的体积是67.2L,则混合气体中H2和O2的体积比为______;
(4)标准状况下,将33.6LNH3溶于水配成500mL溶液,该溶液的物质的量浓度为____;
(5)已知1.505×1023个A气体分子的质量为31g,则A气体的摩尔质量是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对水样中M的分解速率的影响因素进行研究。在相同温度下,M的物质的量浓度 [c(M)]随时间(t) 变化的有关实验数据如下图所示,下列说法不正确的是( )
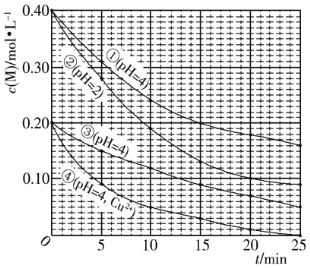
A.水样的PH越小,M的分解速率越快
B.水样中添加Cu2+,能加快M的分解速率
C.由②③得,反应物浓度越大,M的分解速率越快
D.在0~20min内,②中M的平均分解速率为0.015mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以北京大学马丁教授为代表的多个团队,研发出了高效的铁基(如FeC、Fe2C、Fe5C2、Fe3C)费托合成催化剂,以H2和CO为原料可高产率合成烯烃、烷烃,如3CO(g)+ 6H2(g)![]() CH3CH=CH2(g)+3H2O(g)、nCO+(2n+1)H2
CH3CH=CH2(g)+3H2O(g)、nCO+(2n+1)H2![]() CnH2n+2+nH2O,为煤的气化、液化使用开拓了新途径。
CnH2n+2+nH2O,为煤的气化、液化使用开拓了新途径。
(1)Fe3+中能量最高的能级上的电子云有_____种伸展方向,位于不同方向中运动的电子的能量大小关系是_________。当Fe原子电子排布由[Ar]3d64s2→[Ar]3d64s14p1时,体系的能量_______(填“增大”或“减小”)。
(2)Fe、C、O三种元素的第一电离能由大到小的顺序为_____________;CH3CH=CH2分子中碳原子的杂化轨道类型为____,题干所述反应中CO分子中断裂的化学键类型为______(填字母)。
A. 2个σ键、1个π键 B. 1个σ键、2个π键 C. 非极性键
(3)新戊烷[(CH3)4C]分子中5个碳原子形成的空间构型是____________,该分子是________(填“极性”或“非极性”)分子。随着烃分子中碳原子数目的增加,同系物的沸点升高.其原因是__________。
(4)碳铁之间可形成多种化合物,其中一种化合物的晶体结构(面心立方结构)如图所示:

则编号为①的原子的坐标为_______________;该化合物的化学式为_______________,设该晶体的晶胞多数为a pm,阿伏加德罗常数的值为NA,则该晶体的密度为_______________ g·cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,在一固定容积的密闭容器中发生反应:A(g)+B(g)![]() C(s)△H<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
C(s)△H<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是

A. T℃时,该反应的平衡常数值为4
B. c点没有达到平衡,此时反应向逆向进行
C. 若c点为平衡点,则此时容器内的温度高于T℃
D. T℃时,直线cd上的点均为平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚乳酸E在服装、卫生医疗制品等行业具有广泛的应用。某有机化合物A在一定条件下通过一系列反应可合成E;同时还可得到C和D等重要有机化合物。转化关系如下图:
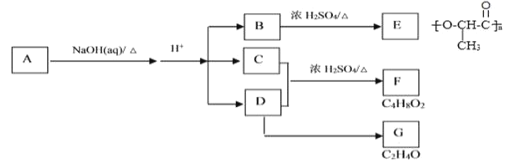
完成下列填空:
(1)B→E反应类型:____________,D→G实验室中反应条件:_______________。
(2)A的分子式:_____________。
(3)与F同类别的同分异构体还有HCOOCH(CH3)2、HCOOCH2CH2CH3和_______ (用结构简式表示)。
(4)写出实验室中判断D中有G生成的方法______________________________________________
(5)石油产品丙烯及必要的无机试剂可合成丙烯酸,设计合成路线如下:![]() 。
。
已知:![]() i.
i.
请完成合成路线中的:ClCH2CH=CH2→甲→乙→丙______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com