
| A、分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| B、1molH2O含有的原子数目为3NA |
| C、常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA |
| D、常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA |


科目:高中化学 来源: 题型:
| /s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A、反应在前50 S内的平均速率v(PCl3)=0.0032mol/(L?s) |
| B、保持其他条件不变,升高温度,平衡时c(PCl3=0.11)mol?L-1,该反应为放热反应 |
| C、相同温度下,起始时向容器中充入1.0 mol PC15、0.20 mol PC13和0.20 mo1 C12,达到平衡的v(正)>v(逆) |
| D、相同温度下,起始时向容器中充入2.0 mol PC13、2.0 mol C12,达到平衡时,PCl3的转化率小于80% |
查看答案和解析>>
科目:高中化学 来源: 题型:
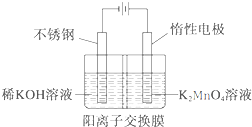 KMnO4是一种重要的氧化剂,广泛用于化学分析和化工生产.工业上可由软锰矿(主要成分为MnO2)制备,方法如下:
KMnO4是一种重要的氧化剂,广泛用于化学分析和化工生产.工业上可由软锰矿(主要成分为MnO2)制备,方法如下:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2 L NO和11.2 L SO3的分子总数为0.5NA |
| B、0.1molBr2与足量H2O或NaOH反应转移的电子数均为0.1NA |
| C、0.1mol的白磷(P4)或四氯化碳(CCl4)中所含的共价键数均为0.4NA |
| D、在精炼铜或电镀铜的过程中,当阴极析出铜32g转移电子数均为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图进行实验,试管中现象对应的离子方程式不正确的是( )
如图进行实验,试管中现象对应的离子方程式不正确的是( )| 选项 | a | b | 试管中现象 | 离子方程式 |
| A | 硫酸 | KI淀粉 | 在空气中放置一段时间后溶液呈蓝色 | 4H++4I-+O2=2I2+2H2O |
| B | 稀盐酸 | Na2CO3 | 开始时无气泡,后来有气泡 | CO32-+H+=HCO3-; HCO3-+H+=H2O+CO2↑ |
| C | 稀盐酸 | Na2SiO3 | 产生白色胶状物 | 2H++SiO32-=H2SiO3(胶体) |
| D | 硫酸 | 滴有酚酞的Ba(OH)2 | 有白色沉淀生成,溶液由红色变为无色 | Ba2++OH-+H++SO42-= BaSO4↓+H2O |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、②④⑤ |
| C、①②⑤ | D、③⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com