
【题目】S4N4的结构如图:
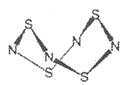
(1)S4N4的晶体类型是__。
(2)用干燥的氨作用于S2Cl2的CCl4,溶液中可制S4N4。化学反应方程为:6S2Cl2+16NH3=S4N4+S8+12NH4Cl
①上述反应过程中,没有破坏或形成的微粒间作用力是__。
a.离子键 b.极性键 c.非极性键 d.金属键 e.配位键 f.范德华力
②S2Cl2中,S原子轨道的杂化类型是__。
科目:高中化学 来源: 题型:
【题目】某学习小组拟探究CO2和锌粒反应是否生成CO,已知CO能与银氨溶液反应产生黑色固体。实验装置如图所示:

下列说法正确的是
A. 实验开始时,先点燃酒精灯,后打开活塞K
B. b、c、f中试剂依次为氢氧化钠溶液、浓硫酸、银氨溶液
C. 装置e的作用是收集一氧化碳气体
D. 用上述装置(另择试剂)可以制备氢气并探究其还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如下图所示。下列说法错误的是
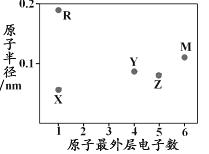
A. R的氧化物含有离子键 B. 最高价含氧酸的酸性:Z<Y
C. M的氢化物常温常压下为气体 D. Y形成的化合物种类最多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向200 mL FeBr2溶液中逐渐通入Cl2,其中n(Fe 3+)、n(Br2) 随通入n(Cl2)的变化如图所示,下列说法不正确的是( )
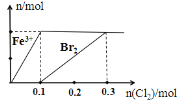
A.氧化性强弱:Br2 > Fe3+
B.由图可知,该FeBr2溶液的浓度为1 mol·L-l
C.n(Cl2) =0. 12 mol时,溶液中的离子浓度有:c (Fe 3+)∶c( Br-)=1∶8
D.n(FeBr2)∶n(Cl2) =1∶1时,反应的离子方程式为:2Fe2++2Br-+ 2Cl2=2Fe3++Br2 + 4Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科学技术的发展,阿伏加德罗常数的测定手段越来越多,测定精确度也越来越高,现有一种简单可行的测定方法,具体步骤为:
(1)将固体NaCl研细、干燥后,准确称取mgNaCl固体并转移到定容仪器A中。
(2)用滴定管向A仪器中滴加苯,不断振荡,继续加苯至A仪器的刻度线,计算出NaCl固体的体积为Vcm3。
①步骤(1)中A仪器最好用__________(仪器名称)。
②步骤(2)中用酸式滴定管好还是碱式滴定管好,__________,理由是______________。
③能否用胶头滴管代替步骤(2)中的滴定管__________;理由是____________________。
④已知NaCl晶体的结构如上图所示,用X射线测得NaCl晶体中靠得最近的Na+与Cl-间的平均距离为acm,则用上述测定方法测得阿伏加德罗常数NA的表达式为:NA=______mol-1。
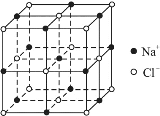
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图所示:
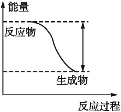
(1)该反应为_________(填“吸热”或“放热”)反应。
(2)若要使该反应的反应速率增大,下列措施可行的是_________(填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度 D.使用催化剂
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为:_________(填“正”或“负”)极,该极上发生的电极反应为:_________,外电路中电子移动方向为:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种氧化镍NiO晶体中就存在如下图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其结果晶体仍呈电中性,但此化合物中Ni和O的比值却发生了变化。某氧化镍样品组成中个数比Ni∶O=97∶100
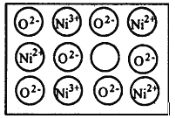
(1)写出该氧化镍样品的化学式_________________。
(2)试计算晶体中Ni2+与Ni3+的离子个数之比__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第16届海南国际车展上:展出了中国研制的新型燃料电池汽车,该车装有“绿色心脏”---质子交换膜燃料电池。某种质子交换膜燃料电池如图所示。下列说法正确的是
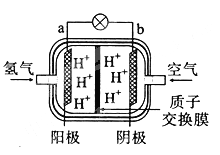
A.该电池的a极发生氧化反应B.正极反应为:O2+4e-+2H2O=4OH-
C.质子(H+)通过质子交换膜移动到a电极D.该燃料电池的能量转化率可达到100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)烷烃A在同温、同压下蒸气的密度是H2的43倍,其分子式为___________。
(2)0.1 mol 烷烃E完全燃烧,消耗标准状况下的O211.2 L,其分子式为___________。
(3)用式量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃产物的数目为____________。
(4)某有机物的结构表达式为![]() ,其名称是_______________。
,其名称是_______________。
(5)萘的结构式为![]() ,其分子式为 ,它的二氯代物又有 种。
,其分子式为 ,它的二氯代物又有 种。
(6)立方烷![]() 其分子式为 ,它的六氯代物有 种。
其分子式为 ,它的六氯代物有 种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com