
【题目】下列变化会释放出能量的是( )
A.碘升华
B.酒精用于降温
C.铝热反应
D.Ba(OH)28H2O和NH4Cl反应
科目:高中化学 来源: 题型:
【题目】实验室常用的分离操作有:①萃取分液法②结晶法③分液法④蒸馏法⑤过滤法。选择以上方法分离混合物,选择正确的是( )
A. | 饱和食盐水与沙子的混合物 | ①萃取分液法 |
B. | 水和汽油的混合物 | ④蒸馏法 |
C. | 从碘的水溶液里提取碘 | ③分液法 |
D. | 从硝酸钾和氯化钠的混合液中获得硝酸钾 | ②结晶法 |
A.A B.B C.C D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达平衡,平衡常数 ![]() .恒容时,温度升高,H2浓度减小.下列说法正确的是( )
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应的化学方程式为CO+H2OCO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组需要230mL1mol/L的Na2CO3溶液。回答下列问题:
(1)配制该溶液时,应称取Na2CO3的质量为_______g,应选用容量瓶的规格是______mL。
(2)配制时正确的操作顺序是__________(用字母表示,每个操作只能用一次)。
A.将已冷却的溶液沿玻璃棒注入容量瓶中
B.用托盘天平准确称量所需Na2CO3的质量,倒入烧杯中,再加入适量蒸馏水,用玻璃棒慢慢搅动,使其溶解
C.用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也都注入容量瓶,轻轻摇动容量瓶
D.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
E.将容量瓶瓶塞盖好,反复上下颠倒,摇勺
F.继续往容量瓶内小心加水,直到液面接近容量瓶颈刻度线下1~2cm处
(3)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”“偏低"或“无影响”)?
①没有进行C操作,所配辩液浓度___________。
②配制溶液时,容量瓶未干燥,所配溶液浓度___________。
③定容时俯视容量瓶颈刻度线,所配溶液浓度___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去杂质的方法正确的是
A.除去CO2气体中混有的CO:通入澄清石灰水洗气
B.除去氯气中混有的HCl:通过氢氧化钠溶液洗气
C.除去NaBr溶液中混有的NaCl: 加入过量Cl2,加热蒸干
D.除去NaCl固体中混有少量的I2:加热升华
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于水的电离平衡的相关说法正确的是( )
A.c(H+)= ![]() 的溶液一定呈中性
的溶液一定呈中性
B.将水加热,Kw增大,pH增大,仍呈中性
C.向0.1mol/L醋酸溶液中加水,溶液中水电离产生的c(H+)将减小
D.向水中加入少量碳酸氢钠固体,溶液的c(H+)增大,平衡逆向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在水溶液中有四种含铁型体,25 ℃时,它们的物质的量分数随pH 的变化如图所示,下列叙述错误的是
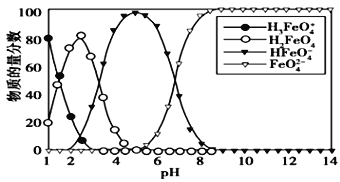
A. 向pH=5 的高铁酸盐溶液中加入KOH溶液,离子方程式为HFeO4-+OH-=FeO42-+H2O
B. 为获得尽可能纯净的高铁酸盐,应控制pH≥9
C. 已知H3FeO4+的电离平衡常数分别为:K1=2.5×10-2,K2=4.8×10-4,K3=5.0×10-8,当pH= 4时,溶液中c(HFeO4-)/ c(H2FeO4)= 1.2
D. pH=2 时,溶液中主要含铁型体浓度的大小关系为 c(H2FeO4)> c(H3FeO4+)> c(HFeO4-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硫酸盐是一种常见的食品添加剂,用如图实验可检验某食品中亚硫酸盐含量(含量通常以1kg样品中含SO2的质量计;所加试剂均足量)。下列说法不正确的是
![]()
A. 葡萄酒酿造时通入SO2起到了杀菌和增酸的作用
B. 反应①中若不通入N2则测得的SO2含量偏低
C. 反应①中煮沸的目的是加快亚硫酸的分解,降低SO2的溶解度
D. 若仅将②中的氧化剂“H2O2溶液”替换为“溴水”,对测定结果无影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com