
【题目】下列条件一定能使反应速率加快的是( )
①增加反应物的物质的量②升高温度③缩小反应容器的体积④加入生成物⑤加入MnO2
A.全部B.①②⑤C.②③D.②
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】氯气在生产生活中有广泛的用途,制取氯气的途径有多种。完成下列填空:
(1)工业上用电解饱和食盐水制取氯气,氯气在电解池的______极产生;氯气与氢氧化钠反应得到消毒剂次氯酸钠,发生反应的化学方程式为________;向次氯酸钠溶液中加入少量稀盐酸,可以增强消毒效果,这是因为生成了_____(填物质名称)。
(2)实验室制取氯气的化学方程式为MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,该反应中,氯气是______(填“氧化”或“还原”)产物;若反应过程中转移了2 mol电子,则在标准状况下可以得到_______L氯气。
MnCl2+Cl2↑+2H2O,该反应中,氯气是______(填“氧化”或“还原”)产物;若反应过程中转移了2 mol电子,则在标准状况下可以得到_______L氯气。
(3)实验室常用排饱和食盐水的方法收集氯气,请用平衡移动原理解释用饱和食盐水而不用水的原因。___________
(4)有机化工中会利用反应4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g)+Q(Q>0)来产生氯气。向5 L的密闭容器中加入0.5 mol HCl与0.2 mol O2,在一定条件下发生反应,Cl2的物质的量与时间t的关系如图中OA段所示。0~8 min时Cl2的平均反应速率为_________________。t0时刻改变某一条件,Cl2的物质的量变化曲线如图中AB段所示,则t0时改变的条件一定是__________。
2Cl2(g)+2H2O(g)+Q(Q>0)来产生氯气。向5 L的密闭容器中加入0.5 mol HCl与0.2 mol O2,在一定条件下发生反应,Cl2的物质的量与时间t的关系如图中OA段所示。0~8 min时Cl2的平均反应速率为_________________。t0时刻改变某一条件,Cl2的物质的量变化曲线如图中AB段所示,则t0时改变的条件一定是__________。
a.降低温度 b.增大压强 c.加入HCl

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验. 
(1)实验过程中铜网出现色和 色交替的现象.
(2)甲和乙两个水浴作用不相同,其中甲中装的是热水,乙中装的是冷水.他们的作用依次为 , .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2的含量是衡最大气污染的一个重要指标,工业上常采用催化还原法或吸收法处理SO2。利用催化还原SO2不仅可消除SO2污染,而且可得到有经济价值的单质S。
(1)在复合组分催化剂作用下,CH4可使SO2转化为S,同时生成CO2和H2O。
己知CH4和S的燃烧热(△H)分别为-890.3k/mol和-297.2kJ/mol,则CH4和SO2反应的热化学方程式为_____________。
(2)用H2还原SO2生成S的反应分两步完成,如图1所示,该过程中相关物质的物质的量浓度随时间的变化关系如图2所示:
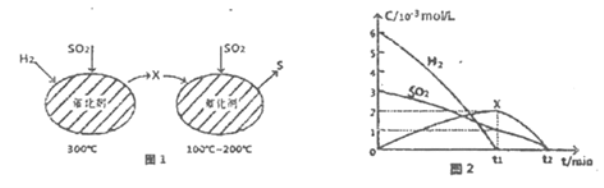
①分析可知X为______(写化学式),0~t1时间段的温度为_____,0~t1时间段用SOz表示的化学反应速率为________。
②总反应的化学方程式为_____________。
(3)焦炭催化还原SO2生成S2,化学方程式为:2C(s)+2SO2(g)![]() S2(g)+2CO2(g),恒容容器中,1mol/LSO2与足量的焦炭反应,SO2的转化率随温度的变化如图3所示。
S2(g)+2CO2(g),恒容容器中,1mol/LSO2与足量的焦炭反应,SO2的转化率随温度的变化如图3所示。

①该反应的△H____0(填“>”或“<”)
②算a点的平衡常数为_________。
(4)工业上可用Na2SO3溶液吸收法处理SO2,25℃时用1mo/L的Na2SO3溶液吸收SO2。当溶液pH=7时,溶液中各离子浓度的大小关系为________。已知:H2SO3的电离常数K1=1.3×10-2,K2=6.2×10-8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是温度和压强对反应 X+Y2Z 影响的示意图.下列叙述正确的是( ) 
A.上述可逆反应的正反应为放热反应
B.X、Y、Z 均为气态
C.X 和 Y 中只有一种是气态,Z 为气态
D.上述反应的正反应的△S<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“钢是虎,钒是翼,钢含钒犹如虎添翼”,金属钒被誉为“合金的维生素”。从废钒(主要成分为V2O5、Fe2O3、SiO2等)中回收V2O5的一种工艺流程如下图所示: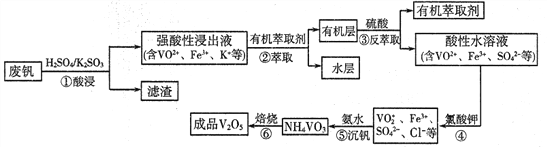
已知:步骤②、③中的变化过程可简化为:Rn+(水层)+nHA(有机层)![]() RAn(有机层)+nH+(水层)(式中Rn+表示VO2+或Fe3+,HA表示有机萃取剂)。
RAn(有机层)+nH+(水层)(式中Rn+表示VO2+或Fe3+,HA表示有机萃取剂)。
回答下列问题:
(1)步骤①酸浸过程中发生氧化还原反应的化学方程式为______________。
(2)萃取时应加入适量碱的作用是___________________。
(3)步骤④中反应的离子方程式为___________________。
(4)步骤⑤25°C时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
通过表中数据分析,在实际生产中,⑤中加入氨水,调节溶液的最佳pH范围为______;
若加入氨水调节溶液pH=2,钒沉淀率达到93%且不产生Fe(OH)3沉淀,则此时溶液中c(Fe3+)<_____mol/L(按25℃计算,25℃时Ksp[Fe(OH)3]=2.6×10-39)。
(5)V2O5是两性氧化物,在强酸性溶液中以VO2+形式存在,VO2+具有强氧化性,能将I-氧化为I2,本身被还原为VO+,则V2O5与氢碘酸反应的离子方程式为_________________。
(6)为提高钒的回收率,步骤②和③需多次进行,假设酸浸所得“强酸性浸出液”中c(VO2+)=amol/L,步骤②和③每进行一次,VO2+萃取率为80%,4次操作后,“强酸性浸出液中”c(VO2+)=_______mol/L(萃取率=![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,现象和结论均正确的是
选项 | ① | ② | ③中现象 | 结论 | 装置图 |
A | 浓硝酸 | Cu | 淀粉-KI溶液变蓝 | NO2为氧化性气体 |
|
B | 稀硫酸 | Na2SO3 | 品红溶液褪色 | Na2SO3未变质 | |
C | 浓盐酸 | MnO2 | FeBr2溶液变为黄色 | 氧化性:Cl2>Br2 | |
D | 浓氨水 | NaOH | 湿润红色石蕊试纸变蓝 | NH3为碱性气体 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二胺(H2NCH2CH2NH2) 与NH3相似,水溶液呈碱性,25℃时,向10mL0.1mol·L-1乙二胺溶液中滴加0.1 mol·L-1盐酸,各组分的物质的量分数δ随溶液pH的变化曲线如图所示,下列说法错误的是

A. 混合溶液呈中性时,滴加盐酸的体积小于10mL
B. Kb2[H2NCH2CH2NH2] 的数量级为10-8
C. a 点所处的溶液中:c(H+)+3c([H3NCH2CH2NH3]2+)=c(OH-) +(Cl-)
D. 水的电离程度:a>b
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com