
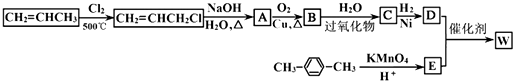
| �������� |
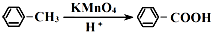
 ��D��E����ˮ�ⷴӦ���ɸ߾���WΪ
��D��E����ˮ�ⷴӦ���ɸ߾���WΪ ���ݴ˽��
���ݴ˽�� ��D��E����ˮ�ⷴӦ���ɸ߾���WΪ
��D��E����ˮ�ⷴӦ���ɸ߾���WΪ ��
�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
�� ����ͬ���칹�壺����FeCl3��Һ����ɫ�����з��ǻ��� �ڿɷ���������Ӧ���ۿ���NaHCO3��Һ����CO2�������Ȼ���ȩ��������������ͬ���칹���У�
����ͬ���칹�壺����FeCl3��Һ����ɫ�����з��ǻ��� �ڿɷ���������Ӧ���ۿ���NaHCO3��Һ����CO2�������Ȼ���ȩ��������������ͬ���칹���У�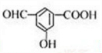 ȡ������λ�ÿ��Ի������ʴ�Ϊ��
ȡ������λ�ÿ��Ի������ʴ�Ϊ�� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ӵ������������������ת���� |
| B�������¶������ڰ����ĺϳ� |
| C��������ˮ���µķ������ϳɻ�������еİ���Һ�� |
| D���˷���������ϳɰ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2 | B��6 | C��8 | D��14 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ba��OH��2��Һ�еμ�ϡ���Ba2++2OH-+2 H++SO42-=BaSO4��+2H2O |
| B����CH3COOH�ܽ�CaCO3��CaCO3+2H+�TCa2++H2O+CO2�� |
| C��NH4HCO3���ڹ�����KOH��Һ�У�HCO3-+OH-�TCO32-+H2O |
| D�������ʵ�����MgCl2��Ba��OH��2��HCl��Һ��ϣ�Mg2++2OH-�TMg��OH��2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
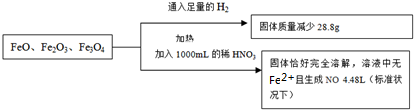
| A��3.8mol?L-1 |
| B��4.0mol?L-1 |
| C��4.4mol?L-1 |
| D��3.6mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ũ���� |
| 170�� |
| Br2 |
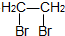
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
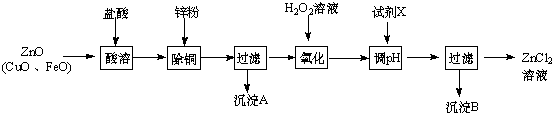
| �������� | ��ʼ������pH | ������ȫ��pH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.2 | 6.4 |
| Fe2+ | 5.8 | 8.8 |
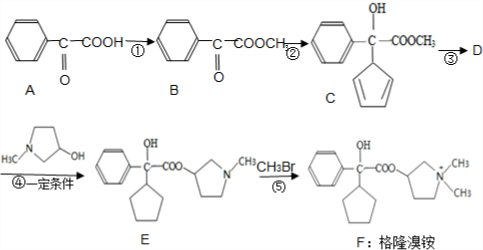
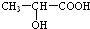 �����ɱ�������C6H8O4���;����ᣬ�������Ľṹ��ʽΪ
�����ɱ�������C6H8O4���;����ᣬ�������Ľṹ��ʽΪ�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com