
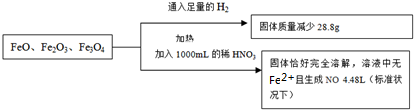
| A、3.8mol?L-1 |
| B、4.0mol?L-1 |
| C、4.4mol?L-1 |
| D、3.6mol?L-1 |
| 28.8g |
| 16g/mol |
| 4.48L |
| 22.4L/mol |
| 4.4mol |
| 1L |


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
| A、乙烷与氯气在光照条件下发生加成反应 |
| B、将石蜡油(液态烷烃混合物)加强热分解生成的气体都是烷烃 |
| C、甲苯能够使溴的四氯化碳溶液和酸性的高锰酸钾溶液褪色 |
| D、乙醇能够被酸性的高锰酸钾溶液直接氧化成乙酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.03mol |
| B、0.045mol |
| C、0.0225mol |
| D、0mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、核裂变是一种化学变化 |
| B、131I 与127I互为同素异形体 |
| C、131I 原子的中子数为78 |
| D、碘在周期表中位于第四周期ⅦA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
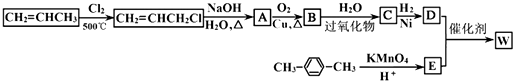
| 过氧化物 |
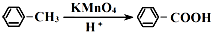
查看答案和解析>>
科目:高中化学 来源: 题型:
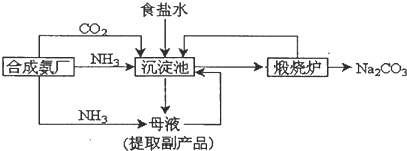
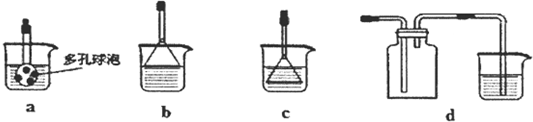
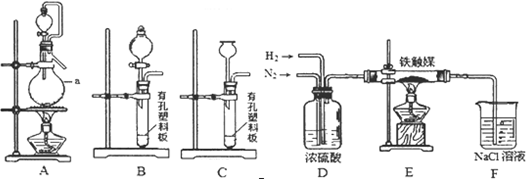
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、相同质量的Na2CO3和NaHCO3与足量盐酸作用时,碳酸氢钠反应速率更快,产生的气体质量相同 |
| B、NaHCO3俗名:小苏打.Na2CO3俗名:大苏打 |
| C、Na2CO3和NaHCO3均可与澄清石灰水反应 |
| D、Na2CO3和NaHCO3均可与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将纳米Fe3O4分散在水中没有丁达尔现象 |
| B、将纳米Fe3O4分散在水中Fe3O4不能透过滤纸 |
| C、每生成1 mol Fe3O4反应转移的电子数为4 NA |
| D、反应物OH-的化学计量数x=2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com