
| A.由水电离出的c(H+)=1.0×10-12mol·L-1 |
| B.加水稀释后,溶液中所有离子的浓度均减少 |
| C.2c(H+)= c(SO42-)+ c(OH-) |
| D.滴加稀氨水使pH=7,则c(NH4+)=" 2" c(SO42-) |
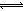 H++OH—中氢离子和氢氧根离子的浓度之比等于系数之比,则由水电离出的c(H+)=1.0×10-12mol·L-1,故A正确;硫酸溶液呈酸性,加水稀释后,酸性减弱,氢离子、硫酸根离子浓度均减小,但温度不变水的离子积不变,即溶液中氢离子浓度与氢氧根离子浓度的乘积不变,所以溶液中氢氧根离子浓度一定增大,故B错;硫酸溶液中含有氢离子、硫酸根离子和氢氧根离子,根据电荷守恒原理可得:c(H+)="2" c(SO42-)+ c(OH-),故C错;无论量的多少,稀硫酸与氨水混合后溶液只有铵根离子、氢离子、硫酸根离子和氢氧根离子,根据电荷守恒规律可得:c(NH4+)+c(H+)="2" c(SO42-)+ c(OH-),由于滴加稀氨水使pH=7,则该溶液中c(NH4+)="2" c(SO42-),故D正确。
H++OH—中氢离子和氢氧根离子的浓度之比等于系数之比,则由水电离出的c(H+)=1.0×10-12mol·L-1,故A正确;硫酸溶液呈酸性,加水稀释后,酸性减弱,氢离子、硫酸根离子浓度均减小,但温度不变水的离子积不变,即溶液中氢离子浓度与氢氧根离子浓度的乘积不变,所以溶液中氢氧根离子浓度一定增大,故B错;硫酸溶液中含有氢离子、硫酸根离子和氢氧根离子,根据电荷守恒原理可得:c(H+)="2" c(SO42-)+ c(OH-),故C错;无论量的多少,稀硫酸与氨水混合后溶液只有铵根离子、氢离子、硫酸根离子和氢氧根离子,根据电荷守恒规律可得:c(NH4+)+c(H+)="2" c(SO42-)+ c(OH-),由于滴加稀氨水使pH=7,则该溶液中c(NH4+)="2" c(SO42-),故D正确。

科目:高中化学 来源:不详 题型:单选题
A.H2O2的电子式为 |
| B.4℃时,纯水的pH<7,溶液呈中性 |
| C.0℃、101kPa,水分子间距:固态>液态 |
| D.101kPa,不同状态水的能量:固态>液态>气态 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(H+)+c(NH4+)=c(OH-) |
| B.与等体积等浓度的氯化铵溶液混合c(NH4+)+c(NH3· H2O)="0.02" mol·L-1 |
| C.与等体积等浓度的盐酸混合后所得溶液显酸性 |
| D.由H2O电离出的c(H+)=1.0×10-12 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若将c1mol/L的醋酸冲稀10倍,则其pH增大1 |
| B.若将c2 mol/L的氢氧化钠溶液冲稀10倍,则其pH减小1 |
| C.若c1? V1=c2?V2,则混合液中c(CH3COO-)=c(Na+) |
| D.若混合液的pH=7,则混合液中c(CH3COO-)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.Ⅱ为氯化铵稀释时pH值变化曲线,a点水的电离程度大于c点水的电离程度 |
| B.b点溶液中水的电离程度比c点溶液中水的电离程度大,且两点的KW相同 |
| C.a点时,等体积的两溶液与NaOH反应消耗的NaOH量相同 |
| D.加入足量NaOH,b点溶液消耗的NaOH比d点溶液消耗的多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.与煤油、柴油相比较,天然气是一种比较清洁的化石燃料 |
| B.乙醇是一种可再生能源,作为燃料的优点的是完全燃烧的产物不污染环境 |
| C.利用太阳能、风能和氢能等能源替代化石能源能有效改善空气质量 |
| D.煤的气化和液化不仅可以获得洁净燃料,而且再燃烧会放出更多的热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.大于7 | B.小于7 | C.等于7 | D.三种都有可能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com