
【题目】向一定量的Cu、Fe2O3、的混合物中加入300mL 1mol/L的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+原混合物中Cu的质量为( )
A.9.6g
B.6.4g
C.3.2g
D.1.6g
【答案】C
【解析】解:Cu、Fe2O3的混合物中加入300mL 1molL﹣1的盐酸溶液,恰好使混合物完全溶解,所得溶液中不含Fe3+ , 溶液中溶质为氯化铜、氯化亚铁,该反应过程为:盐酸与氧化铁恰好反应生成氯化铁与水、生成的氯化铁与铜恰好反应转化为氯化铜、氯化亚铁,由水的分子式H2O可知,氧化物中2n(O)=n(HCl)=0.3L×1mol/L=0.3mol,故n(O)=0.15mol,
则混合物中氧化铁的物质的量为:n(Fe2O3)= ![]() n(O)=0.05mol,
n(O)=0.05mol,
根据铜与氧化铁的反应关系式Cu~Fe2O3可知,Cu的物质的量为0.05mol,质量为64g/mol×0.05mol=3.2g,
故选C.


科目:高中化学 来源: 题型:
【题目】钛被称为继铁、铝之后的第三金属,制备金属钛的一种流程如下:

回答下列问题:
(1)基态钛原子的价电子排布图为___________________,其原子核外共有_____种运动状态不相同的电子。金属钛晶胞如下图2所示,为________________堆积(填堆积方式)。
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l-l >> l-b > b-b(l为孤对电子对,b为键合电子对),则关于H2O中的H-O-H键角可得出的结论是________。
A.180° B.接近120°,但小于120°
C.接近120°,但大于120° D.接近109°28’,但小于109°28’
(3)已知TiCl4在通常情况下是无色液体,熔点为–37℃,沸点为136℃,可知TiCl4为______晶体。
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图1。化合物乙的沸点明显高于化合物甲,主要原因是___________________________。化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为__________________。

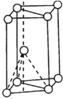
图1 图2
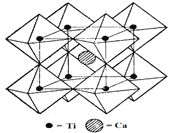
(5)钙钛矿晶体的结构如右图所示。钛离子位于立方晶胞的角顶,被_______个氧离子包围成配位八面体;钙离子位于立方晶胞的体心,被__________个氧离子包围。钙钛矿晶体的化学式为_______。若该晶胞的边长为a pm,则钙钛矿晶体的密度为______________g.cm-3(只要求列算式,不必计算出数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是Al2O3 , 含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
请回答下列问题.
(1)流程甲加入盐酸后生成Al3+的离子方程式为 .
(2)流程乙加入烧碱后生成SiO ![]() 的离子方程式为 .
的离子方程式为 .
(3)验证滤液B含Fe3+ , 可取少量滤液并加入(填试剂名称)
(4)滤液E、K中溶质的主要成分是(填化学式),写出该溶质的一种用途. .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列说法正确的是
A.葵花籽油、人造奶油、牛油均属于高级脂肪酸高级酯
B.无法通过质谱图分析区分乙醇和乙酸乙酯
C.因为人体中没有水解纤维素的酶,所以食用富含纤维素的食品没有意义
D.石油裂解、煤的干馏、玉米制醇、纤维素制火棉都是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表前四周期的一部分,下列 有关R,W,X,Y,Z 5种元素的叙述中,正确的是( ) 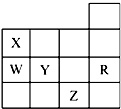
A.常压下5种元素的单质中Z单质的沸 点最高
B.Y,Z的阴离子电子层结构都与R原子的相同
C.Y元素的非金属性比W元素的非金属性强
D.W的氢化物的还原性比Y的氢化物的还原性弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. Si是常用的半导体材料,可以制作光电池
B. 用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后通足量的CO2
C. 二氧化硅不与任何酸反应,可用石英制造耐酸容器
D. 不能用石英坩埚加热熔化氢氧化钠固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在强碱性溶液中可以大量共存的是( )
A. K+、Na+、HCO3-、Cl-B. Na+、Ba2+、AlO2-、NO3-
C. NH4+、K+、Cl-、NO3-D. K+、Na+、Cu2+、S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别向下列溶液中加入少量的过氧化钠固体,不会出现浑浊的是 ( )
A.Na2CO3溶液
B.FeCl3溶液
C.饱和Ca(OH)2溶液
D.CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g) ![]() 2Z(g)+W(s) ΔH<0,下列叙述正确的是 ( )
2Z(g)+W(s) ΔH<0,下列叙述正确的是 ( )
A. 平衡常数K值越大,X的转化率越大
B. 达到平衡时,反应速率v正(X)=2v逆(Z)
C. 达到平衡后降低温度,正向反应速率减小的倍数大于逆向反应速率减小的倍数
D. 达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com