
【题目】有机物的结构简式如图,则此有机物可发生的反应类型有( )
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和 ⑧加聚.
A.①②③⑤⑥
B.②③④⑤⑥⑧
C.②③④⑤⑥⑦
D.①②③④⑤⑥⑦⑧
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式不正确的是( )
A. 铁与稀盐酸反应:2 Fe+6H+=2Fe3++3H2↑
B. 氢氧化钠溶液与盐酸反应:OH-+H+=H2O
C. 锌与硫酸铜溶液反应:Zn+Cu2+=Zn2++Cu
D. 氯化钡溶液与稀硫酸反应:SO42-+Ba2+= BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二草酸合铜(Ⅱ)酸钾{K2[Cu(C2O4)2]2H2O}制备流程如图1: 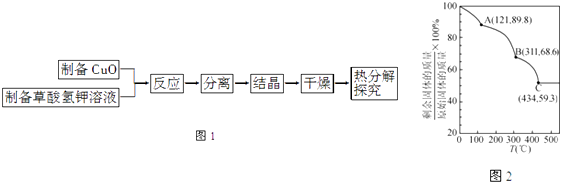
(已知H2C2O4 ![]() CO↑+CO2↑+H2O)
CO↑+CO2↑+H2O)
(1)制备CuO:CuSO4溶液中滴入NaOH溶液,加热煮沸、冷却、双层滤纸过滤、洗涤.①用双层滤纸的可能原因是 .
②用蒸馏水洗涤氧化铜时,如何证明已洗涤干净:
(2)本实验用K2CO3粉末与草酸溶液制取KHC2O4溶液而不用KOH粉末代替K2CO3粉末的可能原因是 .
(3)为了提高CuO的利用率,如何让CuO充分转移到热的KHC2O4溶液中:;50℃水浴加热至反应充分,发生反应的化学方程式为;再经趁热过滤、沸水洗涤、将滤液蒸发浓缩得二草酸合铜(Ⅱ)酸钾晶体.
(4)若实验室只有含少量FeSO47H2O的硫酸铜晶体,欲制备较纯净的CuSO4溶液.
Ⅰ.相关数据(开始沉淀的pH按金属离子浓度为1.0molL﹣1计算):
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Cu2+ | 4.7 | 6.7 |
Fe2+ | 5.8 | 8.8 |
Ⅱ.提供的试剂有:a.蒸馏水 .稀硫酸 .H2O2溶液 d.纯净的Cu(OH)2粉末 .氨水
需经过的步骤有:①、②、③、④过滤得CuSO4溶液.
(5)将制得的K2[Cu(C2O4)2]2H2O进行热重分析,结果如图2,由图2知在C点剩余固体为K2CO3和 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+3C+S===K2S+N2↑+3CO2↑。
(1)其中被还原的元素是________,被氧化的元素是_________,氧化剂是_________,还原剂是_________,氧化产物是_________,还原产物是__________。
(2)用双线桥标出电子转移的方向和数目:2KNO3+ 3C+ S ═ K2S + N2↑+ 3CO2↑________。
(3)当0.1molCO2生成时,则转移的电子数为___________个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有等体积混合而成的四组气体:①NO2+NO;②NO2+O2;③HCl+N2;④NO+N2 , 将其分别通入体积相同的试管,并立即倒立于水槽中,试管内水面上升的高度分别为H1 , H2 , H3 , H4 , 其中高度关系是( )
A.H2>H3>H1>H4
B.H3>H2>H1>H4
C.H1=H2=H3=H4
D.H1>H2>H3>H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应:2Na2O2+2H2O===4NaOH+O2↑,下列说法中正确的是 ( )。
A. Na2O2是氧化剂,H2O是还原剂
B. Na2O2既是氧化剂,又是还原剂
C. 该反应中电子转移的数目为4e-
D. 氧气是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有二价铜离子的电解质溶液会呈现出蓝色且溶液颜色随着铜离子浓度加大而加深。若想知道铜离子浓度,可以用 测量。
A. 比色计B. 酸碱指示剂C. pH计D. pH试纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需用480 mL 1.0 mol·L-1的NaOH溶液。下图是某学生在实验室配制该NaOH溶液的过程示意图。请回答下列问题:

(1)用已知质量为25.6 g的表面皿准确称取NaOH固体。首先在托盘天平的右盘上放置砝码的质量是_____ g(最小的砝码质量为1.0 g);然后将游码___________;在左盘的表面皿中加入NaOH固体。若指针偏向右边,下面他的操作应该是______。
(2)观察配制NaOH溶液的过程示意图,指出其中有错误的是__________(填操作序号)。如果配制过程中没有等到溶液冷却到室温,则配制所得溶液的浓度将__________(填“偏高”、“偏低”或“不变”)。
(3)在上述实验过程中,用到的容量瓶的规格是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com