
����Ŀ��ijͬѧ��ͼ����ʾװ�ü����ģ��ⶨ̼��������ᷴӦ����CO2��������淴Ӧʱ��仯����������Ƴ�ͼ����ʾ���ߣ��йط�������ȷ���ǣ� �� 
A.CaCO3������ķ�ӦΪ���ȷ�Ӧ
B.�ռ���������ʱ���Ϊt1��t2
C.ƽ����Ӧ���ʣ�v��t1��t2����v��t2��t3����v��0��t1����v��t3��t4��
D.��t4���ռ�����CO2���岻�����ӣ�һ����̼�������ȫ��Ӧ
���𰸡�D
���������⣺A��t1��t2�淴Ӧ�Ľ��У���Ӧ���Ũ���Ǽ�С����������������˵����Ӧ�¶����ߣ��÷�Ӧ���ȣ���A��ȷ��
B������ͼ��֪��б��������t1��t2 �� ����������죬��ͬ��ʱ�����ռ���������࣬��B��ȷ��
C��ͼ����б�ʴ�С��K��t1��t2����K��t2��t3����K��0��t1����K��t3��t4����б�ʾ�Խ��Ӧ����Խ������ƽ����Ӧ���ʣ�v��t1��t2����v��t2��t3����v��0��t1����v��t3��t4������C��ȷ��
D����t4���ռ�������������������ӣ�˵����Ӧ������һ���Ѿ������꣬�������̼�������ȫ��Ӧ����D����
��ѡD��
�����㾫�����������ȷ�Ӧ�ͷ��ȷ�Ӧ����Ŀ�����жϼ��ɵõ��𰸣���Ҫ��֪��ѧ�ϰ����������Ļ�ѧ��Ӧ��Ϊ���ȷ�Ӧ����ѧ�ϰѷų������Ļ�ѧ��Ӧ��Ϊ���ȷ�Ӧ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ������֮Դ�����й���ˮ��˵����ȷ����
A.ˮ�Ƿǵ����
B.pH=6.8�Ĵ�ˮ������
C.�����¶ȣ�ˮ��Kw����
D.���ˮ������������ʱ�������м�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʡ���庽�����ѧ2017�������ʮһ��ģ�⣨5�£������ۺϻ�ѧ���⡿ ͼ1Ϊ�����������װ��ʾ��ͼ��ͼ2Ϊ�������[CO(NH2)2]�ļ�����Һ����װ��ʾ��ͼ(�����и�Ĥ����ֹ����ͨ��������������Ϊ���Ե缫)��

ͼ1 �����������װ�� ͼ2 ������صļ�����Һ����װ��
������������ȷ������ ��
A. ͼ1��N�Ͱ뵼��Ϊ������P�Ͱ뵼��Ϊ����
B. ͼ2��Һ�е��Ӵ�B������A��
C. X2����
D. ����ʱ��A���ĵ缫��ӦʽΪCO(NH2)2 + 8OH- - 6e- = CO32- + N2��+ 6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ҫ����0.2 mol/L��NaCl��Һ450 mL������ʱѡ�õ�����ƿ�Ĺ���Ӧ��ȡ��NaCl�ֱ��� �� ��
A. 450 mL��5.27 g B. 500 mL��5.85 g C. 450 mL��5.85 g D. 500 mL��5.27 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ�NA��ʾ����٤�������� �� ��
A. 28g N2�����е�ԭ����ΪNA
B. 18g��NH4�� ����������11NA
C. 22.4LCH4��������NA��������ӵ�����֮�����
D. ��״���£�22.4LCH4��O2�Ļ�����������еķ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ���(PCl5)���л��ϳ�����Ҫ���Ȼ���,���������Ȼ���(PCl3)�Ȼ��õ�:
PCl3(g)+Cl2(g)![]() PCl5(g)����H=-93.0 kJ��mol-1��ij�¶���,���ݻ��㶨Ϊ2.0 L���ܱ������г���2.0 mol PCl3��1.0 mol Cl2,һ��ʱ���Ӧ��ƽ��״̬,ʵ���������±���ʾ:
PCl5(g)����H=-93.0 kJ��mol-1��ij�¶���,���ݻ��㶨Ϊ2.0 L���ܱ������г���2.0 mol PCl3��1.0 mol Cl2,һ��ʱ���Ӧ��ƽ��״̬,ʵ���������±���ʾ:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl5)/mol | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(1)0��150 s�ڵ�ƽ����Ӧ����v(PCl3)=________mol��L-1��s-1��
(2)���¶���,�˷�Ӧ�Ļ�ѧƽ�ⳣ������ֵΪ____(���÷�����ʾ)��
(3)��Ӧ��250 sʱ,�÷�Ӧ�ų�������Ϊ________kJ��
(4)���й���������Ӧ��˵����,��ȷ����______(����ĸ)��
a.�����Ƿ��ƽ��״̬,���������ܶ�ʼ�ղ���
b.300 sʱ,�����¶�,�����淴Ӧ����ͬʱ����
c.350 sʱ,����ܱ������г��뵪��,ƽ��������Ӧ�����ƶ�
d.��ͬ������,����ʼ����ܱ������г���1.0 mol PCl3��0.2 mol Cl2,�ﵽ��ѧƽ��״̬ʱ,n(PCl5)<0.20 mol
(5)�¶�T1ʱ,���������PCl5�����������ʱ��t�仯��ʾ��ͼ���ϡ�����������ͬ,������ͼ�л����¶�ΪT2(T2>T1)ʱ,PCl5�����������ʱ��仯������________��
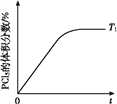
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ����������ȷ���ǣ� ��
A.
ͼ�ɱ�ʾ����������Ԫ�ص�ԭ�Ӱ뾶��ԭ�������ı仯����
B.
ͼ�ɱ�ʾ�ڶ���������Ԫ��������������ԭ�������ı仯����
C.
ͼ�ɱ�ʾCH4��Cl2��������Ӧ����CH3Cl����������Ӧ��Ϊ���ȷ�Ӧ
D.
ͼ�ɱ�ʾһ�������£��ϳɰ���Ӧ�����淴Ӧ������ʱ��ı仯����t1��t2 ʱ�䣺v������Ӧ��=v���淴Ӧ����0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����п�����������Ǧ���أ����Ĺ��ɲ�����п��������ij�ֵ������Һ���������ܷ�Ӧʽ�ǣ�2Zn+O2�T2ZnO����õ�صĸ���������������������1mol����ͨ��ʱ�����������ĵ�O2�ڱ�״���µ������ ��
�����ASES��˾��Ƶ�����������DZͧ��Һ����Һ��ȼ�ϵ����ͼ��ʾ����ȼ�ϵ�ع���ʱ�������ĵ缫��ӦʽΪ����ص��ܷ�ӦΪ �� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���������ˮ��Һ���ܹ�������������� ��
A. H����CO32�D �� NO3�D B. Ba2���� SO42�D��NO3�D
C. Na+��Clһ��HCO3�D D. Ag����K����Cl�D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com