
【题目】下列说法中正确的是(NA表示阿伏伽德罗常数) ( )
A. 28g N2所含有的原子数为NA
B. 18g的NH4+ 离子中含有电子数11NA
C. 22.4LCH4的质量与NA个甲烷分子的质量之和相等
D. 标准状况下,22.4LCH4和O2的混合气体所含有的分子数为NA
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.SO2(g)+H2 O(g)=H2SO3(l),该过程熵值增大
B.SO2(g)= S(s)+O2(g); △H>0, △S<0,该反应能自发进行
C.3S(s)+2H2O(1)= SO2(g)+2H2S(g),室温下能自发进行
D.若某反应的△H<0,△S>0,则该反应一定能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016年普通高等学校招生全国统一考试(新课标Ⅱ卷)】酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉,MnO2,ZnCl2和NH4Cl等组成的糊状填充物,该电池在放电过程产生MnOOH,回收处理该废电池可得到多种化工原料,有关数据下表所示:
溶解度/(g/100g水)
温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-17 | 10-17 | 10-39 |
回答下列问题:
(1)该电池的正极反应式为 ,电池反应的离子方程式为 。
(2)维持电流强度为0.5A,电池工作五分钟,理论上消耗Zn g。(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过____分离回收;滤渣的主要成分是MnO2、______和 ,欲从中得到较纯的MnO2,最简便的方法是 ,其原理是 。
(4)用废电池的锌皮制备ZnSO4·7H2O的过程中,需去除少量杂质铁,其方法是:加稀硫酸和H2O2溶解,铁变为_____,加碱调节至pH为 时,铁刚好完全沉淀(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全);继续加碱调节至pH为_____时,锌开始沉淀(假定Zn2+浓度为0.1mol/L)。若上述过程不加H2O2后果是 ,原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用图甲所示装置及器材,测定碳酸钙与盐酸反应生成CO2气体体积随反应时间变化情况,并绘制出图乙所示曲线.有关分析不正确的是( ) 
A.CaCO3与盐酸的反应为放热反应
B.收集气体最多的时间段为t1~t2
C.平均反应速率:v(t1~t2)>v(t2~t3)>v(0~t1)>v(t3~t4)
D.在t4后,收集到的CO2气体不再增加,一定是碳酸钙已完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表中对应关系正确的是( )
A | ① | 均为加成反应 |
B | ①CH3CH3+Cl2 | 均为取代反应 |
C | ① | 均为加聚反应 |
D | ①C(s)+CO2(g)═2CO(g) | 均为△H>0的反应 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2是实验室常见的强氧化剂,在医疗上可用作消毒剂等. 
(1)实验室可用Na2O2与H2SO4反应制取少量的H2O2 , Na2O2的电子式为 .
(2)一种正在开发的利用O2和H2O作原料通过化合制取H2O2的方法,其原理如1图所示.该方法制取H2O2
的总化学反应方程式为
(3)医疗上可用质量分数为3%过氧化氢溶液对伤口进行消毒,其消毒原理是 .
(4)为探究外界条件对H2O2分解化学反应速率的影响,相关实验设计如表所示:
试管编号 | 实验目的 | H2O2溶液 | 温度 | 水的体积/mL | FeCl3溶液体积/mL | |
质量分数 | 体积/mL | |||||
Ⅰ | 为编号Ⅱ实验参照 | 12% | 5.0 | 常温 | 0 | 0 |
Ⅱ | 温度对反应速率的影响 | 5.0 | 60℃ | 0 | 0 | |
Ⅲ | 为编号Ⅳ实验参照 | 4.0% | 5.0 | 常温 | 0 | |
Ⅳ | 4.0% | 5.0 | 常温 | 0 | 1.0 | |
填写表中缺少的内容:Ⅱ;Ⅲ;Ⅳ .
(5)由铂(Pt)和金(Au)组成的纳米棒放入H2O2溶液中(如下图),纳米棒将发生定向移动.
则:Au一侧为电池的极(选填:“正”或“负”);纳米棒向(选填:“左”或“右”)移动.
(6)断裂1mol过氧化氢中的O﹣O键和氧气中的O=O键所需的能量依次分别为142kJmol﹣1、497.3kJmol﹣1 . 则反应2H2O2(l)═2H2O(l)+O2(g)△H=kJmol﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是常见四种有机物的比例模型示意图.下列说法正确的是( ) 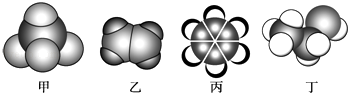
A.甲能使酸性高锰酸钾溶液褪色
B.乙可与溴水发生加成反应使溴水褪色
C.丙与溴水可以发生取代反应
D.丁在稀硫酸作用下可与乙酸发生取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com