
【题目】H2O2是实验室常见的强氧化剂,在医疗上可用作消毒剂等. 
(1)实验室可用Na2O2与H2SO4反应制取少量的H2O2 , Na2O2的电子式为 .
(2)一种正在开发的利用O2和H2O作原料通过化合制取H2O2的方法,其原理如1图所示.该方法制取H2O2
的总化学反应方程式为
(3)医疗上可用质量分数为3%过氧化氢溶液对伤口进行消毒,其消毒原理是 .
(4)为探究外界条件对H2O2分解化学反应速率的影响,相关实验设计如表所示:
试管编号 | 实验目的 | H2O2溶液 | 温度 | 水的体积/mL | FeCl3溶液体积/mL | |
质量分数 | 体积/mL | |||||
Ⅰ | 为编号Ⅱ实验参照 | 12% | 5.0 | 常温 | 0 | 0 |
Ⅱ | 温度对反应速率的影响 | 5.0 | 60℃ | 0 | 0 | |
Ⅲ | 为编号Ⅳ实验参照 | 4.0% | 5.0 | 常温 | 0 | |
Ⅳ | 4.0% | 5.0 | 常温 | 0 | 1.0 | |
填写表中缺少的内容:Ⅱ;Ⅲ;Ⅳ .
(5)由铂(Pt)和金(Au)组成的纳米棒放入H2O2溶液中(如下图),纳米棒将发生定向移动.
则:Au一侧为电池的极(选填:“正”或“负”);纳米棒向(选填:“左”或“右”)移动.
(6)断裂1mol过氧化氢中的O﹣O键和氧气中的O=O键所需的能量依次分别为142kJmol﹣1、497.3kJmol﹣1 . 则反应2H2O2(l)═2H2O(l)+O2(g)△H=kJmol﹣1 .
【答案】
(1)![]()
(2)O2+2H2O ![]() 2H2O2
2H2O2
(3)H2O2使病毒蛋白质发生变性,失去活性
(4)12%;1.0;催化剂对反应速率的影响
(5)正;右
(6)﹣213.3
【解析】解:(1)过氧化钠为离子化合物,阳离子是钠离子,阴离子是过氧根离子,据此写出电子式为: ![]() ,所以答案是:
,所以答案是: ![]() ;(2)利用O2和H2O作原料通过化合制取H2O2的条件是电解,则总反应方程式为:O2+2H2O
;(2)利用O2和H2O作原料通过化合制取H2O2的条件是电解,则总反应方程式为:O2+2H2O ![]() 2H2O2 , 所以答案是:O2+2H2O
2H2O2 , 所以答案是:O2+2H2O ![]() 2H2O2;(3)过氧化氢有强氧化性,对伤口进行消毒,其消毒原理是H2O2使病毒蛋白质发生变性,失去活性,所以答案是:H2O2使病毒蛋白质发生变性,失去活性;(4)实验Ⅰ和实验Ⅱ的温度不同,要探究温度对反应速率的影响,其他条件要相同,则Ⅱ中双氧水的质量分数应与Ⅰ相同,为12%;实验Ⅲ用了催化剂,Ⅳ没有使用,可知这两个实验是探究催化剂对反应速率的影响,要求其他条件相同,控制溶液总体积相同就可使反应物浓度相同,则Ⅲ中应加蒸馏水1.0mL,所以答案是:12%;1.0;催化剂对反应速率的影响;(5)由图2可知铂(Pt)和金(Au)组成的纳米棒与H2O2溶液形成原电池,H2O2中在铂极失电子发生氧化反应生成氧气和氢离子,氢离子移向正极(Au),纳米棒将向右移动,所以答案是:正;右;(6)2H2O2(l)═2H2O(l)+O2(g)反应物中有4molH﹣O,2molO﹣O,生成物中有4molH﹣O,1molO=O,△H=反应物的键能总和﹣生成物的键能总和=2×142kJmol﹣1﹣497.3kJmol﹣1=﹣213.3kJmol﹣1 , 所以答案是:﹣213.3.
2H2O2;(3)过氧化氢有强氧化性,对伤口进行消毒,其消毒原理是H2O2使病毒蛋白质发生变性,失去活性,所以答案是:H2O2使病毒蛋白质发生变性,失去活性;(4)实验Ⅰ和实验Ⅱ的温度不同,要探究温度对反应速率的影响,其他条件要相同,则Ⅱ中双氧水的质量分数应与Ⅰ相同,为12%;实验Ⅲ用了催化剂,Ⅳ没有使用,可知这两个实验是探究催化剂对反应速率的影响,要求其他条件相同,控制溶液总体积相同就可使反应物浓度相同,则Ⅲ中应加蒸馏水1.0mL,所以答案是:12%;1.0;催化剂对反应速率的影响;(5)由图2可知铂(Pt)和金(Au)组成的纳米棒与H2O2溶液形成原电池,H2O2中在铂极失电子发生氧化反应生成氧气和氢离子,氢离子移向正极(Au),纳米棒将向右移动,所以答案是:正;右;(6)2H2O2(l)═2H2O(l)+O2(g)反应物中有4molH﹣O,2molO﹣O,生成物中有4molH﹣O,1molO=O,△H=反应物的键能总和﹣生成物的键能总和=2×142kJmol﹣1﹣497.3kJmol﹣1=﹣213.3kJmol﹣1 , 所以答案是:﹣213.3.
【考点精析】认真审题,首先需要了解反应热和焓变(在化学反应中放出或吸收的热量,通常叫反应热).


科目:高中化学 来源: 题型:
【题目】氨是制造化肥和生产其他化工产品的原料,由氨生产的四种化工产品的说法不正确的是( ) 
A.H2NCH2COOH是一种氨基酸
B.CO(NH2)2与NH4CNO性质相同
C.聚丙烯腈的单体为:CH2═CHCN
D.依据酸碱质子理论,HCO3﹣属于酸碱两性物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是(NA表示阿伏伽德罗常数) ( )
A. 28g N2所含有的原子数为NA
B. 18g的NH4+ 离子中含有电子数11NA
C. 22.4LCH4的质量与NA个甲烷分子的质量之和相等
D. 标准状况下,22.4LCH4和O2的混合气体所含有的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不正确的是( )
A.
图可表示短周期主族元素的原子半径随原子序数的变化规律
B.
图可表示第二周期主族元素最外层电子数随原子序数的变化规律
C.
图可表示CH4与Cl2经两步反应生成CH3Cl,则两步反应均为放热反应
D.
图可表示一定条件下,合成氨反应正、逆反应速率随时间的变化,则t1~t2 时间:v(正反应)=v(逆反应)≠0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图示中物质转化最终生成乙酸和高分子涂料胶黏剂Y的合成路线如下(部分反应条件已省略): 
(1)化合物CH2═CHCOOH中所含官能团名称为和 .
(2)正丁烷的一种同分异构体的结构简式为;Y的结构简式为 .
(3)图中8步反应中,原子利用率没有达到100%的为(填序号).
(4)写出下列反应的化学方程式(注明反应条件):反应⑥为;反应⑧为(同时有水生成) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应式是:2Zn+O2═2ZnO.则该电池的负极材料是;当导线中有1mol电子通过时,理论上消耗的O2在标准状况下的体积是 .
②瑞典ASES公司设计的曾用于驱动潜艇的液氨﹣液氧燃料电池如图所示,该燃料电池工作时,负极的电极反应式为;电池的总反应为 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有短周期主族元素X,Y,Z,R,T;R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成化学式为Z2T的离子化合物.五种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( ) 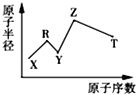
A.原子半径和离子半径均满足:Y<Z
B.最高价氧化物对应的水化物的酸性:T<R
C.气态氢化物的稳定性:Y>T
D.由X,Y,Z,T四种元素组成的化合物水溶液一定呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关营养成分与人体健康的关系叙述错误的是( )
A.缺铁会患贫血症B.为防治佝偻病,过量补钙
C.摄入淀粉量不足,会患低血糖D.食用蔬菜.水果可以补充维生素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应可视为旧键断裂和新键形成的过程.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJmol﹣1):P﹣P:198P﹣O:360O═O:498,则生成1mol P4O6该反应P4(白磷)+3O2═P4O6中的能量变化为( ) 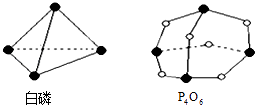
A.吸收1638 kJ能量
B.放出1638 kJ能量
C.吸收126 kJ能量
D.放出126 kJ能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com