
【题目】甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、CO32-、SO42-中的不同阳、阴离子各一种组成已知:
①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;
②0.1mol/L乙溶液中c(H+)>0.1mol/L;
③向丙容器中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。
(1)甲是_____________,乙是_____________,丙是_____________,丁是_____________。
(2)50mL含Na2SO4、Na2CO3的混合溶液中加入过量的甲溶液,得到14.51g白色沉淀,向白色沉淀中加入过量的稀HNO3充分反应后,沉淀减少到4.66g,并有气体产生。
①写出产生气体的离子方程式:______________________________;
②混合溶液中Na+的物质的量的浓度是_________。
【答案】氢氧化钡 硫酸 氯化镁 碳酸铵 BaCO3+2H+=Ba2++H2O+CO2↑ 2.8mol/L
【解析】
(1)①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成,离子组合后发现生成的沉淀应是:碳酸钡、硫酸钡、氢氧化镁,所以甲是:氢氧化钡;
②0.1mol/L乙溶液中c(H+)>0.1mol/L,说明乙是二元强酸,所以乙是:硫酸;
③向丙容器中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成,说明丙中含有Cl-,且丙、丁都易溶于水,故丙为:氯化镁,丁是:碳酸铵;
(2)Ba(OH)2和Na2SO4生成BaSO4不溶于硝酸,Ba(OH)2和Na2CO3反应生成BaCO3溶于硝酸,所以不溶的4.66g是BaSO4;
(1)①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成,离子组合后发现生成的沉淀应是:碳酸钡、硫酸钡、氢氧化镁,所以甲是:氢氧化钡,
②0.1mol/L乙溶液中c(H+)>0.1mol/L,说明乙是二元强酸,所以乙是:硫酸,
③向丙容器中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成,说明丙中含有Cl-,且丙、丁都易溶于水,故丙为:氯化镁,丁是:碳酸铵,
本题答案为:氢氧化钡、硫酸、氯化镁、碳酸铵;
(2)设50mL混合溶液中,含Na2SO4、Na2CO3的物质的量分别为:x、y,根据反应的化学方程式可知: Na2SO4![]() BaSO4 ; Na2CO3
BaSO4 ; Na2CO3![]() BaCO3
BaCO3
1mol:233g = x:4.66g ; 1mol:197g= y:(14.51g-4.46g)
解得:x=![]() =0.02mol,y=
=0.02mol,y=![]() =0.05mol,n(Na+)=2
=0.05mol,n(Na+)=2![]() (0.02+0.05)mol=0.14mol,c(Na+)=
(0.02+0.05)mol=0.14mol,c(Na+)=![]() =2.8mol/L,产生气体的离子方程式为:BaCO3+2H+=Ba2++H2O+CO2↑,
=2.8mol/L,产生气体的离子方程式为:BaCO3+2H+=Ba2++H2O+CO2↑,
本题答案为:BaCO3+2H+=Ba2++H2O+CO2↑,2.8mol/L。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法错误的是
A. 标准状况下,2.24LH2S中含有0.1NA个H2S分子
B. 常温常压下,7.0g由丁烯与丙烯组成的混合气体中含有的氢原子数目为NA
C. 常温下,将2.7g铝片投入足量的浓硫酸中,转移电子的数目为0.3NA
D. 向1L的密闭容器中充入46gNO2气体,容器中氮原子的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质属于同系物的是( )
A. ![]() 与
与![]() B. CH3CH2Cl与CH2ClCH2CH2Cl
B. CH3CH2Cl与CH2ClCH2CH2Cl
C. C2H5OH与CH3OH D. CH3CH2CH3与CH2=CHCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水氯化铝是常用的有机化工试剂,易水解、易升华。实验室用以下装置制取少量氯化铝,反应原理为2Al+6HCl(g) ![]() 2AlCl3+3H2。以下说法正确的是
2AlCl3+3H2。以下说法正确的是
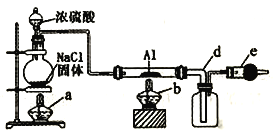
A. 圆底烧瓶中发生反应:NaCl+H2SO4(浓) ![]() HCl↑+NaHSO4
HCl↑+NaHSO4
B. 粗导管d也可换成细导管
C. e中试剂可选用碱石灰、无水氧化钙或五氧化二磷
D. 为了减少HCl的浪费,实验开始时先点燃b处酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水溶液中的行为是中学化学的重要内容,按要求回答下列问题.
(1)在醋酸水溶液中存在平衡CH3COOH![]() CH3COO-+H+若分别改变下列条件:①加水稀释②加热③加少量固体醋酸钠,其中能使醋酸电离程度增大的是_______,能使溶液pH增大的是_______(填序号)。
CH3COO-+H+若分别改变下列条件:①加水稀释②加热③加少量固体醋酸钠,其中能使醋酸电离程度增大的是_______,能使溶液pH增大的是_______(填序号)。
(2)常温下,0.1mol·L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3-、CO32-、OH-四种微粒的浓度由大到小的顺序为:________________________________。
(3)AlCl3溶液加热蒸干并灼烧最终得到物质是________(填化学式),将NaHCO3与Al2(SO4)3溶液混合后可做泡沫灭火剂,其原理是_______(用离子方程式表示)。
(4)已知下列物质在20℃下的Ksp如下:
化学式 | AgCl | AgBr | AgI |
颜色 | 白色 | 浅黄色 | 黄色 |
Ksp | 2.0×10-10 | 5.4×10-13 | 8.3×10-17 |
①当向含相同浓度Cl-、Br-、I-的溶液中滴加AgNO3溶液时,_______先沉淀(填离子符号),
②向BaCl2溶液中加入AgNO3和KBr,当两种淀共存时,  =__________。
=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
已知: ① Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O ② SO2+SeO2+ H2O ![]() Se + SO42-+ H+
Se + SO42-+ H+
(1)依据Se与浓H2SO4的反应,写出Se和浓HNO3(还原产物为NO2)反应的化学方程式:__________________。
(2)Se与浓HNO3的反应中,氧化剂是_______, 反应中被还原的元素是_______。当有标准状况下33.6LNO2气体生成时,转移电子的物质的量是________mol。
(3)依据反应①②, 判断SeO2、浓H2SO4、SO2的氧化性由强到弱的顺序是__________。
(4) 配平反应②, 并用双线桥法标出电子转移的方向和数目:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质能使品红溶液褪色,且褪色原理基本相同的是( )
①活性炭 ②新制氯水 ③二氧化硫 ④臭氧 ⑤过氧化钠 ⑥双氧水
A.①②④
B.②③⑤
C.②④⑤⑥
D.③④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com