
【题目】下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,据此,下列说法正确的是( )

A. 该硫酸的物质的量浓度为9.2 molL-1
B. 配制200 mL 4.6 molL-1的稀硫酸需取该硫酸25 mL
C. 该硫酸与等体积的水混合后所得溶液浓度为9.2 molL-1
D. 该硫酸与等体积水混合后质量分数大于49%
【答案】D
【解析】
A、该硫酸的物质的量浓度为:c=1000ρw%/M=(1000×1.84×98%/98)mol/L=18.4mol/L,故A项错误;
B、根据稀释定律,稀释前后溶质的物质的量不变,设浓硫酸的体积为xmL,则xmL×18.4mol/L=200mL×4.6mol/L,计算得出:x=50,所以应量取的浓硫酸体积是50mL,错误;
C、浓硫酸与等体积的水混合,根据C1V1=C2V2,C2=C1V1 /V2,混合后密度减小V2<2V1,所以浓度大于9.2mol/L,错误;
D、硫酸与等体积的水混合,密度发生变化,设取浓硫酸体积VL,密度为ρ1,加入VL水后,密度为ρ2,![]() ,
,![]() ,故混合后溶液的质量分数大于49%,D正确;
,故混合后溶液的质量分数大于49%,D正确;
答案选D。


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】下图中的每一个方格表示有关的一种反应物或生成物,其中A、C为无色气体
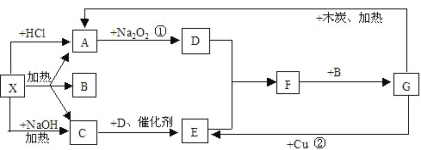
(1)写出有关物质的化学式X:_______;F_______
(2)写出A→D的化学方程式____________
(3)写出实验室制备C的化学方程式_______
(4)C可用于制备尿素,尿素CO(NH2)2适用于各种土壤,在土壤中尿素发生水解,生成两种气体,其水解的化学方程式是______
(5)分别取两份50mLNaOH溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入0.1mol/L的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl的体积之间的关系如图所示,试
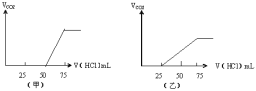
①NaOH在吸收A气体后,乙图所示溶液中存在的溶质是:_____,其物质的量之比是:_________
②原NaOH溶液的物质的量浓度是_______mol/L,甲图所示溶液最多还能吸收A体积为_____mL(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的是
A. 向含0. 1 mol Na2SiO3的溶液中滴加盐酸,生成的H2SiO3胶体中胶粒的数目为0.1NA
B. 常温常压下,1.8g甲基(—CD3)中含有的中子数为NA
C. 常温下,1L pH=10的氨水溶液中,发生电离的水分子数为1×10-10 NA
D. 7.8gNa2O2分别与过量的CO2和过量的SO2充分反应,转移的电子数目均为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向200 mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应后,得到Na2CO3和NaHCO3的混合溶液。向上述所得溶液中,逐滴滴加2 mol·L-1的盐酸,所得气体的体积与所加盐酸体积的关系如图所示。

(1)OA段、AB段发生反应的离子方程式为_________________、__________________。
(2)B点时,反应所得溶液中溶质的物质的量浓度是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室采用气相还原法制备纳米级Fe,其流程如图所示:
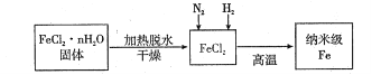
(1)纳米级Fe和稀盐酸反应的离子方程式为__________。
(2)如何将FeCl2·nH2O固体加热脱水制得无水FeCl2________(用简要文字描述)。
(3)生成纳米级Fe的化学方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】G、Q、X、Y、Z均为氯的含氧化合物,我们不了解它们的分子式(或化学式),但知道它们在一定条件下具有如下的转化关系(未配平): ① G → Q + NaCl ② Q + H2O →溶液X + H2 (电解时发生)③ Y + NaOH → G + Q + H2O ④ Z + NaOH → Q + X + H2O这五种化合物中氯的化合价由低到高的顺序为 ( )
A. ZXGYQB. GYZQXC. GYQZXD. QGZYX
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里通常用MnO2与浓盐酸反应制取氯气,其反应的化学方程式为:MnO2 + 4HCl(浓) ![]() MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
(1)用单线桥法表示该反应电子转移的方向和数目:___________。
(2)在该反应中,如有1 mol Cl2生成,被氧化的HCl的物质的量是___________,转移电子的数目是_____________。
(3)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与ClO3-物质的量之比为1∶1的混合液,反应的化学方程式是 _________________________ 。
(4)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com