
����Ŀ����NA��ʾ�����ӵ�������ֵ������˵������ȷ����
A. ��0. 1 mol Na2SiO3����Һ�еμ����ᣬ���ɵ�H2SiO3�����н�������ĿΪ0.1NA
B. ���³�ѹ�£�1.8g��(��CD3)�к��е�������ΪNA
C. �����£�1L pH=10�İ�ˮ��Һ�У����������ˮ������Ϊ1��10-10 NA
D. 7.8gNa2O2�ֱ��������CO2������SO2��ַ�Ӧ��ת�Ƶĵ�����Ŀ��Ϊ0.1NA
���𰸡�C
��������
A. �γɽ����ɢ�ʵķ��ӻ���Ӿۼ��壬�����0. 1 mol Na2SiO3����Һ�еμ����ᣬ���ɵ�H2SiO3�����н�������ĿС��0.1NA��A����
B. ��CD3��Ħ������Ϊ18g/mol��1.8g��CD3�����ʵ���Ϊ0.1mol��������Ϊ0.9 NA��B����
C. pH=10�İ�ˮ��Һ�У�ˮ�������������Ũ��Ϊ![]() ����1Lˮ������������ӵ����ʵ���n=
����1Lˮ������������ӵ����ʵ���n=![]() ������
������![]() ��֪�����������ˮ�����ʵ���Ϊ
��֪�����������ˮ�����ʵ���Ϊ![]() ���ʷ��������ˮ������Ϊ1��10-10 NA��C��ȷ��
���ʷ��������ˮ������Ϊ1��10-10 NA��C��ȷ��
D. Na2O2��CO2��ӦΪ-1�۵�O�����绯��Ӧ������SO2��Ӧ���Ƕ���������+4�۵�S��������+6����۲�ͬ��ת�Ƶ�������ͬ��D����
�ʴ�ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں�Fe3+��S2O82����I���Ļ����Һ�У���ӦS2O82��(aq)+2I��(aq)=2SO42��(aq)+I2(aq)�ķֽ��������Ӧ�����е������仯���£�
�������2Fe3+(aq)+2I��(aq)=I2(aq)+2Fe2+(aq)
�������2Fe2+(aq)+S2O82��(aq)=2Fe3+(aq)+2SO42��(aq)
�����йظ÷�Ӧ��˵����ȷ����
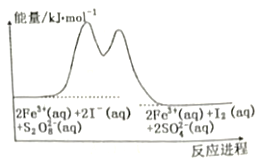
A. ��ѧ��Ӧ������Fe3+Ũ�ȵĴ�С�й�
B. �÷�ӦΪ���ȷ�Ӧ
C. Fe2+�Ǹ÷�Ӧ�Ĵ���
D. ������Fe3+��������Ӧ�Ļ�ܱ��淴Ӧ�Ĵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.ʵ����Ҫ����500 mL 0.2 mol/L NaOH��Һ����ش��������⣺
��1�����ƹ����в���Ҫʹ�õĻ�ѧ������________������ĸ����
A �ձ� B 500 mL����ƿ C ©�� D ��ͷ�ι� E ������
��2����������ƽ��ȡ�������ƣ�������Ϊ________ g��
��3��������Ҫ�����������ȷ˳����________������ţ���
�ٳ�ȡһ���������������ƣ������ձ��У�����������ˮ�ܽ⣻
�ڼ�ˮ��Һ��������ƿƿ���̶�����1��2 cmʱ�����ý�ͷ�ιܵμ�����ˮ����Һ����̶������У�
�۴���ȴ�����º���Һת�Ƶ�500 mL����ƿ�У�
�ܸǺ�ƿ�����������µߵ���ҡ�ȣ�
������������ˮϴ���ձ��ڱںͲ�����2��3�Σ�ϴ��Һת�Ƶ�����ƿ�С�
��4�����ʵ�������ȱ�ٲ���ݣ���ʹ���Ƴ���NaOH��ҺŨ��_______������ƫ�ߡ�ƫ������������������
��.��ͼʵ����ijŨ�����Լ�ƿ��ǩ�ϵ��й����ݣ��Ը��ݱ�ǩ�ϵ��й����ݻش��������⣺
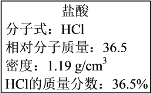
��1����Ũ������HCl�����ʵ���Ũ��Ϊ______ mol/L��
��2��ȡ����������ĸ�������Һʱ�������������в�����ȡ����Ķ��ٶ��仯����______��
A ��Һ��HCl�����ʵ������� B ��Һ��Ũ��
C ��Һ��Cl������Ŀ D ��Һ���ܶ�
��3��ijѧ����������Ũ���������ˮ����500 mL���ʵ���Ũ��Ϊ0.400 mol/L��ϡ���ᡣ��ѧ����Ҫ��ȡ______mL����Ũ����������ơ�
��.����0.27Kg��������Ϊ10����CuCl2��Һ,����Һ��CuCl2�����ʵ���Ϊ___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
����ε���Ҫ����Ϊ�������Ρ������(KIO3)�������軯��[K4Fe(CN)6��3H2O]�����������軯�ص���ˮ���ڸ����»ᷢ���ֽ⣺3K4[Fe(CN)6]![]() 2(CN)2��+12KCN+N2��+Fe3C+C
2(CN)2��+12KCN+N2��+Fe3C+C
��ش��������⣺
��1����Fe2+��̬��������Ų�ʽΪ_____��
��![]() �Ŀռ乹��Ϊ______����������������
�Ŀռ乹��Ϊ______����������������
�ۣ�CN��2������̼ԭ���ӻ��������Ϊ_______��һ����CN-��Ϊ�ȵ�����ķ��ӵĵ���ʽΪ_______��
��1molFe(CN)63�к�����������ĿΪ____mol��
��2�������Fe(CO)x������ԭ�Ӽ۵������������ṩ������֮��Ϊ18����x��___��Fe(CO)x�����³�Һ̬���۵�Ϊ��20.5�棬�е�Ϊ103�棬�����ڷǼ����ܼ����ݴ˿��ж�Fe(CO)x��������____(�������)��
��3����ͼ�Ǵ����������Ӿ���Fe3O4��ȡ�����������侧��ṹ��һ�������壬����������Dz���Fe3O4�ľ���______(����������������)�������������������Ӵ���������Χ�ɵ�________(��ռ�ṹ)��϶��
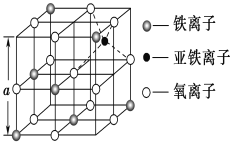
��4��Fe���γɶ������������FeO�����ṹΪNaCl�͡�������ʵ���ϴ��ڿ�λ����λ������ԭ�ӵ�ȱ�ݣ�����ȱ�ݶԾ�������ʻ�����ش�Ӱ�졣���ھ���ȱ�ݣ��ھ�����Fe��O�ĸ����ȷ����˱仯����ΪFexO��x��1���������ijFexO�����ܶ�Ϊ5.71gcm��3�������߳�Ϊ4.28��10��10 m����FexO��x=____�����ô���ʽ��ʾ����Ҫ���������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ���ҵ�Թ��ú���ᷢչ������Ҫ�����塣��ԭ��Ϊ��N2(g)��3H2(g) ![]() 2NH3(g) ��H����92.4 kJ/mol���ݴ˻ش��������⣺
2NH3(g) ��H����92.4 kJ/mol���ݴ˻ش��������⣺
(1)�ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��______________��
�ڸ����¶ȶԻ�ѧƽ���Ӱ����ɿ�֪�����ڸ÷�Ӧ���¶�Խ�ߣ���ƽ�ⳣ����ֵԽ________��
(2)ij�¶��£�����10 mol N2��30 mol H2�������Ϊ10 L���ܱ������ڣ���Ӧ�ﵽƽ��״̬ʱ����û�������а����������Ϊ20%������¶��·�Ӧ��K��________(���÷�����ʾ)��
(3)���ںϳɰ���Ӧ���ԣ������й�ͼ��һ����ȷ����(ѡ�����)________��
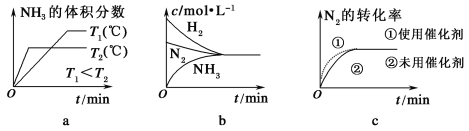
(4)��ͬ�¶��£��к����ܱ�����A�ͺ�ѹ�ܱ�����B���������о�����1 mol N2��3 mol H2����ʱ�������������ȡ���һ�������·�Ӧ�ﵽƽ��״̬��A��NH3���������Ϊa���ų�����Q1 kJ��B��NH3���������Ϊb���ų�����Q2 kJ����a________b(����>��������������<������ͬ)��Q1________Q2��Q1________92.4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijNa2CO3��NaAlO2�Ļ����Һ����μ���1mol/L�����ᣬ�����Һ�е�CO32-��HCO3-��AlO2-��Al3+�����ʵ��������������Һ������仯��ϵ��ͼ��ʾ��������˵����ȷ����
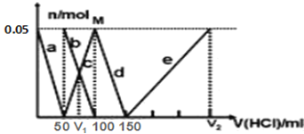
A. a���߱�ʾ�����ӷ���ʽΪ��AlO2-+4H+=Al3++2H2O
B. M��ʱ���ɵ�CO2Ϊ0.05mol
C. ԭ�����Һ�е�CO32-��AlO2-�����ʵ���֮��Ϊ1��2
D. V1��V2=1��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧѧϰС����ij�ִ��ν����ᴿʵ�飬������ͼ��ʾ����֪�����к��е�����������ҪΪ��Mg2+��Ca2+��Fe3+��SO42-��
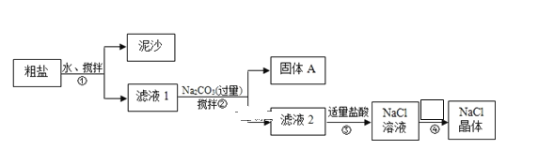
��1������ٺ͢ڵIJ���������___������Ҫ��������Ϊ___��
��2����������ڼ���Na2CO3��Һ֮ǰ����������NaOH��Һ��BaCl2��Һ������A�ǣ�___��___��Fe(OH)3 ��BaSO4��BaCO3 (�û�ѧʽ��ʾ)
��3��������м���SO42-������ȫ�IJ����ǣ�___��
��4��������м��������������(�����ӷ���ʽ��ʾ)___��
��5������ܵIJ���Ϊ��___�����ˡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص������Լ���ǩ�ϵIJ������ݣ��ݴˣ�����˵����ȷ���ǣ� ��

A. ����������ʵ���Ũ��Ϊ9.2 molL-1
B. ����200 mL 4.6 molL-1��ϡ������ȡ������25 mL
C. ��������������ˮ��Ϻ�������ҺŨ��Ϊ9.2 molL-1
D. ������������ˮ��Ϻ�������������49%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25�棬��20 mL 0.1 mol��L-1��ˮ��Һ����μ���0.1 mol��L-1HCl��Һ����pH������������Һ���(V/mL)�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���� (����)
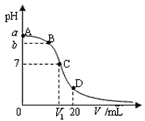
A. ��V=10mLʱ����Һ�д��ڣ� c(H+)+c(NH4+)=c(NH3��H2O)+c(OH-)
B. A��C����һ�㣬��Һ���ܴ��ڣ�c(NH4+)��c(Cl-)��c(OH-)��c(H+)
C. ��C�㣬V1��10mL������ c(NH4+)��c(Cl-)��c(OH-)��c(H+)
D. ��D�㣬���ڣ�c(NH4+)��c(NH3��H2O)>c(Cl-)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com